
【题目】电离平衡常数(用Ka表示)的大小可以判断电解质的相对强弱.25℃时,有关物质的电离平衡常数如表所示:
化学式 | HF | H2CO3 | HClO |
电离平衡常数(Ka) | 7.2×10﹣4 | K1=4.4×10﹣7 | 3.0×10﹣8 |
(1)将浓度为0.1molL﹣1 HF溶液加水稀释一倍(假设温度不变),下列各量增大的是 .
A.c(H+)
B.c(H+)c(OH﹣)
C.![]()
D.![]()
(2)25℃时,在20mL 0.1molL﹣1氢氟酸中加入V mL 0.1molL﹣1 NaOH溶液,测得混合溶液的pH变化曲线如图所示,下列说法正确的是 . 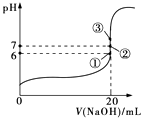
A.pH=3的HF溶液和pH=11的NaF溶液中,由水电离出的c(H+)相等
B.①点时pH=6,此时溶液中c(F﹣)﹣c(Na+)=9.9×10﹣7 molL﹣1
C.②点时,溶液中的c(F﹣)=c(Na+)
D.③点时V=20mL,此时溶液中c(F﹣)<c(Na+)=0.1molL﹣1
(3)物质的量浓度均为0.1molL﹣1的下列四种溶液:①Na2CO3溶液;②NaHCO3溶液;③NaF溶液;④NaClO溶液.依据数据判断pH由大到小的顺序是 .
(4)Na2CO3溶液显碱性是因为CO32﹣水解的缘故,请设计简单的实验事实证明之 .
(5)长期以来,一直认为氟的含氧酸不存在.1971年美国科学家用氟气通过细冰末时获得HFO,其结构式为H﹣O﹣F.HFO与水反应得到HF和化合物A,每生成1mol HF转移mol电子.
【答案】
(1)CD
(2)BC
(3)①④②③(或①>④>②>③,用物质名称表示也对)
(4)在碳酸钠溶液中滴入酚酞溶液变红,再加入BaCl2溶液后产生沉淀且红色褪去或变浅
(5)2
【解析】解:(1)A、加水稀释能促进氢氟酸的电离,溶液中氢离子浓度降低,故A错误;
B、温度不变,水的离子积常数不变,故B错误;
C、溶液中氢离子浓度和氢氟酸浓度都降低,该分式中都乘以氟离子浓度得氢氟酸的电离常数除以负离子浓度,电离常数不变,负离子浓度减小,所以其比值增大,故C正确;
D、溶液中氢氧根离子浓度增大,氢离子浓度减小,故D正确;
所以答案是:CD;(2)A.酸能抑制水的电离,含有弱根离子的盐能促进水的电离,故A错误;
B.c(F﹣)﹣c(Na+)=c(H+)﹣c(OH﹣),故B正确;
C.溶液呈中性,氢离子浓度等于氢氧根浓度,所以氟离子浓度等于钠离子浓度,故C正确;
D.③点时V=20 mL,溶液呈碱性,根据溶液呈电中性知,钠离子浓度大于氟离子浓度,故D错误;
所以答案是:BC;(3)根据相应酸的酸性强弱判断,氢氟酸的酸性大于碳酸的,碳酸的酸性大于次氯酸的,所以顺序为①④②③(或①>④>②>③,用物质名称表示也对),
所以答案是:①④②③(或①>④>②>③,用物质名称表示也对);(4)在碳酸钠溶液中滴入酚酞溶液变红,再加入BaCl2溶液后,碳酸根离子能够与钡离子反应生成碳酸钡沉淀,碳酸根离子浓度降低,若红色褪去或变浅,可以证明,所以答案是:在碳酸钠溶液中滴入酚酞溶液变红,再加入BaCl2溶液后产生沉淀且红色褪去或变浅;(5)HFO与水反应生成氢氟酸和双氧水,每生成1 mol HF转移2 mol电子,所以答案是:2.
【考点精析】通过灵活运用弱电解质在水溶液中的电离平衡,掌握当弱电解质分子离解成离子的速率等于结合成分子的速率时,弱电解质的电离就处于电离平衡状态;电离平衡是化学平衡的一种,同样具有化学平衡的特征.条件改变时平衡移动的规律符合勒沙特列原理即可以解答此题.


 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】下列离子方程式中,能正确表示盐的水解反应的是( )
A.NH4++H2ONH3H2O+H+
B.Fe3++3H2O═Fe(OH)3↓+3H+
C.S2﹣+2H2O═H2S+2OH﹣
D.Br﹣+H2O═HBr+OH﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用括号中的试剂除去各组物质中的杂质,可选试剂不正确的是( )
A.乙醇中的水(新制CaO)
B.乙烷中乙烯(溴水)
C.苯中的甲苯(溴水)
D.乙酸乙酯中的乙酸(饱和Na2CO3溶液)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.1mol/L的K2SO4溶液、0.2mol/L的Al2(SO4)3溶液和纯水混合,要使混合液中的K+、Al3+、SO42﹣的浓度分别为0.1mol/L、0.1mol/L、0.2mol/L,则所取的K2SO4溶液、Al2(SO4)3溶液、纯水三者体积比( )
A.1:1:1
B.2:1:2
C.1:1:2
D.2:1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
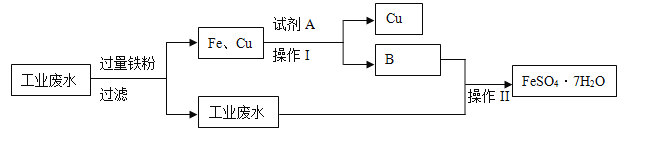
【题目】某工厂的工业废水中含有大量的FeSO4 、较多的Cu2+ 、H+和少量的Na+。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。其一种生产工艺如下:
回答下列问题:
(1)写出工业废水中加入过量铁粉发生化学反应离子方程式,并用“单线桥”表示电子转
移方向和数目_________________________。
(2)试剂A化学式___________;生成物B化学式__________。
(3)操作I的名称________,操作II的名称______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 漂白粉有效成分是氯酸钙
B. 液氯是纯净物,而氯水是混合物
C. 碘化钾水溶液能使淀粉变蓝
D. 氯气通入水中能置换出氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的乙烷完全燃烧,使所有的气体按顺序通过装有无水氯化钙和氢氧化钾的硬质玻璃管,氢氧化钾管的质量增加了4.4g,则乙烷在标准状况下体积( )
A.0.56L
B.1.12L
C.2.24L
D.3.36L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将l00ml 1mol/L 的NaHCO3溶液等分为两份,其中一份加入少许冰醋酸,另外一份加入少许Ba(OH)2固体,忽略溶液体积变化。两份溶液中c(CO32-)的变化分别是
A.减小、减小B.减小、增大C.增大、增大D.增大、减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com