
【题目】乙酰苯胺是常用的医药中间体,可由苯胺与乙酸制备。反应的化学方程式如下:![]() +CH3COOH
+CH3COOH![]()
![]() +H2O
+H2O
某实验小组分别采用以下两种方案合成乙酰苯胺:
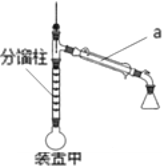
方案甲:采用装置甲:在圆底烧瓶中加入5.0mL苯胺、7.4mL乙酸,加热至沸,控制温度计读数100~105℃,保持液体平缓流出,反应40 min后停止加热即可制得产品。
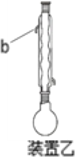
方案乙:采用装置乙:加热回流,反应40 min后停止加热。其余与方案甲相同。
已知:有关化合物的物理性质见下表:
化合物 | 密度(g·cm-3) | 溶解性 | 熔点(℃) | 沸点(℃) |
乙酸 | 1.05 | 易溶于水,乙醇 | 17 | 118 |
苯胺 | 1.02 | 微溶于水,易溶于乙醇 | –6 | 184 |
乙酰苯胺 | — | 微溶于冷水,可溶于热水,易溶于乙醇 | 114 | 304 |
请回答:
(1)仪器a的名称是_________
(2)分别从装置甲和乙的圆底烧瓶中获得粗产品的后续操作是____________
(3)装置甲中分馏柱的作用是______________
(4)下列说法正确的是__________
A.从投料量分析,为提高乙酰苯胺产率,甲乙两种方案均采取的措施是乙酸过量
B.实验结果是方案甲的产率比方案乙的产率高
C.装置乙中b处水流方向是出水口
D.装置甲中控制温度计读数在118℃以上,反应效果会更好
(5)甲乙两方案获得的粗产品均采用重结晶方法提纯。操作如下:
①请选择合适的编号,按正确的操作顺序完成实验(步骤可重复或不使用)
____→____→____→____→过滤→洗涤→干燥
a冷却结晶 b加冷水溶解 c趁热过滤 d活性炭脱色 e加热水溶解
上述步骤中为达到趁热过滤的目的,可采取的合理做法是___________
②趁热过滤后,滤液冷却结晶。一般情况下,有利于得到较大的晶体的因素有_____
A.缓慢冷却溶液 B.溶液浓度较高
C.溶质溶解度较小 D.缓慢蒸发溶剂
③关于提纯过程中的洗涤,下列洗涤剂中最合适的是_____________。
A.蒸馏水 B.乙醇 C.5%Na2CO3溶液 D.饱和NaCl溶液
【答案】直形冷凝管 将圆底烧瓶中的液体趁热倒入盛有100 mL水的烧杯,冷却后有乙酰苯胺固体析出,过滤得粗产物 利用分馏柱进行多次气化和冷凝,使醋酸和水得到有效的分离,或“可提高引馏体与外部空气热交换效率,从而使柱内温度梯度增加,使不同沸点的物质得到较好的分离。” ABC e d c a 将玻璃漏斗放置于铜制的热漏斗内,热漏斗内装有热水以维持溶液的温度,进行过滤(即过滤时有保温装置)或趁热用减压快速过滤 AD A
【解析】
两套装置都是用来制备乙酰苯胺的,区别在于甲装置使用分馏柱分离沸点在100℃至105℃左右的组分,主要是水,考虑到制备乙酰苯胺的反应可逆,这种做法更有利于获得高的转化率;题干中详细提供了乙酸,苯胺和乙酰苯胺的物理性质,通过分析可知,三者溶解性和熔点上存在较明显的差异,所以从混合溶液中获得乙酰苯胺粗品的方法就是利用溶解性和熔点差异实现的;在获取乙酰苯胺粗品后,再采用合适的方法对其进行重结晶提纯即可得到纯度较高的乙酰苯胺。
(1)仪器a的名称即直形冷凝管;
(2)由于乙酸与水混溶,乙酰苯胺可溶于热水而苯胺只易溶于乙醇,并且,乙酰苯胺熔点114℃,而乙酸和苯胺的熔点分别仅为17℃和-6℃;所以分离乙酰苯胺粗品时,可将圆底烧瓶中的液体趁热倒入盛有热水的烧杯中,冷却后,乙酰苯胺固体析出,再将其过滤出来,即可得到乙酰苯胺粗品;
(3)甲装置中温度计控制在100℃至105℃,这与水和乙酸的沸点很接近,因此甲装置中分馏柱的作用主要是将体系内的水和乙酸有效地分离出去;
(4)A.增加乙酸的投料,可以使平衡正向移动获得更高的产率,A项正确;
B.由于甲装置中的分馏柱能够有效地将产物中的水从体系内分离出去,水被分离出去后,对于乙酰苯胺制备反应的正向进行更有利,因此甲装置可以获得更高的转化率,B项正确;
C.冷凝管水流的方向一般是下口进水,上口出水,C项正确;
D.甲装置中温度计示数若在118℃以上,那么反应物中的乙酸会大量的气化溢出,对于反应正向进行不利,无法获得更高的产率,D项错误;
答案选ABC;
(5)①乙酰苯胺可以溶解在热水中,所以重结晶提纯乙酰苯胺粗品,首先要把粗品在热水中溶解,然后加入活性炭吸附杂质以及其他有色物质,过滤的时候为了避免乙酰苯胺的析出,应当趁热过滤,过滤后的滤液再冷却结晶,将结晶再过滤后,对其进行洗涤和干燥即可;趁热过滤时为了维持温度,可以将玻璃漏斗置于铜制的热漏斗内,热漏斗内装热水以维持温度,再进行过滤即可;
②结晶时,缓慢降温,或者缓慢蒸发溶剂有利于获得较大的晶体,答案选AD;
③在对重结晶出的乙酰苯胺晶体进行洗涤时,要避免洗涤过程中产品溶解造成的损耗,考虑到乙酰苯胺的溶解性,应当用冷水对其进行洗涤。


科目:高中化学 来源: 题型:
【题目】二甲醚是一种绿色、可再生的新能源。如图是绿色电源“二甲醚燃料电池”的工作原理示意图(a、b均为多孔性Pt电极)。该电池工作时,下列说法正确的是( )

A. a电极为该电池正极
B. O2在b电极上得电子,被氧化
C. 电池工作时,a电极反应式:CH3OCH3-12e-+3H2O===2CO2↑+12H+
D. 电池工作时,燃料电池内部H+从b电极移向a电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A. 用惰性电极电解 Na2SO4溶液,当 2 mol 电子转移时,可加入 18 g 水恢复
B. 用惰性电极电解 CuSO4溶液,当加入 1 mol Cu(OH)2恢复电解前浓度时,电路中转移了 4 mol e-
C. 用惰性电极电解 1 mol CuSO4和 1 mol NaCl 的混合溶液,溶液的 pH 先减小后增大
D. 要想实现 Cu+H2SO4(稀) ═ CuSO4+H2↑的反应,需在电解池中进行,且 Cu 为阳极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知断裂1molH2(g)中的H—H键需吸收436kJ 能量,断裂1molO2中的共价键需吸收496kJ能量,且氢气在氧气中燃烧的能量变化如图所示。下列说法正确的是
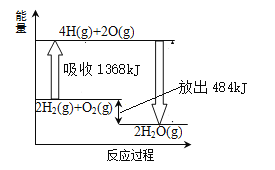
A.H2O(g)=H2(g)+1/2O2(l) △H=+242kJ/mol
B.H2(g)+1/2O2(g)= H2O(l) △H<-242kJ/mol
C.形成1molH2O(g)中的化学键需吸收926kJ
D.2H2(g)+ O2 (g)= 2H2O (g) △H=-1852kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用所学知识,解决下列问题:
(1)AgNO3的水溶液呈______(填“酸”、“中”、“碱”)性,原因是(用离子方程式表示):_____;实验室在配制AgNO3的溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,目的是______。
(2)今有常温下五种溶液:NH4Cl溶液 CH3COONa溶液 (NH4)2SO4溶液 NH4HSO4溶液 NaOH溶液
①NH4Cl溶液的pH_____7(填“>”、“<”或“=”),升高温度可以_______(填“促进”或“抑制”)NH4Cl的水解;
②pH相等的NaOH溶液与CH3COONa溶液,分别加热到相同的温度后CH3COONa溶液的pH_______NaOH溶液的pH(填“>”“=”或“<”);
③浓度相同的下列三种溶液:(A)NH4Cl溶液(B) (NH4)2SO4溶液(C)NH4HSO4 溶液,则c(NH4+)由大到小的顺序为____>___>____(用序号填空)。
(3)蒸干AlCl3溶液不能得到无水AlCl3,使SOCl2与AlCl3·6H2O混合并加热,可得到无水AlCl3,试解释原因________。 (提示:SOCl2与水反应的化学方程式为SOCl2 +H2O= SO2↑+ 2HCl↑)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,在水中溶解度较大,遇酸放出ClO2,是一种高效的氧化剂和优质漂白剂,可用于各种纤维和某些食品的漂白。过氧化氢法制备NaClO2固体的实验装置如图所示:
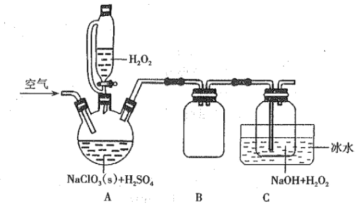
已知:
①ClO2的熔点为-59℃、沸点为11℃,极易溶于水,遇热水、见光易分解;气体浓度较大时易发生分解,若用空气、CO2、氮气等气体稀释时,爆炸性则降低。
②2ClO2+H2O2+2NaOH=2NaClO2+O2↑+2H2O
请回答:
(1)按上图组装好仪器后,首先应该进行的操作是____;装置B的作用是___;冰水浴冷却的主要目的不包括_(填字母)。
a.减少H2O2的分解 b.降低ClO2的溶解度 c.减少ClO2的分解
(2)ClO2是合成NaClO2的重要原料,写出三颈烧瓶中生成ClO2的化学方程式: ____。
(3)装置C中加入NaOH溶液的目的除了作反应物外,还因为_____。空气的流速过慢或过快都会影响NaClO2的产率,试分析原因:________。
(4)该套装置存在的明显缺陷是_________。
(5)为防止生成的NaClO2固体被继续还原为NaCl,所用还原剂的还原性应适中。除H2O2外,还可以选择的还原剂是_(填字母)
A.过氧化钠 B.硫化钠 C.氯化亚铁 D.高锰酸钾
(6)若mg NaClO3(s)最终制得纯净的n g NaClO2(s),则NaClO2的产率是_×100%。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质既能因发生化学反应使溴水褪色,又能使酸性KMnO4溶液褪色的是( )
①SO2 ②![]() ③
③![]() ④
④![]() ⑤CH≡C- CH3 ⑥聚乙烯
⑤CH≡C- CH3 ⑥聚乙烯
A.①②③④B.③④⑤C.①②⑤D.①②⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】TPE(四苯基乙烯)及其衍生物具有诱导发光特性,在光电材料等领域应用前景广泛。TPE的结构简式如下图,下列关于TPE的说法正确的是( )
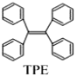
A.TPE的分子式为C26H22
B.TPE能发生加成反应,氧化反应,不能发生取代反应
C.TPE与化合物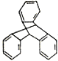 互为同分异构体
互为同分异构体
D.TPE的一氯代物有3种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com