
【题目】(1)研究氯气跟金属的反应时,选用金属铜进行实验。用坩埚钳夹住一束铜丝,灼热后立刻放入充满氯气的集气瓶里。铜丝燃烧后把少量水注入集气瓶里,用玻璃片盖住瓶口,振荡。
①根据哪些实验现象可判断铜丝燃烧后生成了+2价铜的化合物:_______________。
②反应的化学方程式为______________________________________________________。
(2)研究浓硫酸的强氧化性时,选用金属铜跟浓硫酸进行实验,实验装置如下图所示。
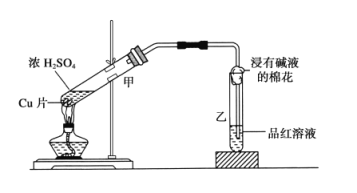
①乙中的现象_______,试管中的浸有碱液的棉花的作用是____________。
②甲中的反应方程式为_____________________________________。
(3)上述两个实验为什么都选金属铜作样本来进行实验________。
A.铜是一种不活泼金属
B.选用铜作实验可以推测更多金属跟氯气或浓硫酸反应的情况
C.铜是一种常见金属
D.铜跟氯气或浓硫酸反应可生成有色溶液,现象明显
【答案】燃烧时产生棕色烟,加水振荡后得到蓝绿色溶液 ② Cu+Cl2![]() CuCl2 品红溶液褪色 防止SO2逸出污染空气 Cu+2H2SO4(浓)
CuCl2 品红溶液褪色 防止SO2逸出污染空气 Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O ABCD
CuSO4+SO2↑+2H2O ABCD
【解析】
(1)①根据铜与氯气的反应现象及生成固体溶于水后溶液变成蓝色分析;
②铜与氯气在点燃条件下反应生成氯化铜;
(2)①二氧化硫具有漂白性,能使品红溶液褪色;二氧化硫为污染气体,需要用氢氧化钠溶液吸收多余的二氧化硫;
②甲中铜与浓硫酸在加热条件下反应生成硫酸铜、二氧化硫气体和水;
(3)根据铜为常见金属且性质不活泼,与氯气、浓硫酸反应后生成物溶于水形成有色溶液等方面考虑。
(1)①铜在氯气中燃烧的现象为:铜丝剧烈燃烧,产生大量棕黄色的烟,加水后形成了蓝绿色溶液,证明反应生成了+2价的铜,
故答案为:燃烧时产生棕色烟,加水振荡后得到蓝绿色溶液。
②铜与氯气反应生成氯化铜,反应的化学方程式为:Cu+Cl2![]() CuCl2,
CuCl2,
故答案为:Cu+Cl2![]() CuCl2。
CuCl2。
(2)①二氧化硫具有漂白性,能使品红溶液褪色;二氧化硫有毒,多余的气体不能直接排放,需要用氢氧化钠溶液吸收SO2气体,防止空气污染,反应的化学方程式为:SO2+2NaOH=Na2SO3+H2O,
故答案为:品红溶液褪色;防止SO2逸出污染空气。
②甲中铜与浓硫酸在加热条件下反应生成二氧化硫,反应的化学方程式为:Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O,
CuSO4+SO2↑+2H2O,
故答案为:Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O。
CuSO4+SO2↑+2H2O。
(3)由于铜是一种不活泼金属,选用铜作实验可以推测更多金属跟氯气或浓硫酸反应的情况,铜又是一种常见金属及铜跟氯气或浓硫酸反应可生成有色溶液,现象明显,所以选金属铜作样本来进行实验,故A、B、C、D正确。
故答案为:ABCD。


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:
【题目】甲、乙两份等质量的碳酸氢钠晶体,将甲用坩埚充分加热后冷却后,将固体完全转移到一试管中, 再加入足量的盐酸;乙不经加热置于另一试管中,也加入足量的盐酸。反应完全后,两试管中实际参 加反应的HC1质量之比为( )
A. 2:3 B. 2:1 C. 1:2 D. 1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图用分类法表示了一些物质或概念之间的从属或包含关系,不正确的是( )
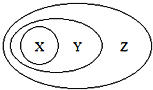
X | Y | Z | |
A | NaAlO2 | 盐 | 纯净物 |
B | 胶体 | 分散系 | 混合物 |
C | Al2O3 | 两性氧化物 | 氧化物 |
D | 单质参与反应 | 置换反应 | 氧化还原反应 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁、钴(Co)是同族元素,都是较活泼的金属,它们的化合物在工业上有重要的应用。
(1)草酸钴(CoC2O4)是一种难溶于水的浅粉红色粉末,通常用CoSO4溶液和(NH4)2C2O4溶液反应制得,写出该反应的离子方程式:______________
(2)现将含0.5mol FeCl3的溶液和含1.5mol KSCN的溶液混合,混合后溶液体积为1L,已知溶液存在平衡:Fe3++ 3SCN-=Fe(SCN)3(忽略其它过程)。平衡浓度 c[Fe(SCN)3]与温度T的关系如图1所示:则该反应△H____0(填“>”或“<”),温度为T1时,反应在5秒钟时达到平衡,则达到平衡时的平均反应速率v(SCN-)=____,该温度下的Fe3+的平衡转化率为____。
(3)工业上用电解浓NaOH溶液制备Na2FeO4,其工作原理如图2所示,则Cu电极连接电源的 ___极,阳极的电极反应式为________________

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、R为五种短周期元素,其原子半径和最外层电子数之间的关系如下图所示。

下列说法不正确的是
A. 简单阳离子半径:X< R
B. 最高价含氧酸的酸性:Z < Y
C. M的氢化物常温常压下为气体
D. X与Y可以形成正四面体结构的分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A是一种常见金属,F是一种红褐色沉淀。试根据图中转化关系,回答下列问题。

(1)写出A、C、F、G的化学式:A________;C________;F________;G________。
(2)保存C溶液时要加固体A的原因是______________________。
(3)写出下列转化的离子方程式。
①D→C:___________________________________________________;
②C→D:___________________________________________________;
③B→C+D__________________________________________________。
(4)写出E→F的化学方程式:__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气及含氮化合物在化工生产和国防工业中具有广泛应用。请回答:
(1)已知:(i)氢气的燃烧热为286.0 kJ·mol-1
(ii)4NH3(g)+3O2(g)![]() 2N2(g)+6H2O (l) ΔH=- 1530.6 kJ·mol-1。
2N2(g)+6H2O (l) ΔH=- 1530.6 kJ·mol-1。
合成氨反应的热化学方程式为_____________________________。
(2)恒温恒容条件下,起始按物质的量之比为1∶1向密闭容器中充入N2(g)和H2(g),发生合成氨的反应。达平衡后,N2(g)的体积分数为_______________;然后只降低温度,N2(g)的体积分数会_________(填选项字母)。
A.增大 B.减小 C.不变 D.不能判断
(3)T℃时,CO2(g)和NH3(g)合成尿素的原理为2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(1)。在2 L恒容密闭容器中,通入1.2 mol NH3(g)和0.6 mol CO2(g),2 min时反应恰好达到平衡,测得c(NH3)=0.2 mol·L-1。
CO(NH2)2(s)+H2O(1)。在2 L恒容密闭容器中,通入1.2 mol NH3(g)和0.6 mol CO2(g),2 min时反应恰好达到平衡,测得c(NH3)=0.2 mol·L-1。
①0~2min内,用NH3表示的反应速率υ(NH3)=___________;反应的平衡常数K=____________。
②若其他条件不变,2 min时将容器体积迅速压缩到1L,在3 min时重新达到平衡,请在图1中画出2~3 min内c(NH3)随时间(t)变化的曲线关系图。

(4)碱性氨气燃料电池的装置如图2 所示,写出负极的电极反应式____________________。当电路中每通过3.6 mol e-,则需要标况下空气的体积________________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验结果与图像不相符的是

A. 向含有盐酸、氯化镁和氯化铝的溶液中逐渐加入氢氧化钠溶液直至过量
B. 向澄清石灰水中通入二氧化碳气体直至过量
C. 向氯化铝的溶液中逐渐加入氢氧化钠溶液直至过量
D. 向氯化铝的溶液中逐渐加入氨水直至过量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)现有下列7种有机物:
①CH4 ②![]() ③
③ ④
④ ⑤
⑤ ⑥
⑥![]() ⑦
⑦
请回答:其中属于醇类的是________(填序号,下同),互为同系物的是_______,能与金属钠反应的有_________,互为同分异构体的是________。
(2)肉桂酸甲酯由C、H、O三种元素组成,已知其相对分子质量为162,核磁共振氢谱显示有6个峰,其面积之比为1︰2︰2︰1︰1︰3 ,利用红外光谱仪检测其中的某些基团,测得红外光谱如下图,则肉桂酸甲酯的结构简式是 ____________________(不考虑立体异构)。

(3)写出2-甲基-2-丁烯的结构简式:____________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com