
【题目】下列实验结果与图像不相符的是

A. 向含有盐酸、氯化镁和氯化铝的溶液中逐渐加入氢氧化钠溶液直至过量
B. 向澄清石灰水中通入二氧化碳气体直至过量
C. 向氯化铝的溶液中逐渐加入氢氧化钠溶液直至过量
D. 向氯化铝的溶液中逐渐加入氨水直至过量
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】某溶液中只含有Na+、Al3+、Cl﹣、SO42﹣ 四种离子,已知前三种离子的个数比为3:2:1,则溶液中Al3+和 SO42﹣的离子个数比为( )
A.1:2
B.1:4
C.3:4
D.3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)PVAc是一种具有热塑性的树脂,可合成重要高分子材料M,合成路线如下:
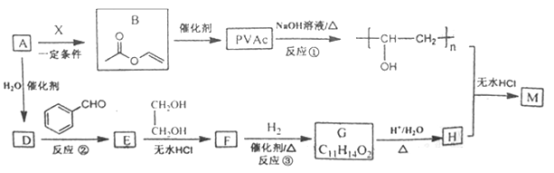
己知:R、R1、R2为H原子或烃基
Ⅰ. 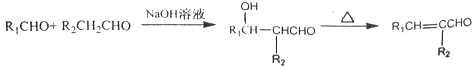
Ⅱ. 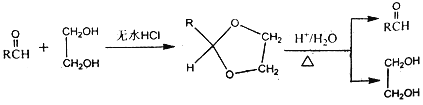
Ⅲ.羟基连在碳碳双键或碳碳三键上不稳定。
(1)已知标准状况下,4.48L气态烃A的质量是5.2g,A→B为加成反应,则X的结构简式为__________________;B中官能团的名称是_______________________。
(2)E能使溴的四氯化碳溶液褪色,反应②的反应试剂和条件是________________,在E→F→G→H的转化过程中,乙二醇的作用是___________________________________。
(3)反应①的化学方程式为_________________________________________。
(4)己知M的链节中除苯环外,还含有六元环状结构,则M的结构简式为_________________。
(5)E的同分异构体中含有苯环和甲基,且甲基不与苯环直接相连的同分异构体有_____种。
(6)以甲醛、苯乙醛(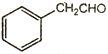 )以及上述合成路线中的必要有机试剂为原料合成
)以及上述合成路线中的必要有机试剂为原料合成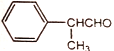 (其他无机试剂任选),请写出合成路线。______________________
(其他无机试剂任选),请写出合成路线。______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求进行填空:
(1)6.20 g Na2O 晶体中含 Na+的物质的量是 _________________。
(2)等质量的 NH3 和 H2S 中,氢原子的个数比是______________________。
(3) 铁与水蒸气反应的化学方程式_______________________________________。
(4) 向少量氯化铝溶液中加入足量氢氧化钠的离子方程式________________________。
(5)人通过呼吸作用吸入氧气,氧化体内的葡萄糖(C6H12O6)提供能量以维持生命活动,反应式为:C6H12O6+6O26CO2+6H2O+能量,该反应中的还原剂是______,若在该反应中消耗氧化剂的体积在标准状况下为4.48L,则反应中转移电子的物质的量为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应:2NO2![]() 2NO+O2在体积固定的密闭容器中进行,达到平衡状态的标志是
2NO+O2在体积固定的密闭容器中进行,达到平衡状态的标志是
①单位时间内生成nmolO2的同时消耗2nmolNO2
②单位时间内生成nmolO2的同时消耗2nmolNO
③用NO2、NO、O2表示的反应速率之比为2∶2∶1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的压强不再改变的状态
⑦混合气体的平均相对分子质量不再改变的状态
A. ②④⑥⑦ B. ②③⑤⑦ C. ①③④⑤ D. 全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关金属及其化合物的说法正确的是( )
A.钠保存在煤油里的原因之一是它极易与氧气反应
B.焰色反应是化学变化,可以用玻璃棒做焰色反应实验
C.CaO、Na2O、Na2O2均为碱性氧化物
D.可用澄清石灰水来鉴别NaHCO3和Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳是自然界中形成化合物种类最多的元素,CO和CO2是碳的最常见氧化物。
(1)研究和解决二氧化碳捕集和转化问题是当前科学研究的前沿领域。在太阳能的作用下,缺铁氧化物[Fe0.9O]能分解CO2,其过程如图1所示。过程①的化学方程式是______。在过程②中每产生0.1molO2,转移电子______mol。

(2)在催化剂作用下,将二氧化碳和氢气混合反应生成甲烷,是目前科学家们正在探索的处理空气中的二氧化碳的方法之一。
①已知:
共价键 | C=O | H—H | C—H | O—H |
键能/(kJmol-1) | 745 | 436 | 413 | 463 |
则CO2(g)+4H2(g)![]() CH4(g)+2H2O(g) △H=______kJmol-1。
CH4(g)+2H2O(g) △H=______kJmol-1。
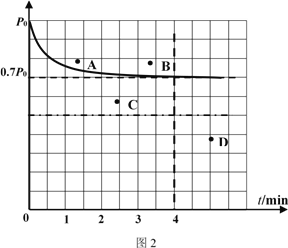
②向1L固定容积的密闭容器中加入4.0 mol H2(g)、1.0mol CO2,控制条件(催化剂:铑—镁合金、高温T1)使之反应,若测得容器内气体的压强随着时间的变化如图2所示。则4 min时容器内气体的密度为______;温度T1 下,该反应的化学平衡常为______。若采用2 L固定容积的密闭容器,投料量、催化剂和反应温度均保持不变,则反应重新达到平衡时对应体系内的压强的点是______(填字母)。
(3)工业合成原料气CO会与设备、管道及催化剂表面的金属铁、镍反应,生成羰基化合物。四羰基镍是热分解法制备高纯镍的原料,也是有机合成中供给一氧化碳的原料,还可做催化剂。Ni(s)+4CO(g)![]() Ni(CO)4(g) △H<0 Ni(CO)4(g)
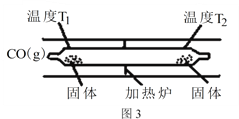
Ni(CO)4(g) △H<0 Ni(CO)4(g)![]() Ni(s)+4CO(g)。如图3所示,在石英真空管的温度为T1一端,放入少量粗镍和CO(g),一段时间后,在温度为T2的一端可得到纯净的镍。则温度T1______T2(填“>”“<”或“=”),上述反应体系中循环使用的物质为______(填化学式)。
Ni(s)+4CO(g)。如图3所示,在石英真空管的温度为T1一端,放入少量粗镍和CO(g),一段时间后,在温度为T2的一端可得到纯净的镍。则温度T1______T2(填“>”“<”或“=”),上述反应体系中循环使用的物质为______(填化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com