
金属镁及其化合物不仅在国防上有重要应用,在化学研究中也有广泛应用。
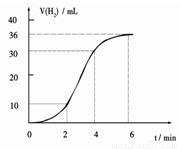
(1)某同学研究反应速率时用如下方法:取一段镁条,用砂纸擦去表面的氧化膜,使足量镁条与一定量盐酸反应生成H2的量与反应时间的关系曲线如图所示。镁与盐酸反应的离子方程式为 ;在前4min内,镁条与盐酸的反应速率逐渐加快,在4 min之后,反应速率逐渐减慢,请简述其原因:_____________。
(2)向少量的Mg(OH)2悬浊液中加入适量的饱和氯化铵溶液,固体完全溶解,写出NH4Cl饱和溶液使Mg(OH)2悬浊液溶解的离子方程式 。
(3)Mg Al可形成原电池:
编号 | 电极材料 | 电解质溶液 | 电子流动方向 |
1 | Mg Al | 稀盐酸 | Mg流向Al |
2 | Mg Al | NaOH溶液 |
|
根据上表中的实验现象完成下列问题:
①实验1中Mg为 极;
②实验2中电子流动方向 ,Al为 极,为什么? 。
(1)Mg+2H+=Mg2++H2↑(1分)
镁和盐酸反应是放热反应,随着反应体系温度升高,反应速率增大(1分);
4min后由于溶液中H+浓度降低,所以导致反应速率减小(1分)。
(2)Mg(OH)2(s)+2NH4+= Mg2++2NH3·H2O(2分)
(3) ① 负极(1分)②Al流向Mg(1分),负(1分),Al能和NaOH溶液反应而Mg不能,故Al作负极,Mg作正极。(2分)
【解析】
试题分析:(1)盐酸是强电解质,应写成离子的形式:Mg+2H+=Mg2++H2↑(1分)
镁和盐酸反应是放热反应,随着反应的不断进行,放出的热量使得反应体系温度升高,导致反应速率增大;但是随着时间的推移,4min后由于溶液中H+浓度降低,尽管热量还在放出,但是此时温度对化学反应速率的影响程度已远小于浓度的变化对化学反应速率的影响,所以导致反应速率减小(1分)。
(2)Mg(OH)2(s)+2NH4+= Mg2++2NH3·H2O(2分)
(3)该题中一定要注意反应条件的转变:在酸性条件下镁比铝的金属性强,但是在碱性条件下,铝显得比镁要活泼。
考点:考查影响化学反应速率的因素,不同物质在不同介质中的活泼性的差别。


 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源:2016届云南省高一下学期第一次月考化学试卷(解析版) 题型:选择题
氯气是一种重要的工业原料。工业上利用反应在3Cl2+2NH3=N2+6HCl检查氯气管道是否漏气。下列说法错误的是( )
A.若管道漏气遇氨就会产生白烟
B.该反应利用了Cl2的强氧化性
C.该反应属于复分解反应
D.生成1molN2有6mol电子转移
查看答案和解析>>
科目:高中化学 来源:2015届福建省四地六校高二下学期第一次月考化学试卷(解析版) 题型:选择题
具有下列最外层电子排布的基态原子,其相应的元素一定属于主族的是( )
A.ns1 B.ns2 C.ns2np6 D.ns2np2
查看答案和解析>>
科目:高中化学 来源:2015届湖南省益阳市高二下学期第一次月考化学试卷(解析版) 题型:选择题
下列化合物的核磁共振氢谱中出现三组峰,其氢原子数之比为6:1:2的是( )
A.2,2,3,3-四甲基丁烷 B.2,4-二甲基戊烷
C.3,4-二甲基己烷 D.2,5-二甲基己烷
查看答案和解析>>
科目:高中化学 来源:2015届湖南省益阳市高二下学期第一次月考化学试卷(解析版) 题型:选择题
下列物质是同分异构体的是
①对二甲苯和乙苯;②乙醇和乙二醇;③1?氯丙烷和2?氯丙烷;④丙烯和环丙烷;⑤乙烯和聚乙烯
A.①②③④⑤ B.①③④ C.②③④ D.①②④
查看答案和解析>>
科目:高中化学 来源:2015届湖北省黄石市高二上学期期末考试化学试卷(解析版) 题型:选择题
下列说法错误的是
A.常温下,将pH=3的醋酸溶液稀释到原体积的10倍后,溶液的pH小于4
B.为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH。若pH>7,则H2A是弱酸;若pH<7,则H2A是强酸
C.用0.200 mol·L-1 NaOH标准溶液滴定HCl与CH3COOH的混合液(混合液中两种酸的浓度均约为0.1 mol·L-1),至中性时,溶液中的酸未被完全中和
D.相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水、②0.1 mol·L-1盐酸、③0.1 mol·L-1氯化镁溶液、④0.1 mol·L-1硝酸银溶液中,Ag+浓度: ④>①>②>③
查看答案和解析>>
科目:高中化学 来源:2015届湖北省黄石市高二上学期期末考试化学试卷(解析版) 题型:选择题
下列各离子方程式中,属于水解反应且使溶液显碱性的是
A.CH3COOH+OH-= CH3COO-+H2O
B.H2O+H2O H3O++OH-
H3O++OH-
C.NH4+ + H2O NH3·H2O + H+
NH3·H2O + H+
D.PO43-+H2O HPO42-+OH-
HPO42-+OH-
查看答案和解析>>
科目:高中化学 来源:2015届湖北省荆门市高二上学期期末考试化学试卷(解析版) 题型:选择题
高氯酸、硫酸、硝酸和盐酸都是强酸,其酸性在水溶液中差别不大。以下是某温度下这四种酸在冰醋酸中的电离常数:从下表格中判断下列说法正确的是
酸 | HClO4 | H2SO4 | HCl | HNO3 |
Ka | 1.6×10-5 | 6.3×10-9 | 1.6×10-9 | 4.2×10-10 |
A.在冰醋酸和水中这四种酸都没有完全电离
B.在冰醋酸中高氯酸是这四种酸中最弱的酸
C.在冰醋酸中硫酸的电离方程式为H2SO4=2H++SO42-
D.水对于这四种酸的强弱没有区分能力,但醋酸可以区别这四种酸的强弱
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com