
【题目】下列说法正确的是
①pH=2和pH=1的HNO3中c(H+)之比为1∶10
②0.2 mol/L与0.1 mol/L醋酸中,c(H+)之比大于2∶1
③Na2CO3溶液中c(Na+)与c(CO![]() )之比为2∶1
)之比为2∶1
④纯水在100℃和20℃时,pH前者大
⑤同温时,pH=10的KOH溶液和pH=10的KCN溶液中由水电离的OH-浓度后者大
⑥100 mL 0.1 mol/L的醋酸溶液与10 mL 1.0 mol/L的醋酸溶液中H+的数目,前者多
A.①④⑤ B.①⑤⑥ C.①②⑤ D.①②③⑥
【答案】B
【解析】
试题分析:①pH=2与pH=1的硝酸中c(H+)分别为0.01moL/L和0.1mol/L,则之比为1:10,故①正确;
②醋酸是弱酸,不能完全电离,醋酸浓度越小,电离程度越大,0.2mol/L与0.1mol/L醋酸中,c(H+)之比小于2:1,故②错误;③因CO32-水解,则c(Na+)与c(CO32-)之比大于2:1,故③错误;④纯水在100℃和20℃时,pH后者大,故④错误;⑤氢氧化钾抑制水的电离,KCN水解使溶液显碱性促进水的电离,故⑤正确;⑥100mL 0.1molL-1的醋酸和10mL 1.0molL-1的醋酸中含醋酸的物质的量相等,醋酸浓度越小其电离程度越大,所以100mL 0.1mol/L的醋酸溶液与10mL 1.0mol/L的醋酸溶液中H+的数目,前者多,故⑥正确;故选B。


科目:高中化学 来源: 题型:
【题目】电化学气敏传感器可用于检测环境中NH3的含量,其工作原理示意图如下。
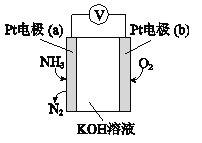
下列说法不正确的是
A. O2在电极b上发生还原反应
B. 溶液中OH+向电极a移动
C. 负极的电极反应式为:2NH3-6e-+6OH-=N2+6H2O
D. 反应消耗的NH3与O2的物质的量之比为4:5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在t ℃时,Ag2CrO4(橘红色)在水溶液中的沉淀溶解平衡曲线如图所示。又知AgCl的Ksp=1.8×10-10。下列说法不正确的是

A.t ℃时,Ag2CrO4的Ksp为1×10-8
B.饱和Ag2CrO4溶液中加入K2CrO4不能使溶液由Y点变为X点
C.t ℃时,Y点和Z点时Ag2CrO4的Ksp相等
D.t ℃时,将0.01 mol·L-1 AgNO3溶液滴入20 mL 0.01 mol·L-1 KCl和0.01 mol·L-1 K2CrO4的混合溶液中,Cl-先沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相同温度、相同浓度下的六种溶液,其pH由小到大的顺序如图所示,图中①②③代表的物质可能分别为 ( )
![]()
A.NH4Cl (NH4)2SO4 CH3COONa
B.(NH4)2SO4 NH4Cl CH3COONa
C.(NH4)2SO4 NH4Cl NaOH
D.CH3COOH NH4Cl (NH4)2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取一定质量的Cu2O和CuO混合粉末,将其均匀混合后分成两等份,取其中一份用足量的氢气还原,测得反应后固体质量减少6.40g,另一份中加入400mL稀硝酸,固体恰好完全溶解,且同时收集到标准状况下NO气体4.48L,则所用硝酸的物质的量浓度为( )
A. 4.0mol/L B. 3.2mol/L
C. 2.0mol/L D. 1.6mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,某碱性溶液中,由水电离出来的c(OH-)=10-4 mol/L,则该溶液中的溶质可能是
A. Al2(SO4)3 B. KHSO4 C. NaOH D. CH3COONa
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.某同学为了检验浓硫酸与木炭粉在加热条件下反应产生的所有气体产物,选用了如下图所示的实验装置。
|
|
|
|
A | B | C | D |
(1)为验证上述气体,将混合气体依次通过所用仪器,其顺序为:混合气体→_____→ A →_____→_____(每种仪器只能使用一次)
(2)A中品红溶液的作用是__________________________。
(3)确定有CO2生成的实验现象是____________________________________________。
(4)在不影响实验检验结果的情况下,理论上B中的高锰酸钾溶液还可以用下列哪些试剂代替_____________
①饱和NaHCO3溶液 ②浓硫酸 ③氯水 ④H2S溶液 ⑤Na2SO3溶液
Ⅱ.实验室二氧化硫尾气吸收与工业烟气脱硫的化学原理相通。石灰-石膏法和碱法是常用的烟气脱硫法。
石灰-石膏法的吸收反应为SO2+Ca(OH)2=CaSO3↓+H2O。吸收产物亚硫酸钙由管道输送至氧化塔氧化,反应为2CaSO3+O2+4H2O=2CaSO4·2H2O。其流程如下图:
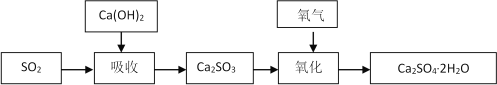
碱法的吸收反应为SO2+2NaOH=Na2SO3+H2O。碱法的特点是氢氧化钠碱性强、吸收快、效率高。其流程如下图:
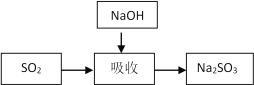
已知:
试剂 | Ca(OH)2 | NaOH |
价格(元/kg) | 0.36 | 2.9 |
吸收SO2的成本(元/mol) | 0.027 | 0.232 |
(1)石灰-石膏法和碱法吸收二氧化硫的化学原理相同之处是 ____________________ 。和碱法相比,石灰-石膏法的优点是 ________________ ,缺点是 ________________ 。
(2)某学习小组在石灰-石膏法和碱法的基础上,设计一个改进的、能实现物料循环的烟气脱硫方案,流程图中的甲、乙、丙各是__________________、___________________、___________________(填化学式)

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用如图所示装置制备氯气并进行一系列相关的实验(加热装置和夹持设备已省略).
![]()
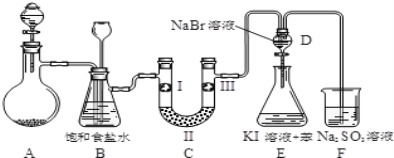
(1)A中盛装液体仪器的名称是:______.
(2)洗气装置B是为了除去Cl2中的HCl气体,应放入的试剂是______;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:____________.
(3)制备氯气选用的药品为:MnO2和浓盐酸,写出制备氯气的化学反应方程式___________________.
(4)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、Ⅱ、Ⅲ依次放入(填符号)______.
a | b | c | d | |
I | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
Ⅱ | 碱石灰 | 硅胶 | 无水氯化钙 | 浓硫酸 |
Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(5)设计装置D、E的目的是比较氯、溴、碘的非金属性.当向D中缓缓通入一定量氯气时,可以看到无色溶液逐渐变为黄色,说明非金属性氯___溴(填“>”或“<”).
(6)反应一段时间后,打开活塞,将装置D中少量溶液加入装置E中,振荡。观察到的现象是_________________,根据上述现象(“能”、“不能”)___说明非金属性溴强于碘。
(7)F处为尾气吸收装置,写出其离子反应方程式__________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某集团拟在太空建立巨大的激光装置,把太阳光变成激光用于分解海水制氢气,其反应式可表示为2H2O ![]() 2H2↑+O2↑。有下列几种说法:①水的分解反应是放热反应;②氢气是一级能源;③使用氢气作燃料有助于控制温室效应;④ 该过程将光能转化为化学能。以上叙述中正确的是
2H2↑+O2↑。有下列几种说法:①水的分解反应是放热反应;②氢气是一级能源;③使用氢气作燃料有助于控制温室效应;④ 该过程将光能转化为化学能。以上叙述中正确的是
A. ①② B. ②③ C. ③④ D. ①④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com