
【题目】为了纪念元素周期表诞生150周年,联合国将2019年定为“国际化学元素周期表年”。回答下列问题:
(1)Ag与Cu在同一族,则Ag在周期表中_____(填“s”、“p”、“d”或“ds”)区。[Ag(NH3)2]+中Ag+空的5s轨道和5p轨道以sp杂化成键,则该配离子的空间构型是_____。
(2)表中是Fe和Cu的部分电离能数据:请解释I2(Cu)大于I2(Fe)的主要原因:______。
元素 | Fe | Cu |
第一电离能I1/kJ·mol-1 | 759 | 746 |
第二电离能I2/kJ·mol-1 | 1561 | 1958 |
(3)亚铁氰化钾是食盐中常用的抗结剂,其化学式为K4[Fe(CN)6]。
①CN-的电子式是______;1mol该配离子中含σ键数目为______。
②该配合物中存在的作用力类型有______(填字母)。
A.金属键 B.离子键 C.共价键 D.配位键 E.氢键 F.范德华力
(4)MnO的熔点(1660℃)比MnS的熔点(1610℃)高,其主要原因是________。
(5)第三代太阳能电池利用有机金属卤化物碘化铅甲胺(CH3NH3PbI3)半导体作为吸光材料,CH3NH3PbI3具有钙钛矿(AMX3)的立方结构,其晶胞如图所示。
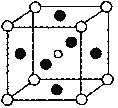
①AMX3晶胞中与金属阳离子(M)距离最近的卤素阴离子(X)形成正八面体结构,则M处于_______位置,X处于______位置(限选“体心”、“顶点”、“面心”或“棱心”进行填空)。
③CH3NH3PbI3晶体的晶胞参数为a nm,其晶体密度为dg·cm-3,则阿伏加德罗常数的值NA的计算表达式为_________。
【答案】ds 直线形 失去第二个电子时,Cu失去的是全充满3d10 电子,Fe 失去的是4s1电子 ![]() 12NA BCD 二者均为离子晶体,O2-半径小于S2-半径,MnO的晶格能大于MnS 体心 面心
12NA BCD 二者均为离子晶体,O2-半径小于S2-半径,MnO的晶格能大于MnS 体心 面心 
【解析】
(1)Ag在第五周期第ⅠB族,属于ds区;依题意:[Ag(NH3)2]+中Ag+以sp杂化成键,应该是直线形;
(2)Cu+的价电子排布式为3d10,Fe+的价电子排布式为3d64s1,Cu+再失去的是3d10上的电子,而Fe+失去的是4s1的电子,由于原子核外电子处于全充满、半充满或全空时是稳定的状态,显然3d10处于全充满,更稳定。所以失去第二个电子时,Cu 失去的是全充满 3d10 电子,需要的能量高,而Fe 失去的是 4s1 电子,所需能量低;故I2(Cu)大于I2(Fe)。
(3)①CN-与N2是等电子体,结构相似,根据氮气电子式书写氢氰根离子电子式为![]() ;CN-与Fe2+以配位键结合,这6个配位键都属于σ键,还有6个CN-中各有一个σ键,1个配离子中含有的σ键共有12个,则1mol该配离子中含有 12 NA个σ键;
;CN-与Fe2+以配位键结合,这6个配位键都属于σ键,还有6个CN-中各有一个σ键,1个配离子中含有的σ键共有12个,则1mol该配离子中含有 12 NA个σ键;
②K4 [Fe(CN)6]是离子化合物,含有离子键,阳离子K+与配离子之间以离子键结合,Fe2+与CN-以配位键结合,CN-中的两种原子以极性共价键结合, 故选BCD;
(4)MnO和MnS的阳离子相同,阴离子所带电荷也相同,但是O2-的半径比S2-小,离子键作用力强,所以MnO中的晶格能比MnS中的大,物质的熔点也比MnS的高;
(5)①依题意可知:卤素阴离子位于立方体的6个面的面心,正好构成正八面体,M位于八面体的体心,也是立方体的体心;
②晶体体积=晶体体积=a3×10-21cm3,晶体密度ρ=![]() ,则NA =
,则NA = ![]() 。1mol晶胞含1molCH3NH3PbI3,据d=
。1mol晶胞含1molCH3NH3PbI3,据d=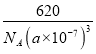 ,所以NA=
,所以NA=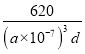 。
。


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
【题目】下列有关说法不正确的是( )
A. 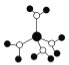 水合铜离子的模型如图所示,1个水合铜离子中有4个配位键
水合铜离子的模型如图所示,1个水合铜离子中有4个配位键
B. 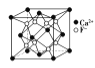 CaF2晶体的晶胞如图所示,每个CaF2晶胞平均占有4个Ca2+
CaF2晶体的晶胞如图所示,每个CaF2晶胞平均占有4个Ca2+
C.  H原子的电子云图如图所示,H原子核外的大多数电子在原子核附近运动
H原子的电子云图如图所示,H原子核外的大多数电子在原子核附近运动
D.  金属Cu中Cu原子堆积模型如图所示,该金属晶体为最密堆积,每个Cu原子的配位数均为12
金属Cu中Cu原子堆积模型如图所示,该金属晶体为最密堆积,每个Cu原子的配位数均为12
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将NaAlO2、Ba(OH)2、NaOH配成100.0 mL混合溶液,向该溶液中通入足量CO2,生成沉淀的物质的量n(沉淀),与通入CO2的物质的量n(CO2)的关系,如图所示,下列说法中正确的是

A. P点的值为0.6
B. 混合溶液中c(NaOH)+c(NaAlO2)=4.0 mol/L
C. bc段的化学反应方程式为:NaOH+CO2=NaHCO3
D. cd段表示Al(OH)3沉淀溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是

选项 | a中的物质 | b中的物质 | c中收集的气体 | d中的物质 |
A | 浓氨水 | CaO | NH3 | H2O |
B | 浓硫酸 | Na2SO3 | SO2 | NaOH溶液 |
C | 稀硝酸 | Cu | NO2 | H2O |
D | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的恒容密闭容器中发生反应:2SO2(g)+O2(g)![]() 2SO3(g),下列证据能说明反应一定达到化学平衡状态的是
2SO3(g),下列证据能说明反应一定达到化学平衡状态的是
A.容器内的压强不再改变B.c(SO2):c(O2):c(SO3)=2:1:2
C.混合气体的密度不再改变D.SO2的生成速率与SO3的消耗速率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25℃时醋酸的电离常数为1.6×10-5,该温度下向20 mL 0.01 mol·L-1醋酸溶液中不断滴入0.01 mol·L1 NaOH(aq),溶液pH变化如图所示。此过程溶液中离子浓度的关系错误的是
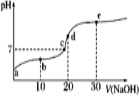
A. a点溶液的c(H+)=4×10-4mol·L-1
B. 水电离程度:e>d>c>b>a
C. b点:2c(Na+)=c(CH3COO-)+c(CH3COOH)
D. d点:c(OH-)=c(CH3COOH)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学—选修3:物质结构与性质]
前四周期原子序数依次增大的元素A,B,C,D中,A和B的价电子层中未成对电子均只有1个,平且A-和B+的电子相差为8;与B位于同一周期的C和D,它们价电子层中的未成对电子数分别为4和2,且原子序数相差为2。
回答下列问题:
(1)D2+的价层电子排布图为_______。
(2)四种元素中第一电离最小的是________,电负性最大的是________。(填元素符号)
(3)A、B和D三种元素责成的一个化合物的晶胞如图所示。
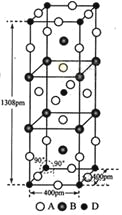
①该化合物的化学式为_________________;D的配位数为___________;
②列式计算该晶体的密度_______g·cm-3。
(4)A-、B+和C3+三种离子组成的化合物B3CA6,其中化学键的类型有_____________;该化合物中存在一个复杂离子,该离子的化学式为_______________,配位体是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环己烯常用于有机合成。现通过下列流程,以环己烯为原料合成环醚、聚酯、橡胶,其中 F 可以作内燃机的抗冻剂,J 分子中无饱和碳原子。已知:R1—CH==CH—R2→R1—CHO+R2—CHO
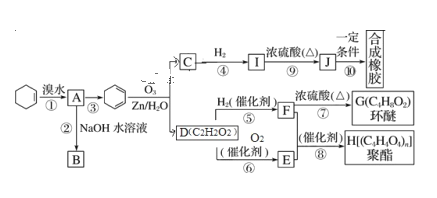
(1)A的结构简式为_____③的反应试剂及条件是______
(2)有机物B和 I的关系为_____(填字母)。
A.同系物 B.同分异构体 C.都属于醇类 D.都属于烃
(3)H的名称_________
(4)写出下列反应的化学方程式并注明反应类型:
反应⑨_________;________
(5)写出两种C的属于酯类的链状同分异构体的结构简式:_________;________
(6)参照题给信息,试写出以 2-丁烯为原料制取乙酸乙酯的合成路线流程图(无机原料任选)
_____________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为2 L的密闭容器中发生反应xA(g)+yB(g)![]() zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是( )
zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是( )
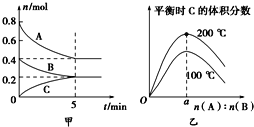
A. 200℃时,反应从开始到平衡的平均速率v(B)=0.04 mol·L-1·min-1
B. 200℃时,该反应的平衡常数为25
C. 当外界条件由200℃降温到100℃,原平衡一定被破坏,且正逆反应速率均增大
D. 由图乙可知,反应xA(g)+yB(g)![]() zC(g)的△H<0,且a=2
zC(g)的△H<0,且a=2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com