
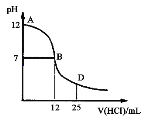
【题目】下图为常温下向25 mL 0.1 mol/L MOH溶液中逐滴滴加0.2 mol/L HCl溶液过程中溶液pH的变化曲线。下列推断正确的是
A.MOH在水中的电离方程式是:MOH=N++OH-
B.在B点表示酸碱恰好中和
C.A点→D点,溶液的导电能力逐渐增强(忽略体积变化)
D.在D点时,存在c(H+)>c(OH-)>c(Cl-)>c(M+)
【答案】C
【解析】
试题分析:常温下0.1molL-1 MOH溶液中pH=12,则c(OH-)=0.01mol/L,所以MOH在溶液中部分电离,即MOH为弱碱,A.MOH在溶液中部分电离,用可逆号表示,则电离方程式为:MOH![]() M++OH-,A错误;B.酸碱恰好反应生成强酸弱碱盐MCl,MCl在溶液中水解显酸性,B点表示的溶液的pH=7,溶液显中性,所以B点不是酸碱恰好中和的点,B错误;C.MOH为弱电解质,加盐酸产生MCl为强电解质,溶液中离子浓度增大,所以溶液的导电性增强,C正确;D.25mL0.1molL-1 MOH溶液中逐滴滴加0.2molL-1 HCl溶液,当HCl的体积为25mL时,溶液中溶质为等物质的量的MCl和HCl,溶液显酸性,则溶液中离子浓度关系为:c(Cl-)>c(H+)>c(M+)>c(OH-),D错误,答案选C。
M++OH-,A错误;B.酸碱恰好反应生成强酸弱碱盐MCl,MCl在溶液中水解显酸性,B点表示的溶液的pH=7,溶液显中性,所以B点不是酸碱恰好中和的点,B错误;C.MOH为弱电解质,加盐酸产生MCl为强电解质,溶液中离子浓度增大,所以溶液的导电性增强,C正确;D.25mL0.1molL-1 MOH溶液中逐滴滴加0.2molL-1 HCl溶液,当HCl的体积为25mL时,溶液中溶质为等物质的量的MCl和HCl,溶液显酸性,则溶液中离子浓度关系为:c(Cl-)>c(H+)>c(M+)>c(OH-),D错误,答案选C。


科目:高中化学 来源: 题型:
【题目】I.某温度下,Kw = 10-12。
(1)若保持温度不变,向少量水中加入_________g的NaOH固体,并加水至1 L,才能使溶液中水电离产生的H+、OH-的浓度乘积即:c(H+)·c(OH-) = 10-22
(2)若保持温度不变,某溶液中c(H+)为1×10-7 mol/L,则该溶液显________性(选填“酸”、“碱”或“中”)。
II.(3)实验室中常用NaOH进行洗气和提纯,当600 mL 1 mol/L NaOH溶液吸收标准状况下8.96 L CO2气体时所得溶液中各离子浓度由大到小的顺序是 。
(4)已知常温下Kw[Fe(OH)3] = 4.0×10-38,在FeCl3溶液中加入NaHCO3溶液,发生反应的离子方程式为_____________。若所得悬浊液的pH调整为4,则溶液中Fe3+的浓度为__________mol/L。
(5)试利用平衡移动原理解释下列事实:FeS不溶于水,但能溶于稀盐酸中_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA阿伏伽德罗常数的值。己知反应
(1)CH4(g)+2O2(g)═CO2(g)+2H2O(l) △H1="a" kJ/mol
(2)CH4(g)+2O2(g)═CO2(g)+2H2O(g) △H2="b" kJ/mol,其它数据如表:
化学键 | C═O | O═O | C-H | O-H |
键能kJ·mol-1 | 798 | x | 413 | 463 |
下列说法正确的是
A. 上表中 x=(1796+b)/2
B. H2O(g)═H2O(l) △S<0,△H═(a-b )kJ/mol
C. 当有4NA个C-H键断裂时,该反应放出热量一定为a kJ
D. 利用反应(1)设计的原电池电解精炼铜时,当负极输出0.2NA个电子时,电解槽的阳极质量一定减轻6.4g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组的甲、乙同学分别设计了以下实验来验证元素周期律。
(Ⅰ)甲同学在a、b、c三只烧杯里分别加入50 mL水,再分别滴加几滴酚酞溶液,依次加入大小相近的锂、钠、钾块,观察现象。
①甲同学设计实验的目的是____________________
②反应最剧烈的烧杯是_______(填字母);
③写出b烧杯里发生反应的离子方程式_________________
(Ⅱ)乙同学设计了下图装置来探究碳、硅元素的非金属性强弱,根据要求完成下列各小题
(1)实验装置:

填写所示仪器名称A___________B___________
(2)实验步骤: 连接仪器、________、加药品后,打开a、然后滴入浓硫酸,加热。
(3)问题探究:(已知酸性强弱:亚硫酸>碳酸)
①铜与浓硫酸反应的化学方程式是______________,装置E中足量酸性KMnO4溶液的作用是_______________。
②能说明碳元素的非金属性比硅元素非金属性强的实验现象是_________________;
③试管D中发生反应的离子方程式是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质的类别的说法不正确的是
A.能在水溶液中或熔融状态下导电的化合物就是电解质
B.胶体是一种能产生丁达尔效应的分散系
C.纯碱不属于碱,干冰属于酸性氧化物
D.Na2O和Na2O2都能与水反应生成对应的碱,它们都是碱性氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法中正确的是
A. 1 mol/L的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H2A)>c(A2-)
B. 有甲、乙两醋酸溶液,测得甲的pH=a,乙的pH=a+1,若用于中和等物质的量浓度等体积的NaOH溶液,需甲、乙两酸的体积V (乙)>10V(甲)
C. 常温下中和等体积、pH相同的CH3COOH和HCl溶液,消耗NaOH的量相同
D. 将pH=3的醋酸稀释为pH=4的过程中,![]() 比值不变
比值不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】-C3H7和-C3H7O取代苯环上的氢原子,形成的有机物中能与金属钠反应的同分异构体有
A. 10种 B. 15种 C. 30种 D. 36种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,可逆反应3X(g)+Y(g)![]() 2Z(g)达到平衡的标志是:
2Z(g)达到平衡的标志是:
A.单位时间内生成3nmolX,同时生成nmolY
B.2v逆(Y)=v正(Z)
C.X、Y、Z的浓度相等
D.X、Y、Z的分子个数比为3:1:2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com