
【题目】下列解释事实的方程式不正确的是( )
A. 金属钠露置在空气中,光亮表面颜色变暗:4Na+O2=2Na2O
B. 硫酸铵溶液与氢氧化钡溶液混合后加热,产生气体:NH4++OH-![]() NH3↑+H2O
NH3↑+H2O
C. 铝条插入烧碱溶液中,开始没有明显现象:Al2O3+2OH-=2AlO2-+H2O
D. 碘化银悬浊液滴加硫化钠溶液,黄色沉淀变成黑色:2AgI+S2-=Ag2S+2I-
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源: 题型:
【题目】化合物X是一种医药中间体,其结构简式如图所示.下列有关化合物X的说法正确的是( )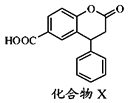
A.分子中两个苯环一定处于同一平面
B.不能与饱和Na2CO3溶液反应
C.在酸性条件下水解,水解产物只有一种
D.1mol化合物X最多能与7molH2反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用 A 质子数 B 中子数 C 核外电子数 D 最外层电子数 E 电子层数 填写下列空白:
(1)原子种类由_______决定;
(2)元素种类由_______决定;
(3)元素的化学性质主要由_______决定;
(4)元素的原子半径由_______决定;
(5)元素的化合价主要由_______决定。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某芳香烃X(相对分子质量为92)是一种重要的有机化工原料,研究部门以它为初始原料设计出如下转化关系图(部分产物、合成路线、反应条件略去).其中A是一氯代物,H是一种功能高分子,链节组成为C7H5NO. 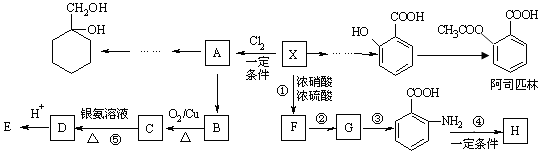
已知: ![]()
(1)F的结构简式是 , 反应①~⑤中属于取代反应的有 .
(2)反应②③两步能否互换(填“能”或“不能”),理由是 .
(3)B→C的化学方程式是 .
(4)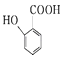 有多种同分异构体,请写出符合下列条件的同分异构体的结构简式(任写一种) ①能发生银镜反应
有多种同分异构体,请写出符合下列条件的同分异构体的结构简式(任写一种) ①能发生银镜反应
②含有苯环且分子中有四种不同化学环境的氢原子
③1mol该有机物最多能与2molNaOH反应.
(5)请用合成反应流程图表示出由 ![]() 和其他无机试剂合成
和其他无机试剂合成 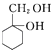 最合理的方案. 示例:H2C=CH2
最合理的方案. 示例:H2C=CH2 ![]() CH3CH2Br
CH3CH2Br ![]() CH3CH2OH.
CH3CH2OH.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于脂质的叙述中错误的是 ( )
A.脂肪是重要的储能物质,同质量的脂肪中含有比糖类更多的能量
B.脂质中的磷脂是构成细胞膜的主要成分之一
C.有的脂质可以由内分泌腺分泌,如性激素
D.胆固醇对生命活动具有一定的调节作用,所以它既是脂质也是激素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】淀粉酶能在极短时间内催化淀粉水解,但不能使麦芽糖发生水解,这体现了酶的( )
A. 高效性和多样性 B. 催化性和专一性
C. 高效性和专一性 D. 催化性和高效性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】每年3月22日是“世界水日”,联合国确定2016年“世界水日”的宣传主题是““水与就业”。下列关于水的叙述不正确的是 ( )
A.生化反应必须在水中进行
B.水是细胞鲜重中含量最多的化合物
C.水在细胞中的存在形式并非一成不变
D.自由水与结合水的比例与新陈代谢的强弱关系不大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素①—⑨在表中的位置,回答下列问题。
族 周期 | ⅠA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(1)第三周期中元素非金属性最强的元素的原子结构示意图是_____________。
(2)②③⑦最高价氧化物对应水化物酸性由强到弱的顺序是_________(填化学式)。
(3)用电子式表示⑨的氢化物的形成过程:_________________________。
(4)下列可以判断⑤和⑥金属性强弱的是________________(填序号)。
a. 单质的熔点⑤比⑥低 b. 化合价⑤比⑥低
c. 单质与水反应⑤比⑥剧烈 d. 最高价氧化物的水化物的碱性⑤比⑥强
(5)为验证ⅦA族部分元素非金属性的递变规律,设计下图装置进行实验,请回答:
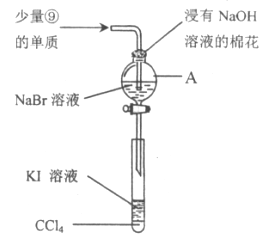
①仪器A的名称是_____________,A中发生的反应的离子方程式是_________。
②棉花中浸有的NaOH溶液的作用是(用离子方程式表示)_____________________。
③为验证溴与碘非金属性强弱:通入少量⑨的单质,充分反应后,将A中液体滴入试管内,取下试管,充分振荡、静置,可观察到____________________。该实验必须控制加入的⑨单质的量,否则得不出溴的非金属性比碘强。理由是_____________________。
④ⅦA族元素,非金属性随元素核电荷数增加而逐渐减弱的原因:同主族元素从上到下原子半径逐渐______________(填“增大”或“减小”),得电子能力逐渐减弱。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com