
【题目】已知相同条件下,下列反应的焓变和乎衡常数分别表示为: ①2H2O(g)=O2(g)+2H2(g)△H1 K1=x
②Cl2(g)+H2(g)=2HCl(g)△H2 K2=y
③2Cl2(g)+2H2O(g)=4HCl(g)+O2(g)△H3 K3=x
则下列关系正确的是( )
A.△H3=△H1+2△H2 x=xy2
B.H3=△H1+△H2 z=x+y
C.H3=△H1+2△H2 x=x﹣y2
D.H3=△H1+△H2 z= ![]()
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】根据原子结构及元素周期律的知识,下列推断正确的是( )
A.![]() Cl2与
Cl2与 ![]() Cl2氧化能力相近,二者互为同位素
Cl2氧化能力相近,二者互为同位素
B.![]() Se与
Se与 ![]() Se所含质子数相同,中子数不同
Se所含质子数相同,中子数不同
C.同主族元素形成的含氧酸的酸性随核电荷数的增加而减弱
D.同周期主族元素形成的简单离子半径随核电荷数的增大而减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于糖类、油脂和蛋白质是的说法中,正确的是( )
A. 葡萄糖和蔗糖都能发生水解反应
B. 油脂有油和脂肪之分,但都属于酯
C. 糖类、油脂、蛋白质都是由C、H、O、N四种元素组成
D. 淀粉与纤维素的分子式同为(C6H10O5)n,两者互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室进行NaCl溶液蒸发时,一般有以下操作过程,其正确的操作顺序是
①放置酒精灯 ②固定铁圈位置 ③放上蒸发皿 ④加热搅拌 ⑤停止加热,余热蒸干
A. ②③④⑤ B. ①②③④⑤ C. ②③①④⑤ D. ②①③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既不是氧化剂也不是还原剂等。下列反应与C+H2O(g)![]() CO+H2相比较,水的作用相同的是 ( )
CO+H2相比较,水的作用相同的是 ( )
A. 3NO2+H2O=2HNO3+NO B. Na2O+H2O=2NaOH
C. 2F2+2H2O=4HF+O2 D. 3Fe+4H2O(g)![]() Fe3O4+4H2
Fe3O4+4H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将7.2gCO和H2的混合气体与足量O2充分燃烧后,立即通入足量的Na2O2固体中,固体的质量增加 ( )
A. 2.1g B. 3.6g C. 7.2g D. 无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是重要的工业原料.煤化工可以利用煤炭制取水煤气从而合成甲醇:CO(g)+2H2(g)CH3OH(g).已知常温常压下反应的能量变化如图1所示: 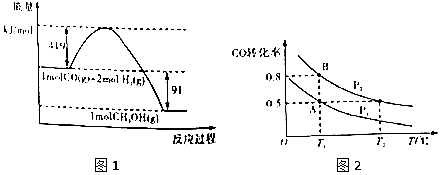 ②
②
化学键 | H﹣H | H﹣O | O=O |
键能kj/mol | 436 | x | 496 |
③CO(g)+ ![]() O2(g)=CO2(g)△H=﹣280kJ/mol
O2(g)=CO2(g)△H=﹣280kJ/mol
H2(g)+ ![]() O2(g)=H2O(I)△H=﹣284kJ/mol
O2(g)=H2O(I)△H=﹣284kJ/mol
H2O(I)=H2O(g)△H=+44kJ/mol
请回答下列问题:
(1)甲醇气体分解为CO和H2两种气体这一反应的活化能为kj/mol;
(2)请写出表示气态甲醇燃烧热的热化学方程式;
(3)H﹣O的键能x值为;
(4)如图2:在一容积可变的密闭容器中充入10molCO气体和30molH2气体,当达到平衡状态A时,容器的体积为20L.如反应开始时仍充入10molCO和30molH2 , 则在平衡状态B时容器的体积V(B)=L;
(5)在甲、乙、丙三个不同密闭容器中按不同方式投料,一定条件下发生该反应(起始温度和起始体积相同,反应物和生成物反应前后均为气态).相关数据如表所示:
容器 | 甲 | 乙 | 丙 |
相关条件 | 恒温恒容 | 绝热恒容 | 恒温恒压 |
反应物投料 | 1molCO、2molH2 | 1molCH3OH | 1molCH3OH |
平衡时容器体积 | V(甲) | V(乙) | V(丙) |
反应的平衡常数K | K(甲) | K(乙) | K(丙) |
平衡时CH3OH的浓度/molL﹣1 | C(甲) | C(乙) | C(丙) |
平衡时CH3OH的反应速率/molL﹣1min﹣1 | v(甲) | v(乙) | v(丙) |
则下列说法正确的是 .
A.V(甲)>V(丙)
B.K(乙)>K(丙)
C.c(乙)>c(甲)
D.v(甲)=v(丙)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质溶于水电离出的Cl-数目,与2mol NaCl溶于水电离出的Cl- 数目相同的是( )。
A. 1mol MgCl2 B. 2mol KClO3 C. 1mol AlCl3 D. 1.5mol CaCl2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com