
【题目】用水稀释0.1mol/L氨水时,溶液中随着水量的增加而减小的是( )
A.![]()
B.![]()
C.c(H+)和c(OH﹣)的乘积
D.OH﹣的物质的量
【答案】B
【解析】解:A、由NH3 . H2OOH﹣+NH4+可知,加水促进电离,则n(NH3 . H2O)减少,n(OH﹣)增大, ![]() 增大,故A错误; B、由NH3 . H2OOH﹣+NH4+可知,加水促进电离,则n(NH3 . H2O)减少,n(OH﹣)增大,
增大,故A错误; B、由NH3 . H2OOH﹣+NH4+可知,加水促进电离,则n(NH3 . H2O)减少,n(OH﹣)增大, ![]() 减小,故B正确;
减小,故B正确;
C、因加水稀释时,温度不变,则c(H+)和c(OH﹣)的乘积不变,故C错误;
D、由NH3 . H2OOH﹣+NH4+可知,加水促进电离,OH﹣的物质的量增大,故D错误;
故选:B.
用水稀释0.1mol/L氨水时,溶液中随着水量的增加,由NH3 . H2OOH﹣+NH4+可知,n(OH﹣)增大,但溶液的体积增大的多,则c(OH﹣)减小,加水促进电离,则n(NH3 . H2O)减少.


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案科目:高中化学 来源: 题型:
【题目】下列叙述中,错误的是( )
A. 虽然固体氯化钠不能导电,但氯化钠是电解质
B. 纯水的pH随温度的升高而减小
C. 在醋酸钠溶液中加入少量氢氧化钠,溶液中c(OH-)增大
D. 在纯水中加入少量硫酸铵,可抑制水的电离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空
(1)H3PO3与NaOH反应只生成NaH2PO3和Na2HPO3两种盐,则H3PO3为____元酸,Na2HPO3为_____(填“正盐”或“酸式盐”)。
(2)酸性条件下,次磷酸(H3PO2)可发生下列反应而用于化学镀银。
Ag++口H3PO2+口 =口Ag+口H3PO4+口
试回答下列问题
①该反应的氧化产物是_________。
②请将反应物和生成物补充完整并配平,并用单线桥法标出电子转移的数目_________。
③若反应中生成10.8gAg,则转移电子的数目约为________。
(3)在同温、同压下,实验测得CO2和O2两种气体的混合气体的密度是H2的20倍,则该混合气体的平均摩尔质量为______,其中O2的体积分数为______(保留3位有效数字)。
(4)常温常压下,将0.2mol钠、镁分别放入到100mL1mol/L的盐酸中,产生氢气的体积比为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一包NaHCO3和KHCO3的混合物样品.某研究性学习小组对其进行了如下探究,请按要求完成下列探究报告.
(1)【探究目的】实验测定样品中NaHCO3和KHCO3物质的量之比. 【探究思路】设计实验测量有关反应物和生成物的量,并通过计算确定样品中NaHCO3和KHCO3物质的量之比.
【实验探究】实验装置如图甲所示.将一定质量的混合物样品加入锥形瓶中,用针筒a注入一定体积的稀硫酸充分反应,再用针筒b收集生成气体的体积(忽略针筒管壁间的摩擦).
如果往锥形瓶中注入的稀硫酸的体积为V1mL,充分反应后,针筒b中气体的读数为V2mL,则反应中生成的CO2气体体积为mL.写出锥形瓶中反应的离子方程式 .
【结果处理】锥形瓶中放有混合均匀的NaHCO3和KHCO3的样品3.6g,向锥形瓶中滴入一定量的稀硫酸,生成的气体体积(已换算成标准状况)与加入的稀硫酸的体积关系如图乙所示: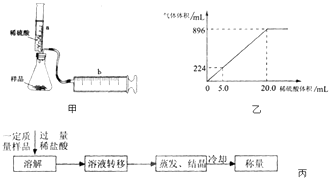
实验所用稀硫酸中溶质的物质的量浓度是mol/L.
(2)样品中NaHCO3和KHCO3物质的量之比为 . 【拓展探究】某同学设计了另一种方案,其操作流程如图丙:在转移溶液时,如果溶液转移不完全,则测得的混合物中NaHCO3和KHCO3物质的量之比(选填“偏大”、“偏小”或“不变”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4mol A气体和2mol B气体在体积为2L的密闭容器中混合,并在一定条件下发生反应:2A(g)+B(g)xC(g),若经2s后测得A的物质的量为2.8mol,C的物质的量浓度为0.6mol/L.现有几种说法:①2s内用物质A表示的平均反应速率为0.3mol/(Ls);②2s内用物质B表示的平均反应速率为0.6mol/(Ls);③2s时物质B的转化率为70%;④x=2.其中正确的是( )
A.①③
B.①④
C.②③
D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】8.34g FeSO47H2O样品在隔绝空气条件下受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示.下列说法中正确的是( ) 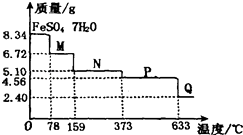
A.温度为78℃时固体物质M的化学式为FeSO4?5H2O
B.温度为l59℃时固体物质N的化学式为FeSO4?3H2O
C.在隔绝空气条件下由N得到P的化学方程式为FeSO4 ![]() ?FeO+SO3↑
?FeO+SO3↑
D.取适量380℃时所得的样品P,隔绝空气加热至650℃,得到一种固体物质Q,同时有两种无色气体生成,Q的化学式为Fe2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同一周期三种非金属元素X、Y、Z,其最高价氧化物的水化物的酸性由强到弱的顺序是:HXO4>H2YO4>H3ZO4。下列说法正确的是( )
A.元素的非金属性:X<Y<Z
B.气态氢化物的稳定性:HX>H2Y>ZH3
C.阴离子的还原性:X->Y2->Z3-
D.X、Y、Z依次位于ⅤA族、ⅥA族、ⅦA族。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向50mL NaOH溶液中逐渐通入一定量的CO2(假设溶液体积不变),随后取此溶液10mL,将其稀释至100mL,并向此稀释后的溶液中逐滴加入0.1molL﹣1的盐酸,产生CO2气体的体积(标准状况下)与所加入的盐酸的体积关系如图所示. 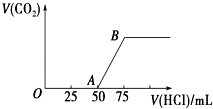
(1)写出OA段所发生反应的离子方程式: .
(2)NaOH在吸收CO2后,所得溶液的溶质为 , 其物质的量浓度之比为 .
(3)产生的CO2体积(标准状况下)为 .
(4)原NaOH溶液的物质的量浓度为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知相同条件下,下列反应的焓变和乎衡常数分别表示为: ①2H2O(g)=O2(g)+2H2(g)△H1 K1=x
②Cl2(g)+H2(g)=2HCl(g)△H2 K2=y
③2Cl2(g)+2H2O(g)=4HCl(g)+O2(g)△H3 K3=x
则下列关系正确的是( )
A.△H3=△H1+2△H2 x=xy2
B.H3=△H1+△H2 z=x+y
C.H3=△H1+2△H2 x=x﹣y2
D.H3=△H1+△H2 z= ![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com