
����Ŀ����Ҫ�����
��1��H3PO3��NaOH��Ӧֻ����NaH2PO3��Na2HPO3������,��H3PO3Ϊ____Ԫ�ᣬNa2HPO3Ϊ_____(����������������ʽ����)��
��2�����������£�������(H3PO2)�ɷ������з�Ӧ�����ڻ�ѧ������
Ag++��H3PO2+�� =��Ag+��H3PO4+��
�Իش���������
�ٸ÷�Ӧ������������_________��
���뽫��Ӧ��������ﲹ����������ƽ�����õ����ŷ��������ת�Ƶ���Ŀ_________��
������Ӧ������10.8gAg,��ת�Ƶ��ӵ���ĿԼΪ________��
��3����ͬ�¡�ͬѹ�£�ʵ����CO2��O2��������Ļ��������ܶ���H2��20������û�������ƽ��Ħ������Ϊ______������O2���������Ϊ______(����3λ��Ч����)��
��4�����³�ѹ�£���0.2mol�ơ�þ�ֱ���뵽100mL1mol/L�������У����������������Ϊ___��
���𰸡� �� ���� H3PO4 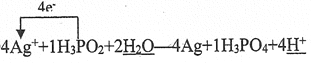 6.02��1022��0.1NA 40g/mol 33.3% 2:1
6.02��1022��0.1NA 40g/mol 33.3% 2:1
����������1��H3PO3��NaOH��Ӧֻ����NaH2PO3��Na2HPO3������,��˵��H3PO3ֻ�ܵ����2�������ӣ�Ϊ��Ԫ�ᣬ��Na2HPO3Ϊ���Σ��ʴ�Ϊ���� �����Σ���2�������ݷ�Ӧ��������Ԫ�ػ��ϼ����ߣ���������Ϊ��������ʴ�Ϊ��H3PO4 ����Ԫ�ػ��ϼ�����4�ۣ���Ԫ�ػ��ϼ۽���1�ۣ����������Ӻ͵ı���Ϊ4:1������ԭ���غ���ƽ����ʽ����Ӧ��ת��4�����ӣ��ʵ����ű�ʾΪ��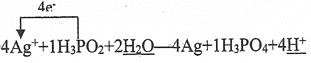 ��������10.8g������0.1mol����ת��0.1mol���ӣ���6.02��1022��0.1NA����3����ͬ�¡�ͬѹ�£��ܶȱȵ���Ħ������֮�ȷ�������������ƽ��Ħ������Ϊ40g/mol�������������������Ϊx������44��1-x��+32x=40����x=33.3% ����4��0.2mol����ȫ��Ӧ����0.1mol������0.2molþ��ʣ�࣬������ȫ��Ӧ������0.05mol���������߱���Ϊ0.1:0.05=2:1��
��������10.8g������0.1mol����ת��0.1mol���ӣ���6.02��1022��0.1NA����3����ͬ�¡�ͬѹ�£��ܶȱȵ���Ħ������֮�ȷ�������������ƽ��Ħ������Ϊ40g/mol�������������������Ϊx������44��1-x��+32x=40����x=33.3% ����4��0.2mol����ȫ��Ӧ����0.1mol������0.2molþ��ʣ�࣬������ȫ��Ӧ������0.05mol���������߱���Ϊ0.1:0.05=2:1��


 ͨ��ѧ��Ĭд����ϵ�д�
ͨ��ѧ��Ĭд����ϵ�д� ���ƽ̸�������ѡ����ĩ���100��ϵ�д�
���ƽ̸�������ѡ����ĩ���100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������������
A.���ӻ������в����ܴ��ڷǼ��Լ�
B.�����Ӽ��Ļ�����һ�������ӻ�������, �����ۼ��Ļ����ﲻһ�������ۻ�����
C.���ۻ�������һ���������Ӽ�
D.�ǽ����ͷǽ���֮������γɹ��ۼ���Ҳ�����γ����Ӽ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ̽����ϩ����ļӳɷ�Ӧ����ͬѧ��Ʋ���������ʵ�飺��ȡһ�����Ĺ�ҵ����ϩ����(�ڴ���ƿ��)��ʹ����ͨ����ˮ�У�������Һ��ɫ����֤����ϩ����ˮ�����˼ӳɷ�Ӧ����ͬѧ�����ڼ�ͬѧ��ʵ���У���ɫ�����Һ������������ɫ�������ʣ��Ʋ��ڹ�ҵ���Ƶõ���ϩ�л����ܺ���������ԭ���������ʣ��ɴ�����������ȳ�ȥ���ʣ�Ȼ����ϩ������ˮ��Ӧ��
����ش��������⡣
(1)��ͬѧ��ʵ��������ϩ�йصĻ�ѧ����ʽΪ��______________________��
(2)��ͬѧ��Ƶ�ʵ��________(��ܡ����ܡ�)��֤��ϩ���巢���ӳɷ�Ӧ����������________��(��д���)
��ʹ��ˮ��ɫ�ķ�Ӧδ���Ǽӳɷ�Ӧ
��ʹ��ˮ��ɫ�ķ�Ӧ���Ǽӳɷ�Ӧ
��ʹ��ˮ��ɫ������δ������ϩ
��ʹ��ˮ��ɫ�����ʾ�����ϩ
(3)��ͬѧ�Ʋ����ϩ�бض�����һ������������________��������ˮ��Ӧ�Ļ�ѧ����ʽ��_______________������֤�����б���ȫ����ȥ����ȥ�����ʵ��Լ�����________��
(4)Ϊ��֤��һ��Ӧ�Ǽӳɷ�Ӧ������ȡ����Ӧ����ͬѧ�������pH��ֽ�����Է�Ӧ����Һ�����ԣ�������_______________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������������������Һ�Ʊ������Եļ�ʽ������[Ala��SO4��b��OH��c]�������������������������Ĺ�����ͼ1�� 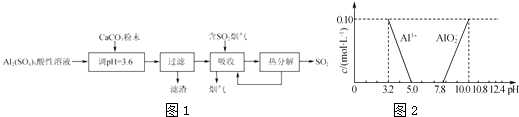
��1����CaCO3������Һ��pH��3.6����Ŀ�����к���Һ�е��ᣬ��ʹAl2��SO4��3ת��ΪAla��SO4��b��OH��c �� ����ʱ���õIJ��������������ձ�����������Ҫ�ɷ�Ϊ���ѧʽ����
��2�����������о���ȫ�ȷֽ�ų���SO2������С�����յ�SO2��������Ҫԭ������������SO2ǰ����Һ��ȣ��ȷֽ��ѭ�����õ���Һ��pH�����������С�����䡱����
��3��Ala��SO4��b��OH��c��a��b��c�Ĵ�����ϵʽΪ ��
��4����֪�ڳ�������Һ��Al3+��AlO2����Ũ������ҺpH�Ĺ�ϵ��ͼ2��ʾ��Ϊȷ����ʽ����������ɣ���������ʵ�飺 ��ȡ2.18g��ʽ��������Ʒ�ڿ��������������أ���Ʒ����������0.36g��
����ȡ2.18g��ʽ����������ˮ��������Һ��pH��5.0��7.8��
�۽��ڲ����ij������ˡ�ϴ�ӡ����������أ�����ʣ�����Ϊ1.02g��
�������Ʒ��Al3+��SO42�������ʵ���֮�ȣ�д��������̣���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2015��11����C919��ɻ���װ���ߣ���־���ҹ������ɻ������Ƚ��������У� �ٻ�����Ƥʹ�õ��ǵ�������﮺Ͻ���ϣ����в�������﮺Ͻ����ʵ���������ĸ����
a���ܶȴ� b��Ӳ�ȴ� c������ʴ
�ڷɻ���̥��������Ʒ�����в��Ͽ������ϳ�����������ĸ����
a��ʯӢɰ b��ʯ��ʯ c�������ϩ
�ۻ����Ƚ����ϲ��ϵ�ʹ���ʴ�12%���������ڸ��ϲ��ϵ���������ĸ����
a���ѺϽ� b�������� c����ͨ�մɣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ�ܰ������Ǹ��õ���ʶ���������� �ټ�������δϴ�����ɣ�����һ��ʱ�����ֺ��ɫ��ߣ�����Ҫ��ԭ��������������ʴ��
�ڳ˳���ֹЯ����Ʒ�IJ��ֱ�ʶ��ͼ��ʾ����Ũ���ᡢʳ�Ρ����͡�ʯ��������Ʒ�У�����Я���ϳ����� ��
�۹������ᣨ ![]() ���ֽ�Ϊ�������������ϡ�ܳ����ڲ;���е����������������ֽ�Ļ�ѧ����ʽ �� ijθҩ����Ҫ�ɷ���AlbMgc��OH��mCO3 �� ����������θ����࣬д��������θ�ᷴӦ�Ļ�ѧ����ʽ ��
���ֽ�Ϊ�������������ϡ�ܳ����ڲ;���е����������������ֽ�Ļ�ѧ����ʽ �� ijθҩ����Ҫ�ɷ���AlbMgc��OH��mCO3 �� ����������θ����࣬д��������θ�ᷴӦ�Ļ�ѧ����ʽ �� 
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵���в���ȷ����
����������ͬ������һ������ͬ��Ԫ�أ� ����������ͬ�����Ӳ�һ����ͬһ��Ԫ�أ� ��һ��Ԫ��ֻ����һ������������ij��Ԫ�ص����ԭ������ȡ������������������������������ͬ��������Ҳ��ͬ�����ӣ���������һ�ַ��Ӻ�һ�����ӣ���ͬλ�ص����ʼ�����ȫ��ͬ��
��A���٢ۢܢ� B���٢ڢܢ� C���ڢۢݢ� D�� �ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮϡ��0.1mol/L��ˮʱ����Һ������ˮ�������Ӷ���С���ǣ� ��
A.![]()
B.![]()
C.c��H+����c��OH�����ij˻�
D.OH�������ʵ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ԭ�ӽṹ��Ԫ�������ɵ�֪ʶ�������ƶ���ȷ���ǣ� ��
A.![]() Cl2��
Cl2�� ![]() Cl2�����������������Ϊͬλ��
Cl2�����������������Ϊͬλ��
B.![]() Se��
Se�� ![]() Se������������ͬ����������ͬ
Se������������ͬ����������ͬ
C.ͬ����Ԫ���γɵĺ������������˵���������Ӷ�����
D.ͬ��������Ԫ���γɵļ����Ӱ뾶��˵�������������С
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com