
����Ŀ�������Լ�ƿ��ǩ�ϵ�������ͼ��ʾ:

��1������������ʵ���Ũ����____________mol/L��
��2��ij��ѧ��ȤС������������ʵ�ʵ��̽��ʱ,��Ҫ240mL 4.6mol��L-1��ϡ����,������ϡ����ʱ��Ҫȡ____mL�ĸ�����;����ʱ��ѡ�õ�������Ҫ����Ͳ���ձ�����������_______����ͷ�ιܣ��ں�������д��ȱ���������ƣ���
��3�����ƹ�����,���в�����ʹ���Ƶ�ϡ������ҺŨ��ƫ�ߵ���____������ţ���
����ȡŨ�������Ͳ������ˮϴ��2~3��,����ϴ��Һת������ƿ
������ƿʹ��ʱδ����
���ܽ��δ����ȴ����Һ������
������ʱ��С������������ˮ�ε�ƿ��
�����ݺ���ҡ�ȡ�����,����Һ����ڿ̶��ߣ��ټ�����ˮ�����̶���
���𰸡�18��462��5250 mL����ƿ�٢�
��������
(1).����������ʵ���Ũ������c(H2SO4)=![]() =18.4mol/L���ʴ�Ϊ��18.4��
=18.4mol/L���ʴ�Ϊ��18.4��
(2).ʵ������240mL��������ƿ������Ӧѡ��250mL��������ƿ��������������ҪŨ��������Ϊa mL������ϡ�Ͷ�������a ��10��3L��18.4mol/L=0.25L��4.6mol/L�����a=62.5mL�����Ƹ�������Һʱ��Ҫ��������Ҫ����Ͳ���ձ�����������250mL����ƿ����ͷ�ιܵ����ʴ�Ϊ��62.5��250mL����ƿ��
(3). ��. ��ȡŨ�������Ͳ������ˮϴ��2~3��������ϴ��Һת������ƿ�У���ʹ����ƫ�࣬���Ƶ���ҺŨ��ƫ�ߣ�
��.����ʱҪ��ˮ����������ƿʹ��ʱδ��������Ƶ���ҺŨ����Ӱ�죻
��.Ũ����ϡ�ͷ��ȣ��ܽ��δ����ȴ����Һ�����ݣ���ʹ��Һ�����ƫС�����Ƶ���ҺŨ��ƫ�ߣ�
��.����ʱ��С������������ˮ�ε�ƿ�⣬�����Ƶ���ҺŨ����Ӱ�죻
��.���ݺ���ҡ�ȡ�����������Һ����ڿ̶��ߣ�Ϊ������������ټ�����ˮ�����̶���ʹ��Һ���ƫ�����Ƶ���ҺŨ��ƫ�ͣ�������������ʹ���Ƶ���ҺŨ��ƫ�ߵ����٢����ʴ�Ϊ���٢ۡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������0.1000 mol��L��1KMnO4������Һ�ζ�δ֪Ũ�ȵ���ɫH2C2O4��Һ����Ӧ���ӷ���ʽ�ǣ�2MnO4����5H2C2O4��6H+ = 2Mn2+��10CO2����8H2O
���������⣺
��1���õζ�ʵ������IJ���������______________��������ĸ��
A����ʽ�ζ���B����ʽ�ζ��� C����Ͳ D����ƿ E������̨F���ζ��ܼ�G���ձ�H����ֽ I��©��
��2������________(��ᡱ�)ʽ�ζ���ʢ�Ÿ��������Һ���Է���ԭ��___________________________________________��
��3���ζ��յ������Ϊ___________________________________��
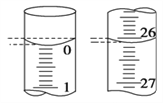
��4�����ζ���ʼ�ͽ���ʱ���ζ����е�Һ����ͼ��ʾ������ʼ����Ϊ________mL���յ����Ϊ________mL��
��5��ijѧ������3��ʵ��ֱ��¼�й��������±���
�ζ� ���� | ����H2C2O4��Һ�����/mL | 0.1000 mol/L KMnO4�������mL�� | ||
�ζ�ǰ�̶� | �ζ���̶� | ��Һ���/mL | ||
��һ�� | 25.00 | 0.00 | 26.11 | 26.11 |
�ڶ��� | 25.00 | 1.56 | 30.30 | 28.74 |
������ | 25.00 | 0.22 | 26.31 | 26.09 |
�����ϱ�������ʽ�����H2C2O4��Һ�����ʵ���Ũ��Ϊ_______________��
��6�����в����п���ʹ�ⶨ���ƫ�͵���___________(����ĸ)��
A����ʽ�ζ���δ�ñ�Һ��ϴ��ֱ��ע��KMnO4��Һ
B���ζ�ǰʢ�Ų�����Һ����ƿ������ˮϴ����û�и���
C����ʽ�ζ��ܼ��첿���ڵζ�ǰû�����ݣ��ζ���������
D����ȡKMnO4��Һʱ����ʼ���Ӷ������ζ�����ʱ���Ӷ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�������ֵ������������ȷ���ǣ� ��
A.��״���£�22.4LH2O�����ķ�����ΪNA
B.14g���������ĵ�ԭ����ΪNA
C.��״���£�22.4LNH3�����ĵ�����ΪNA
D.1molNa��Cl2��Ӧת�Ƶ�����Ϊ2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£������ΪV L���ܱ������з�����ѧ��ӦCO(g)��2H2(g) ![]() CH3OH(g)�����жϸÿ��淴Ӧ�ﵽ��ѧƽ��״̬�ı�־�ǣ� ��
CH3OH(g)�����жϸÿ��淴Ӧ�ﵽ��ѧƽ��״̬�ı�־�ǣ� ��
A. v����(CH3OH)��v����(CO) B. CO��H2��CH3OH��Ũ�ȱ�Ϊ1:2:1
C. ���������ܶȲ��ٸı� D. ��������ƽ����Է����������ٸı�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��CO(g)��H2O(g)![]() CO2(g)��H2(g)����H����41 kJ��mol��1����ͬ�¶��£����ݻ���ͬ�����������ܱ������У�����һ�����ķ�Ӧ�����Ӧ������������£�
CO2(g)��H2(g)����H����41 kJ��mol��1����ͬ�¶��£����ݻ���ͬ�����������ܱ������У�����һ�����ķ�Ӧ�����Ӧ������������£�
������� | ��ʼʱ���������ʵ���/mol | ��ƽ�������ϵ�����ı仯 | |||
CO | H2O | CO2 | H2 | ||
�� | 1 | 4 | 0 | 0 | �ų�������32.8 kJ |
�� | 0 | 0 | 1 | 4 | �����仯��Q kJ |
����˵���У�����ȷ����(����)
A. �������з�Ӧ��ƽ��ʱ��CO��ת����Ϊ80%
B. ��������CO��ת���ʵ�����������CO2��ת����
C. ƽ��ʱ����������CO2��Ũ�����
D. ������ʱCO�ķ�Ӧ���ʵ���H2O�ķ�Ӧ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����100��ʱ����0.100mol N2O4�������1L���ݳ�յ��ܱ������У�������Ӧ��N2O4��g��![]() 2NO2��g������һ��ʱ��Ը����������ʵ�Ũ�Ƚ��з����õ�������ݡ��ش��й�����;
2NO2��g������һ��ʱ��Ը����������ʵ�Ũ�Ƚ��з����õ�������ݡ��ش��й�����;
ʱ��(s) | 0 | 20 | 40 | 60 | 80 |
c(N2O4)/mol��L��1 | 0.100 | c1 | 0.050 | c3 | c4 |
c(NO2)/mol��L��1 | 0.000 | 0.060 | c2 | 0.120 | 0.120 |
��c3________c4(�>������<������)��
�������������£��ӷ�Ӧ��ʼֱ���ﵽ��ѧƽ��ʱ��N2O4��ƽ����Ӧ����Ϊ_________mol��L��1��s��1��
�۴�ƽ������������ĸı��ʹNO2����Ũ���������_______(�����)��
A�������������ݻ� B���ٳ���һ������N2O4
C�������һ������NO2 D���ٳ���һ������He
��������ͬ�����£���ʼʱֻ����0.200 mol NO2���壬��ﵽƽ��ʱNO2�����ת����Ϊ_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������绯��ʴʱ�������Ϸ����ķ�Ӧ�ǣ� ��
A.2H++2e-=H2��B.2H2O+O2+4e-=4OH-
C.Fe-2e-=Fe2+D.4OH--4e-=O2��+2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���鷨�벻���ķ��ı�(�ʡ�ī��ֽ����)�������õ��Ǻ�����ī�õ�ī���Լ���ֽ(����ֽ)������̨�õ���ʯ����Ҫ�ɷ�������
A. ���ǡ�̿�ڡ������ʡ�����
B. ���ϡ�ú̿�����ǡ�����
C. �����ʡ�̿�ڡ����ǡ�����
D. �����ʡ�ú̿�����ǡ��л�����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com