
【题目】单晶硅是信息产业中重要的基础材料.通常用碳在高温下还原二氧化硅制得粗硅(含铁、铝、硫、磷等杂质),粗硅与氯气反应生成四氯化硅(反应温度450﹣500℃),四氯化硅经提纯后用氢气还原可得高纯硅.以下是实验室制备四氯化硅的装置示意图.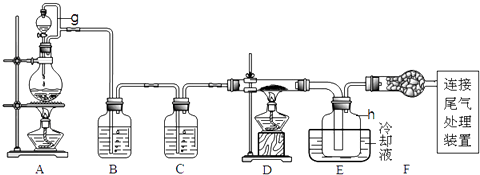
查阅相关资料获悉:
a.四氯化硅遇水极易水解;
b.铝、铁、磷在高温下均能与氯气直接反应生成相应的氯化物;
c.有关物质的物理常数见下表:
物质 | SiCl4 | AlCl3 | FeCl3 | PCl5 |
沸点/℃ | 57.7 | ﹣ | 315 | ﹣ |
熔点/℃ | ﹣70.0 | ﹣ | ﹣ | ﹣ |
升华温度/℃ | ﹣ | 180 | 300 | 162 |
请回答下列问题:
(1)写出装置A中发生反应的离子方程式 .
(2)装置A中g管的作用是;装置C中的试剂是;装置E中的h瓶需要冷却理由是 .
(3)装置E中h瓶收集到的粗产物可通过精馏(类似多次蒸馏)得到高纯度四氯化硅,精馏后的残留物中,含有铁、铝等元素的杂质.为了分析残留物中铁元素的含量,先将残留物预处理,使铁元素还原成Fe2+ , 再用KMnO4标准溶液在酸性条件下进行氧化还原反应滴定,锰元素被还原为Mn2+ . ①写出用KMnO4滴定Fe2+的离子方程式:;
②滴定前是否要滴加指示剂?(填“是”或“否”),判断滴定终点的方法是 .
③某同学称取5.000g残留物,预处理后在容量瓶中配制成100ml溶液,移取25.00ml试样溶液,用1.000×10﹣2molL﹣1KMnO4标准溶液滴定.达到滴定终点时,消耗标准溶液20.00ml,则残留物中铁元素的质量分数是 . 若滴定前平视,滴定后俯视KMnO4液面,对测定结果有何影响(填“偏高”、“偏低”、或“无影响”)
【答案】
(1)MnO2+4H++2Cl﹣ ![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
(2)平衡压强,使液体顺利流出并防止漏气;浓硫酸;产物SiCl4沸点低,需要冷凝收集
(3)5Fe2++MnO4﹣+8H+=5Fe3++Mn2++4H2O;否;当滴入最后一滴KMnO4溶液时,溶液颜色由无色变为紫色,且30秒不褪色;4.480%;偏低
【解析】解:(1)装置A是氯气发生装置,A中的离子方程式为MnO2+4H++2Cl﹣ ![]() Mn2++Cl2↑+2H2O;所以答案是:MnO2+4H++2Cl﹣
Mn2++Cl2↑+2H2O;所以答案是:MnO2+4H++2Cl﹣ ![]() Mn2++Cl2↑+2H2O;(2)浓盐酸有挥发性,故分液漏斗要加盖,加盖后如没有g管,则盐酸就不易流下去,g管的作用是平衡压强,使液体顺利流出并防止漏气;制得的氯气中含有氯化氢和水,装置B用饱和食盐水除去氯化氢,装置C用浓硫酸吸水;产物SiCl4沸点低,需要冷凝收集;所以答案是:平衡压强,使液体顺利流出并防止漏气;浓硫酸;产物SiCl4沸点低,需要冷凝收集;(3)①用KMnO4标准溶液在酸性条件下进行氧化还原滴定,反应的离子方程式是:5Fe2++MnO4﹣+8H+=5Fe3++Mn2++4H2O,所以答案是:5Fe2++MnO4﹣+8H+=5Fe3++Mn2++4H2O;②MnO4﹣转变成Mn2+溶液颜色有紫色变成无色,KMnO4标准溶液在酸性条件下进行氧化还原滴定时,不需要指示剂,判断是否达到滴定终点的方法为:当滴入最后一滴KMnO4溶液时,溶液颜色由无色变为紫色,且30秒不褪色,所以答案是:否;当滴入最后一滴KMnO4溶液时,溶液颜色由无色变为紫色,且30秒不褪色;③利用关系式法计算: 5Fe2+~MnO4﹣4×10﹣3mol 1.000×10﹣2molL﹣1×0.02L×4铁元素的质量为:4×10﹣3mol×56g/mol=2.24×10﹣1g,铁元素的质量分数
Mn2++Cl2↑+2H2O;(2)浓盐酸有挥发性,故分液漏斗要加盖,加盖后如没有g管,则盐酸就不易流下去,g管的作用是平衡压强,使液体顺利流出并防止漏气;制得的氯气中含有氯化氢和水,装置B用饱和食盐水除去氯化氢,装置C用浓硫酸吸水;产物SiCl4沸点低,需要冷凝收集;所以答案是:平衡压强,使液体顺利流出并防止漏气;浓硫酸;产物SiCl4沸点低,需要冷凝收集;(3)①用KMnO4标准溶液在酸性条件下进行氧化还原滴定,反应的离子方程式是:5Fe2++MnO4﹣+8H+=5Fe3++Mn2++4H2O,所以答案是:5Fe2++MnO4﹣+8H+=5Fe3++Mn2++4H2O;②MnO4﹣转变成Mn2+溶液颜色有紫色变成无色,KMnO4标准溶液在酸性条件下进行氧化还原滴定时,不需要指示剂,判断是否达到滴定终点的方法为:当滴入最后一滴KMnO4溶液时,溶液颜色由无色变为紫色,且30秒不褪色,所以答案是:否;当滴入最后一滴KMnO4溶液时,溶液颜色由无色变为紫色,且30秒不褪色;③利用关系式法计算: 5Fe2+~MnO4﹣4×10﹣3mol 1.000×10﹣2molL﹣1×0.02L×4铁元素的质量为:4×10﹣3mol×56g/mol=2.24×10﹣1g,铁元素的质量分数 ![]() ×100%=4.480%,若滴定前平视,滴定后俯视KMnO4液面,导致高锰酸钾的体积变小,测定结果偏低,所以答案是:4.480%;偏低.
×100%=4.480%,若滴定前平视,滴定后俯视KMnO4液面,导致高锰酸钾的体积变小,测定结果偏低,所以答案是:4.480%;偏低.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】若3.01×1023个气体分子在某状况下的体积为22.4L,则该状况下的气体摩尔体积为
A. 11.2L/mol B. 22.4L/mol C. 44.8L/mol D. 67.2L/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物甲经氧化后得乙(分子式为C2H302C1),而甲经水解可得丙.1mol丙和2mol乙反应得一种含氯的酯(C6H804Cl2),由此推断甲的结构简式为( )
A.HCOOCH2Cl
B.ClCH2CH2OH
C.CH2ClCHO
D.HOCH2CH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法不正确的是( )
A.聚氯乙烯分子中含碳碳双键
B.以淀粉为原料可制取乙酸乙酯
C.戊烷有3种同分异构体
D.油脂的皂化反应属于水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按照要求填空:
(1)下面列出了几组物质,请将物质的合适组号填写在空格上. 同位素 , 同素异形体 , 同分异构体 , 同系物 .
①金刚石与“足球烯”C60;②D与T;③16O、17O和18O;④氧气(O2)与臭氧(O3);
⑤ 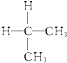 与
与 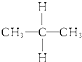 ⑥乙醇(CH3CH2OH)和甲醚(CH3OCH3);
⑥乙醇(CH3CH2OH)和甲醚(CH3OCH3);
⑦ ![]() 和
和 ![]() ;⑧
;⑧ ![]() 和
和 ![]() ;
;
(2)完成离子方程式:MnO4﹣+C2O42﹣+=Mn2++CO2↑+
(3)命名有机物: ![]()
(4)写出乙酸与甲醇(CH3OH)酯化的化学方程式 .
(5)将铂丝插入KOH溶液中做电极,并在两极片上分别通入甲烷和氧气,形成一种燃料电池:通甲烷的铂丝为原电池的极,发生的电极反应为 .
(6)PET是涤纶的主要成分,可用作饮料瓶、磁带和胶片的片基等,其结构简式如图: ![]() .该高分子材料是由两种单体通过缩聚反应制备而成,其单体的结构简式为和 .
.该高分子材料是由两种单体通过缩聚反应制备而成,其单体的结构简式为和 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组内的离子,在溶液中不能大量共存的是 ( )
A. Mg2+ K+ NO3- Cl- B. K+ Na+ Mg2+ SO42-
C. H+ SO42- Ba2+ NO3- D. Ca2+ H+ NO3- Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组利用下列装置进行进行CO2与饱和Na2CO3溶液反应制备NaHCO3实验.
(1)选取必要的实验装置,正确的连接顺序为(填序号).
(2)为确定制得的固体样品是纯净的NaHCO3 小组同学提出下列实验方案:甲方案:将样品溶液与饱和澄清石灰水反应,观察现象.
乙方案:将样品溶液与BaCl2观察现象.
丙方案:测定pH法
丁方案:热重分析法
①判定甲方案(填“可行”或“不可行”);
②为判断乙方案的可行性,某同学用分析纯的NaHCO3配制的溶液,与BaCl2溶液等体积混合进行实验,结果如下. 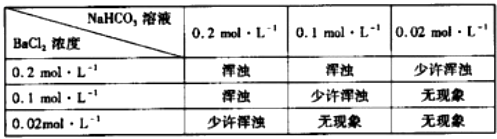
(i)此实验巳可说明乙方案是不可行的.请结合以下数据,并通过计算说明产生浑浊的原因.答: . [已知:0.1 molL﹣1 NaHC03溶液电离出的c(CO32﹣)为0.0011 molL﹣1 , Ksp(BaCO3)=5.1×10﹣9]
(ⅱ)产生浑浊的离子方程式为 .
③使用pH计进行测定的丙方案是 .
④进行丁方案实验,测得样品在不同升温速率下的热重曲线如右图.请填空:
(i)样品的纯度为 .
(ⅱ)升温速率对实验结果(填“有较大”、“有较小”或“没有”)影响.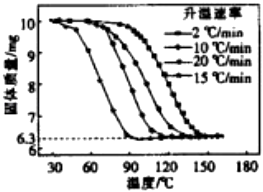
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com