
【题目】绿色化是一种生产生活方式。下列行为与“绿色化”理念不相符的是
A. 大力发展清洁能源,减少对传统能源的依赖
B. 生活垃圾分类收集处理,实现资源化再利用
C. 大量生产和贮存石灰,修复酸雨浸蚀的土壤
D. 推广共享单车,倡导低碳、环保的出行方式
科目:高中化学 来源: 题型:
【题目】(2016·江苏化学,14,4分)H2C2O4为二元弱酸。20 ℃时,配制一组c(H2C2O4)+c(HC2O![]() )+c(C2O
)+c(C2O![]() )=0.100 mol·L-1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示。下列指定溶液中微粒的物质的量浓度关系一定正确的是(双选)( )
)=0.100 mol·L-1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示。下列指定溶液中微粒的物质的量浓度关系一定正确的是(双选)( )

A.pH=2.5的溶液中:c(H2C2O4)+c(C2O![]() )>c(HC2O
)>c(HC2O![]() )
)
B.c(Na+)=0.100 mol·L-1的溶液中:c(H+)+c(H2C2O4)=c(OH-)+c(C2O![]() )
)
C.c(HC2O![]() )=c(C2O
)=c(C2O![]() )的溶液中:c(Na+)>0.100 mol·L-1+c(HC2O
)的溶液中:c(Na+)>0.100 mol·L-1+c(HC2O![]() )
)
D.pH=7.0的溶液中:c(Na+)>2c(C2O![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.芳香烃的获取主要来自煤的干馏和对石油分馏产品的催化重整
B.正丁烷转化为异丁烷一定有能量变化
C.石油的催化裂化主要目的是提高轻质液体燃料的产量尤其是汽油的产量
D.石油的常压分馏能得到润滑油、石蜡等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:![]()
(1)①反应类型______________
②反应类型________________
(2)现有如下有机物:
① CH3—CH3 ② CH2=CH2 ③ CH3CH2C![]() CH
CH
④ CH3C![]() CCH3 ⑤ C2H6 ⑥ CH3CH=CH2
CCH3 ⑤ C2H6 ⑥ CH3CH=CH2
一定互为同系物的是_______,一定互为同分异构体的是_______(填序号)
(3)人造羊毛的主要成分是聚丙烯腈(丙烯腈:CH2=CH—CN),试写出以乙炔、HCN为原料,两步反应合成聚丙烯腈的化学方程式。
①_________________________________
②_________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二碳化学的研究在工业生产中具有重要意义。
(1)在一定温度和压强下,已知:
化学键 | C—H | C—O | O—H | C=O | O=O | C—C |
键能(kJ·mol-1) | 414 | 326 | 464 | 728 | 498 | 332 |
①CH3CH2OH(g)+1/2O2(g)![]() CH3CHO(g)+H2O(g)△H1=____________。
CH3CHO(g)+H2O(g)△H1=____________。
②若2CH3CHO(g)+O2(g)![]() 2CH3COOH(g)反应可自发进行,
2CH3COOH(g)反应可自发进行,
则CH3CH2OH(g)+O2(g)![]() CH3COOH(g)+H2O(g)△H2_____0(填“>”、“<”或“=”)。
CH3COOH(g)+H2O(g)△H2_____0(填“>”、“<”或“=”)。
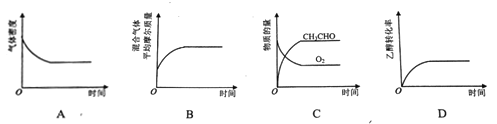
(2)将一定量CH3CH2OH和O2充入恒温、恒压密闭容器中,发生反应2CH3CH2OH(g)+O2(g)![]() 2CH3CHO(g)+2H2O(g)至平衡状态。下列图像不合理的是_________。
2CH3CHO(g)+2H2O(g)至平衡状态。下列图像不合理的是_________。
(3)己知:25℃,Ka(CH3COOH)=1.75×10-5,Kb(NH3·H2O)= 1.75×10-5, ![]() ≈1.3,lgl.3≈0.1
≈1.3,lgl.3≈0.1
①25℃,0.lmol·L-1CH3COOH 溶液的pH =______;将0.1 mol·L-1CH3COOH溶液与0.1mol·L-1的氨水等体积混合,所得溶液中离子浓度大小关系为__________________。
②25℃,0.2 mol·L-1NH4Cl溶液中NH4+水解反应的平衡常数Kh=_____ (保留2位有效数字)。
③25℃,向0.1 mol·L-1氨水中加入少量NH4Cl固体,NH3·H2O![]() NH4+ + OH-的电离平衡_______(填“正”、“逆”或者“不”)移;请用氨水和某种铵盐(其它试剂与用品自选),设计一个实验证明NH3·H2O是弱电解质___________。
NH4+ + OH-的电离平衡_______(填“正”、“逆”或者“不”)移;请用氨水和某种铵盐(其它试剂与用品自选),设计一个实验证明NH3·H2O是弱电解质___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法是还原沉淀法。该法的工艺流程为:![]()
其中第①步存在平衡:2 CrO42-(黄色)+2H+![]() Cr2O72- (橙色)+H2O
Cr2O72- (橙色)+H2O
(1) 若平衡体系的pH=12,则溶液显_______色。
(2) 能说明第①步反应达平衡状态的是______________。
a.Cr2O72-和CrO42-的浓度不变
B.2v(Cr2O72-) =v(CrO42-)
C.溶液的颜色不变
(3)第②步中,还原lmol Cr2O72-离子,需要_______mol的FeSO47H2O。
(4)第③步生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:
Cr (OH)3 (s)![]() Cr3+ (aq) +3OH- (aq)
Cr3+ (aq) +3OH- (aq)
常温下,Cr(OH)3的溶度积Ksp=c(Cr3+)·c3(OH-) = 10-32,要使0.01mol/Lc(Cr3+)开始沉淀,溶液的pH应调至__________,若使c(Cr3+)降至10-5mol/L,溶液的pH应调至___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z三种气体进行下列反应:3X+Y ![]() 2Z,在三种不同情况下测得的速率值为:
2Z,在三种不同情况下测得的速率值为:
① v(X)=1 mol·L-1·s-1; ② v(Y)=0.5 mol·L-1·s-1; ③ v(Z)=0.5 mol·L-1·s-1。
这三种情况下反应的速率大小情况为
A. ③>②>① B. ②>①>③ C. ①>②>③ D. ③>①>②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.为了探究化学反应速率及其影响因素,某研究小组以盐酸和碳酸钙反应进行了如下实验。实验方案与数据如下表,t表示收集a mLCO2所需的时间。
序号 | 反应温度/℃ | C(HCl)/ mol·L-1 | V(HCl)/ mL | 10g碳酸钙的形状 | t/min |
1 | 20 | 2 | 10 | 块状 | t1 |
2 | 20 | 2 | 10 | 粉末 | t2 |
3 | 20 | 4 | 10 | 粉末 | t3 |
4 | 40 | 2 | 10 | 粉末 | t4 |
(1)设计实验1和实验2的目的是研究 _________________对化学反应速率的影响。
(2)为研究温度对对化学反应速率的影响,可以将实验_____和实验____(填序号)作对比。
(3)将实验2和实验3作对比,可知t2___________t3(填“﹥”、“﹤”或“﹦”)。
II.在一体积为10L密闭容器中,通入一定量的CO和H2O,在 850℃时发生如下反应:
CO(g)+H2O(g)![]() CO2(g)+H2(g),CO浓度变化如图,
CO2(g)+H2(g),CO浓度变化如图,

(1)则0~4 min的平均反应速率v(CO)=_____________mol·L-1·min -1。
(2)该反应达到最大限度所需的时间为____________,此时CO的转化率为_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com