
【题目】某实验小组用下图装置制备家用消毒液,并探究其性质。
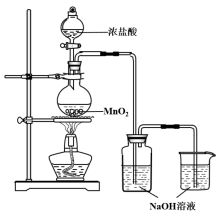
反应停止后,取洗气瓶中无色溶液5mL分别进行了如下实验:
操作 | 现象 |
a. 测溶液pH, 并向其中滴加2滴酚酞 | pH = 13, 溶液变红,5min后褪色 |
b. 向其中逐滴加入盐酸 | 溶液逐渐变成黄绿色 |
(1)写出利用上述装置制备消毒液涉及反应的化学方程式 、 。
(2)查阅资料:酚酞的变色范围为8.2~10,且酚酞在强碱性溶液中红色会褪去
为探究操作a中溶液褪色的原因,又补充了如下实验:
操作 | 现象 |
取 NaOH溶液,向其中滴加2滴酚酞 | 溶液变红,30min后褪色 |
获得结论:此实验小组制备的消毒液具有 性。
(3) 该小组由操作b获得结论:随着溶液酸性的增强,此消毒液的稳定性下降。
① 操作b中溶液变成黄绿色的原因: (用离子方程式表示)。
② 有同学认为由操作b获得上述结论并不严谨,需要进一步确认此结论的实验方案是 。
(4) 有效氯的含量是检测含氯消毒剂消毒效果的重要指标。具体用“单位质量的含氯消毒液在酸性条件下所能释放出氯气的质量”进行表征,一般家用消毒液有效氯含量在5%以上。小组同学进行如下实验测定有效氯:取此消毒液5 g,加入20 mL 0.5 mol·L-1 KI溶液,10 mL 2 mol·L-1的硫酸溶液;加几滴淀粉溶液后,用0.1 mol·L-1 Na2S2O3溶液滴定生成的I2,达滴定终点时消耗Na2S2O3 20 mL。(已知:2S2O32- + I2 === S4O62- + 2I-) 。注:相对原子质量Cl35.5,Na23,S32,O 16 ,I 127, K39
①达到滴定终点时的实验现象是 。
②此消毒液有效氯含量为 %(保留一位有效数字)。获得结论:此实验制得的消毒液 (填“符合”或“不符合”)家用要求。
【答案】(1)4HCl + MnO2 ![]() Cl2↑ + MnCl2 + 2H2O、Cl2 + 2NaOH === NaClO + NaCl + H2O
Cl2↑ + MnCl2 + 2H2O、Cl2 + 2NaOH === NaClO + NaCl + H2O
(2) 5mL pH = 13 ;漂白性
(3)① 2H+ + ClO- + Cl- === Cl2↑+ H2O
② 取洗气瓶中溶液5mL,向其中逐滴加入硫酸,观察溶液是否逐渐变为黄绿色
(4)① 溶液蓝色褪去② 1.42 % 不符合
【解析】
试题分析:(1)该装置中发生的反应有两个,一个是制取氯气,反应的方程式为4HCl + MnO2 ![]() Cl2↑ + MnCl2 + 2H2O,另一个是氯气与氢氧化钠发生反应制取消毒液,发生反应的方程式为Cl2 + 2NaOH === NaClO + NaCl + H2O。
Cl2↑ + MnCl2 + 2H2O,另一个是氯气与氢氧化钠发生反应制取消毒液,发生反应的方程式为Cl2 + 2NaOH === NaClO + NaCl + H2O。
(2)根据资料可知,酚酞在强碱性溶液中红色会褪去,则为了验证溶液褪色的原因,需要补充碱性溶液使酚酞褪色的对比实验,在这一过程中要注意物质的体积与浓度原溶液相同,所以应取5mL,PH=13的NaOH溶液;通过对比实验的现象,溶液在30min后褪色,与原实验对比5min后褪色证明溶液褪色原因为消毒液的漂白性。
(3)①溶液变成黄绿色的原因为ClO- 与 Cl-在酸性条件下发生氧化还原反应生成了氯气,反应的方程式为2H+ + ClO- + Cl- === Cl2↑+ H2O;②操作b中加入的酸为盐酸,盐酸中含有参与反应的Cl-,所以不严谨,所以补充的实验为将盐酸换成硫酸即可,故答案为取洗气瓶中溶液5mL,向其中逐滴加入硫酸,观察溶液是否逐渐变为黄绿色。
(4)①用Na2S2O3溶液滴定生成的I2,而这反应的方程式为2S2O32- + I2 === S4O62- + 2I-,则滴定终点的现象为溶液蓝色褪去;②n(Na2S2O3)=20×10-3×0.1=2×10-3mol,2S2O32- + I2 === S4O62- + 2I-,则n(I2)=1/2n(Na2S2O3)=10-3mol,消毒液在酸性条件下与KI反应的离子方程式为4H++2ClO-+2I-=Cl2+I2+2H2O,则n(Cl2)= n(I2)=10-3 mol,则有效氯含量为71×10-3/5=1.42 %<5%,则该消毒液不符合家用要求。


科目:高中化学 来源: 题型:
【题目】钯(Pd)是有机合成中常用的催化剂。一种由废钯催化剂(主要成分为Pd,还有PdO、Fe有机物残留以及其他杂质)制取金属Pd的工艺流程如图:
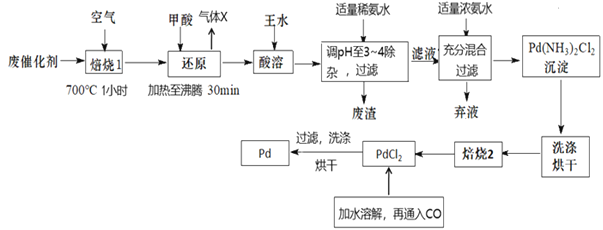
回答下列问题:
(1)废钯催化剂经烘干、粉碎后,再在700℃的高温下焙烧,不断通入足量空气的目的除了使有机物充分燃烧而除去,还可以___。
(2)查资料可知,PdO不溶于王水,加入甲酸还原PdO,其目的是___,
(3)钯在王水(浓硝酸与浓盐酸按体积比1∶3)中转化为H2PdCl4,硝酸还原为NO,该反应的化学方程式为___;酸溶时温度不能过高,原因是___。
(4)加入适量的稀氨水溶液调节pH至3~4除杂,废渣的主要成分是___。
(5)焙烧2的目的是___;
(6)有水参加情况下,可以将CO通入氯化钯(PdCl2)得到黑色金属Pd粉末,化学方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的产物中,有的有同分异构体,有的没有同分异构体,其中一定不存在同分异构体的反应是
A.异戊二烯(![]() )与等物质的量的Br2发生加成反应
)与等物质的量的Br2发生加成反应
B.2氯丁烷与NaOH乙醇溶液共热发生消去HCl分子的反应
C.甲苯在一定条件下发生硝化反应生成一硝基甲苯的反应
D.邻羟基苯甲酸与NaHCO3溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生产上用过量烧碱溶液处理某矿物(含Al2O3、MgO),过滤后得到滤液用NaHCO3溶液处理,测得溶液pH和Al(OH)3生成的量随加入NaHCO3溶液体积变化的曲线如下:
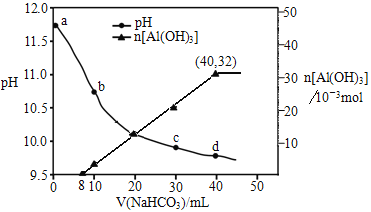
下列有关说法不正确的是
A. NaHCO3溶液的物质的量浓度为0.8 mol/L
B. b点与c点溶液所含微粒种类相同
C. a点溶液中存在的离子是Na+、AlO2-、OH-、H+
D. 生成沉淀的离子方程式为:HCO3-+AlO2-+H2O === Al(OH)3↓+CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用亚硫酸钠固体和70%的浓硫酸制备SO2气体,反应方程式为Na2SO3+H2SO4=Na2SO4+SO2↑+H2O,请设计一套实验装置,收集一试管干燥的SO2气体。
(1)在下面方框中,A表示由分液漏斗和锥形瓶组成的气体发生器,请在答题卡上的A后完成该反应的实验装置示意图(夹持装置、连接胶管不必画出,尾气处理部分必须画出,需要加热的仪器下方用△标出),按气流方向在每件仪器下方标出字母B、C…;其它可选用的仪器(数量不限)简易表示如下:___

(2)根据方框中的装置图甲,在答题卡上填写下表(可不填满)___
仪器标号 | 仪器中所加物质 | 作用 |
A | 亚硫酸钠、浓硫酸 | 产生SO2 |
(3)某实验小组用如图乙装置测定收集到的气体中SO2的含量,反应管中装有酸性高猛酸钾溶液。
①SO2和酸性高猛酸钾溶液发生反应的离子方程式为:___。
②反应管内溶液紫红色消失后,若没有及时停止通气,则测得的SO2含量___(选填:“偏高”、“偏低”或“无影响”)
③若酸性高猛酸钾溶液体积为V1mL,浓度为cmol/L,量气管内增加的水的体积为V2mL(已折算成标准状况下的体积)。用c、V1、V2表示SO2的体积百分含量为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,下列说法正确的是
A.28g乙烯与丙烯混合物中含C-H键的数目为4NA
B.标准状况下,22.4L氦气与11.2LH2含有的质子数均为NA
C.1mol Cl2与足量的铁在一定条件下充分反应,转移了3NA电子
D.25℃时,1LpH=11的NaOH溶液与1LpH=11的CH3COONa溶液,含阴离子数均为10-11NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃的衍生物A的化学式为C6H12O2,已知:

又知D不与Na2CO3反应,C和E均不能发生银镜反应,则A的结构可能有( )
A. 1种 B. 2种 C. 3种 D. 4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列金属冶炼的反应原理及方程式书写,正确的是( )
A.2AlCl3(熔融)![]() 2Al+3Cl2↑B.Fe2O3+2Al
2Al+3Cl2↑B.Fe2O3+2Al![]() Fe+Al2O3
Fe+Al2O3
C.Cu2S+O2![]() 2Cu+SO2D.Ag2O
2Cu+SO2D.Ag2O![]() 2Ag+O2↑
2Ag+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知:①Fe(s)+1/2O2(g)===FeO(s) ΔH1=-272.0 kJ·mol-1;
②2Al(s)+3/2O2(g)===Al2O3(s) ΔH2=-1 675.7 kJ·mol-1。
Al和FeO发生铝热反应的热化学方程式是__________________________。某同学认为,铝热反应可用于工业炼铁,你的判断是________(填“能”或“不能”),你的理由是_________________。
(2)反应物与生成物均为气态的某可逆反应在不同条件下的反应历程分别为A、B,如图所示。

①据图判断该反应是________(填“吸”或“放”)热反应
②其中B历程表明此反应采用的条件为_____ (填字母)。
A.升高温度 B.增大反应物的浓度 C.降低温度 D.使用催化剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com