
【题目】将如图中的K闭合,下列判断正确的是( )

A.去掉盐桥,此装置也能正常工作
B.盐桥中的K+向盛有硫酸铜溶液的烧杯移动,高锰酸根离子向b移动
C.一段时间后,硫酸铜溶液浓度减小
D.C极上的电极反应式为Fe3++e-=Fe2+
【答案】D
【解析】
原电池的构造原理要求装置能够形成闭合回路,盐桥在此使两个烧杯连接,形成闭合回路,据此分析;该原电池中Cu为负极,失电子形成铜离子,C为正极,铁离子得电子生成亚铁离子;因此b为电解池的负极,a为正极,电解池中阳离子向负极移动,阴离子向正极移动,据以上分析进行解答。
A、去掉盐桥,不能形成闭合回路,此装置不能正常工作,故A错误;
B、C极为原电池的正极,钾离子向盛有硫酸铁溶液的烧杯移动,a为电解池的阳极,高锰酸根离子向a移动,故B错误;
C、因为铜极发生氧化反应,极反应为Cu-2e-=Cu2+,所以溶液中铜离子浓度增大,故C错误;
D、C极为原电池正极,发生还原反应,极反应为Fe3++e-=Fe2+,故D正确;
故答案选D。


 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案科目:高中化学 来源: 题型:
【题目】某些化学反应可用下式表示,A+B→C+D+H2O请回答下列问题:
(1)若A、C、D均含有氯元素,且A的化合价介于C与D之间,写出该反应的离子方程式:________
(2)若气体D能使湿润的红色石蕊试纸变蓝,写出该反应的化学方程式: ____________。
(3)若A金属单质,C是一种遇空气会变为红棕色的无色气体,写出该反应的离子方程式______________
(4)若A为难溶于水的固体,C为能使澄清石灰水变浑浊的无色无味气体,请写出符合上式的离子方程式:_____________。
(5)若C、D均为气体且都能使澄清石灰水变浑浊,且D可以使品红褪色,则A与B反应的化学方程式为: _____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组欲利用CuO与NH3反应,研究NH3的某种性质并测定其组成,设计了如下实验装置(夹持装置未画出)进行实验。请回答下列问题:
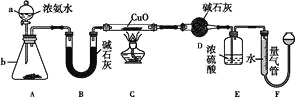
(1)仪器a的名称为____,仪器b中可选择的试剂为____。
(2)实验室中,利用装置A,还可制取的无色气体是____(填字母)。
A.Cl2 | B.O2 | C.CO2 | D.NO2 |
(3)实验中观察到装置C中黑色CuO粉末变为红色固体,量气管有无色无味的气体产生,上述现象证明NH3具有____性,写出相应的化学方程式:_______________________。
(4)E装置中浓硫酸的作用是_____________________________________。
(5)读取气体体积前,应对装置F进行的操作:____________________________。
(6)实验完毕,若测得干燥管D增重m g,装置F测得气体的体积为n L(已折算成标准状况),则氨分子中氮、氢的原子个数比为____(用含m、n字母的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇燃料电池能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注,其工作示意图如图,其总反应为:2CH3OH+3O2=2CO2+4H2O。下列说法不正确的是

A. 电极A是负极,发生氧化反应
B. 电池工作时,电解液中的H+通过质子交换膜向B电极迁移
C. 放电前后电解质溶液的pH不变
D. b物质在电极上发生的电极反应式为:O2+4e-+4H+=2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是一种正投入生产的大型蓄电系统,放电前,被膜隔开的电解质为Na2S2和NaBr3,放电后分别变为Na2S4和NaBr。下列叙述正确的是( )
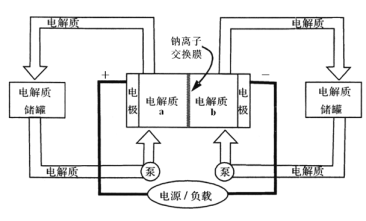
A. 放电时,负极反应为3NaBr-2e-=NaBr3+2Na+
B. 充电时,阳极反应为2Na2S2-2e-=Na2S4+2Na+
C. 放电时,Na+经过离子交换膜,由b池移向a池
D. 用该电池电解饱和食盐水,产生2.24 L H2时,b池生成17.40gNa2S4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图的各方框表示有关的一种反应物或生成物(某些物质已经略去),常温下A、C、D为无色气体,C能使湿润的红色石蕊试纸变蓝。

(1)写出下列各物质的化学式:X:______A:______C:______F:______。
(2)写出下列变化的化学方程式:
X![]() :______;
:______;
C→E:______;
F→G:______;
(3)检验X中阳离子的方法:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磺酰氯(SO2Cl2)在医药、染料行业有重要用途,也可用于制备表面活性剂。沸点为69.2℃,遇水水解,剧烈反应生成两种强酸。学习小组在实验室用SO2和Cl2在活性炭作用下,制备SO2Cl2并测定产品纯度,设计如图实验如图1(夹持装置略去)。请回答下列问题:
Ⅰ.SO2的制备
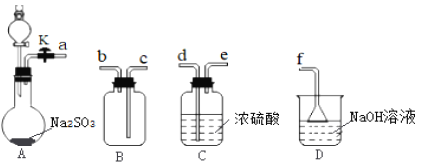
(1)欲收集一瓶干燥的SO2,装置中气流方向合理的连接顺序为____(填小写字母)。
(2)A装置分液漏斗中装的是70%的硫酸溶液,A中反应的化学方程式为____。
Ⅱ.SO2Cl2的制备和纯度的测定
将上述收集到的SO2充入注射器h中,用图2装置制备SO2Cl2。

(3)仪器e的名称为____,b中试剂的名称为____。
(4)f的作用是____。
(5)取反应后的产品4.0g,配成200mL溶液;取出20.00mL,用0.5000mol ·L-1NaOH溶液滴定;达到滴定终点时消耗标准液的体积为20.00mL(杂质不参加反应)。
①产品加水配成溶液时发生的反应为____。
②SO2Cl2的质量分数为____。(保留三位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃、101kPa时,C(s)、H2(g)、CH3COOH(l)的燃烧热分别为393.5kJ/mol、285.8kJ/mol、870.3kJ/mol,则2C(s)+2H2(g)+O2(g)= CH3COOH(l)的焓变为( )
A. -488.3kJ/molB. 488.3kJ/molC. 191kJ/molD. -191kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中溶质的物质的量浓度为1 mol/L的是
A.将40g NaOH溶解于1L水中配成的溶液
B.将80gSO3溶于水配成1L溶液(已知,SO3+H2O=H2SO4)
C.将0.5mol/L的NaNO3溶液100mL加热蒸发掉50g水后的溶液
D.含K+为2mol的K2SO4溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com