
【题目】如图为实验室制取和收集纯净干燥的氯气,并进行氯气性质探究的实验装置图:
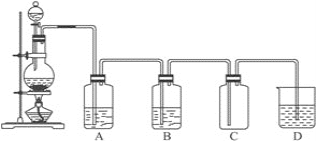
(1)反应前,在__中装浓盐酸(填写仪器名称),__中装MnO2(填写仪器名称)。
(2)装置A中所装试剂是__,目的__。装置B中所装的试剂是___,目的__。
(3)装置D中所装试剂是__,发生反应的化学方程式为__。
(4)实验室制取Cl2的化学方程式___。
【答案】分液漏斗 圆底烧瓶 饱和食盐水 除去氯气中的氯化氢 浓硫酸 干燥氯气 氢氧化钠溶液 Cl2+2NaOH=NaCl+NaClO+H2O MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
【解析】
实验室制取纯净、干燥的氯气,首先用MnO2和浓盐酸在圆底烧瓶中反应,生成的氯气中混有氯化氢和水蒸气,先用饱和食盐水除去氯化氢,再通过浓硫酸除去水蒸气,用向上排空气法收集氯气,多余的氯气用氢氧化钠溶液吸收,防止污染环境。
(1)装浓盐酸的仪器是分液漏斗,装MnO2的仪器是圆底烧瓶。
(2)装置A中所装试剂是饱和食盐水,目的是除去氯气中的氯化氢。装置B中所装的试剂是浓硫酸,目的是干燥氯气。
(3)装置D中所装试剂是氢氧化钠溶液,吸收多余的氯气,防止氯气逸出污染环境。发生反应的化学方程式为Cl2+2NaOH=NaCl+NaClO+H2O。
(4)实验室用MnO2和浓盐酸制取Cl2的化学方程式为MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】美国圣路易斯大学研制了一种新型的乙醇电池,用质子(H+)溶剂,在200℃左右时供电。电池总反应为:C2H5OH +3O2=2CO2+3H2O,电池示意如下图,下列说法正确的是
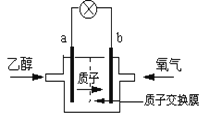
A. a极为电池的正极
B. 电池工作时电子由b极沿导线经灯泡再到a极
C. 电池正极的电极反应为:4H+ + O2+ 4e=2H2O
D. 电池工作时,1mol乙醇被氧化时就有6mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由丙烯经下列反应可得到F、G两种高分子化合物,它们都是常用的塑料。
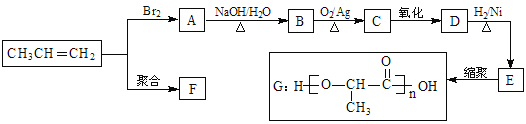
(1)D中官能团名称______________________。
(2)丙烯转化为A的反应类型为___________,A转化为B的反应类型为___________。
(3)E的化学名称为______________________。
(4)丙烯聚合为F的化学方程式是_________________________________
(5)写出C与银氨溶液反应的化学方程式________________________________________。
(6)E有多种同分异构体,其中一种能发生银镜反应,且核磁共振氢谱有五组峰,则该种同分异构体的结构简式为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应3Fe(s)+4H2O(g)![]() Fe3O4(s)+4H2(g)在温度和容积不变的条件下进行。下列叙述能表明反应达到平衡状态的是( )
Fe3O4(s)+4H2(g)在温度和容积不变的条件下进行。下列叙述能表明反应达到平衡状态的是( )
A.容器内压强不再改变B.v(H2O)=v(H2)
C.气体的密度不再改变D.反应不再进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组在实验室中探究金属钠与二氧化碳的反应。回答下列问题:

(1)选用如图所示装置及药品制取CO2。打开弹簧夹,制取CO2。为了得到干燥.纯净的CO2,产生的气流应依次通过盛有_________的洗气瓶(填试剂名称)。反应结束后,关闭弹簧夹,可观察到的现象是____________________________。不能用稀硫酸代替稀盐酸,其原因是______________________________。
(2)金属钠与二氧化碳反应的实验步骤及现象如下表:
步骤 | 现象 |
将一小块金属钠在燃烧匙中点燃,迅速伸入盛有CO2的集气瓶中。充分反应,放置冷却 | 产生大量白烟,集气瓶底部有黑色固体产生,瓶壁上有白色物质产生 |
在集气瓶中加入适量蒸馏水,振荡.过滤 | 滤纸上留下黑色固体,滤液为无色溶液 |
①为检验集气瓶瓶壁上白色物质的成分,取适量滤液于2支试管中,向一支试管中滴加1滴酚酞溶液,溶液变红:向第二支试管中滴加澄清石灰水,溶液变浑浊。
据此推断,白色物质的主要成分是________(填标号)。
A.Na2O B.Na2O2 C.NaOH D.Na2CO3
②为检验黑色固体的成分,将其与浓硫酸反应,生成的气体具有刺激性气味。据此推断黑色固体是________________。
③本实验中金属钠与二氧化碳反应的化学方程式为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在工业上可用含SiO2、CeO2和Fe2O3的废料作原料来获得硫酸铁铵晶体(Fe2(SO4)3·2(NH4)2 SO4·3H2O),同时可回收CeO2,工艺流程设计如下
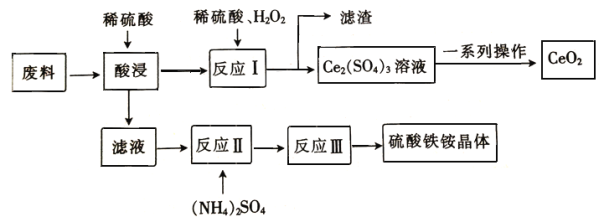
已知: ①SiO2、CeO2不溶于稀硫酸;②酸性条件下,CeO2可与H2O2反应;③“反应Ⅰ”所得溶液中含有Ce3+;④碱性条件下,NH4+与OH-结合生成NH3·H2O。
请回答下列问题
(1)“酸浸”时未发生的反应 物质是__________________(填化学式)。
(2)“滤液”中含有的阳离子有___________________(填离子符号)。
(3)写出“反应Ⅰ”的化学方程式:________________________________________。
(4)在酸性条件下,H2O2、CeO2两种物质中,氧化性较弱的是__________________(填化学式)。
(5)若往硫酸铁铵溶液中加入过量的NaOH,写出该反应的离子方程式:_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)在室温下,等体积、等浓度的氢氧化钠与醋酸混合后溶液呈__性,溶液中c(Na+)__c(CH3COO-)(填“>”“=”或“<”);pH=13的氢氧化钠与pH=1的醋酸等体积混合后溶液呈__性,溶液中c(Na+)___c(CH3COO-)(填“>”“=”或“<”);
(2)下列溶液,①0.1mol/L HCl溶液②0.1mol/L H2SO4溶液③0.1mol/L NaOH溶液④0.1mol/L CH3COOH溶液,按pH由小到大顺序为___。
(3)CuSO4的水溶液呈酸性的原因是(用离子方程式表示):____;实验室在配制CuSO4的溶液时,常将CuSO4固体先溶于较浓的硫酸中,然后再用蒸馏水稀释到所需的浓度,以___(填“促进”、“抑制”)其水解。
(4)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,充分反应后溶液呈中性,则反应后溶液存在的离子有____,其浓度由大到小的顺序为_____,氨水的浓度a__0.01 mol·L-1(填“>”、“ <”或“=”)。
(5)已知:难溶电解质Cu(OH)2在常温下的KSP=2×10-20,则常温下:某CuSO4溶液中c(Cu2+)=0.02molL-1,如要生成Cu(OH)2沉淀,应调整溶液的pH最小为____。
(6)某工厂的电镀污泥中含有铜、铁等金属化合物。为实现资源的回收利用并有效防止环境污染,设计如下工艺流程:


①酸浸后加入H2O2的目的是_____________,调pH的最适宜范围为_______。
②调pH过程中加入的试剂最好是_________。
A.NaOH B.CuO C.NH3·H2O D.Cu2(OH)2CO3
③煮沸CuSO4溶液的原因是_____;向CuSO4溶液中加入一定量的NaCl、Na2SO3,可以生成白色的CuCl沉淀,反应的化学方程式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国“神舟七号”载人飞船的火箭燃料主要是偏二甲肼(用R表示)和四氧化二氮,在火箭发射时,两者剧烈反应产生大量气体并释放出大量的热,该反应的化学方程式为:R+2N2O4═3N2+4H2O+2CO2,下列叙述错误的是
A.此反应是氧化还原反应
B.R的分子式为C2H8N2
C.在反应中N2O4做还原剂
D.生成3mol N2时电子转移数为16mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是巨大的资源宝库,工业上从海水中提取食盐和溴的过程如图:

操作Ⅱ发生反应的离子方程式为___;如果用碳酸钠溶液代替操作Ⅱ中的二氧化硫水溶液,则生成物中溴的化合价分别为+5和﹣1价,且操作Ⅲ中用稀硫酸代替氯气,请写出这种情况下操作Ⅲ中发生反应的离子方程式:___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com