
| 6.4g |
| 80g/mol |
| 100mL |
| 20mL |
| 6.20g |
| 310g/mol |
| 100mL |
| 20mL |
| 46.2g-64g/mol×0.4mol-95g/mol×0.2mol |
| 16g/mol |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
 结构的有机物可被酸性高锰酸钾溶液氧化成二元醇,如:CH2=CH2
结构的有机物可被酸性高锰酸钾溶液氧化成二元醇,如:CH2=CH2| 酸性高锰酸钾溶液 |
 )为原料合成环状化合物F和高分子化合物E和G.
)为原料合成环状化合物F和高分子化合物E和G.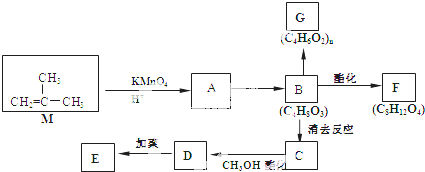
查看答案和解析>>
科目:高中化学 来源: 题型:
 某稀硫酸和硝酸的混合溶液200mL,分成两份.向其中一份逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO).向另一份逐渐加入铁粉,产生气体的量随铁粉质量增加的变化曲线如图所示.
某稀硫酸和硝酸的混合溶液200mL,分成两份.向其中一份逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO).向另一份逐渐加入铁粉,产生气体的量随铁粉质量增加的变化曲线如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2a=b | B、a=2b |
| C、a=b | D、无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Mg、Al合金 |
| B、Cu、Zn合金 |
| C、Zn、Fe合金 |
| D、Mg、Zn合金 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 ⑦CH3-CH2-CH2-O-CH3⑧CH2═CH-CH2-CH2-CH3
⑦CH3-CH2-CH2-O-CH3⑧CH2═CH-CH2-CH2-CH3查看答案和解析>>
科目:高中化学 来源: 题型:



查看答案和解析>>
科目:高中化学 来源: 题型:
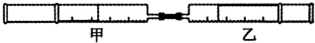
| 实验序号 | 甲针筒内物质 | 乙针筒内物质 | 乙针筒里的现象 |
| A | HCl | AgNO3溶液 | 产生白色沉淀 |
| B | NH3 | FeCl3溶液 | 出现红褐色沉淀 |
| C | CO2 | BaCl2 | 产生白色沉淀 |
| D | Cl2 | 紫色石蕊溶液 | 先变红后褪色 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Y2-的离子半径大于W3+的离子半径 |
| B、Y、Z形成的化合物为离子化合物 |
| C、W的最高价氧化物对应的水化物的酸性比X的强 |
| D、Z的气态简单氢化物的稳定性比R的强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com