
����Ŀ���������Ρ����Ӽ������������HPF�����Һ�е���Ҫ��Ⱦ��(���л�����Cl����SO![]() ��Na����)������NaClO3��H2SO4���ѳ����Լ���
��Na����)������NaClO3��H2SO4���ѳ����Լ���
��1��Cl2���ȵ�NaOH��Һ��Ӧ����NaClO3���÷�Ӧ�Ļ�ѧ����ʽΪ____________________________��
��2�� ����ʱ����ӦC6H5O����H2O ![]() C6H5OH��OH����ƽ�ⳣ��ΪK��________(C6H5OH��Ka��1��10��10)��
C6H5OH��OH����ƽ�ⳣ��ΪK��________(C6H5OH��Ka��1��10��10)��
��3�������÷�ˮ�辭Ԥ�������ٴ����Ρ�
����Ũ�����600 mL HPF�����Һ�����ữԤ����(��Ӧ�¶�100��)���������1��ʾ��
��1��Ԥ����ǰ����������Ũ�ȱ仯���
��Ŀ | S2O | SCN��(g��L��1) | ����(g��L��1) | pH |
����ǰ | 34.28 | 70.11 | 1.3 | 8.55 |
������ | 0.91 | 69.76 | 1.35 | 2.4 |
�ɱ�1��֪���ô�����������Ҫ����ȥ����Ⱦ����________��
����Ԥ�������Һ�����ٴ���(��Ӧ�¶�100 ��)ʱ��13���������Һ�м����Լ�������2��ʾ��
��2��13�����μ����Լ����
���� | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
NaClO3/g | 16.3 | 0 | 0 | 0 | 0 | 0 | 7.6 | 0 | 5.7 | 0 | 10.9 | 0 | 7.1 |
ŨH2SO4/mL | 0 | 2 | 2 | 2 | 4 | 4 | 0 | 4 | 0 | 4 | 0 | 4 | 0 |
ʵ������ͼ1��ʾ��

ǰ6�α����ѳ��ʿɴﵽ80%�������ù����б���ת��Ϊ��ɫ����(������)��������Һ��ClO![]() ��Cl����Ӧ����Cl2�йء��ð�ɫ�������ܵĽṹ��ʽΪ______________��
��Cl����Ӧ����Cl2�йء��ð�ɫ�������ܵĽṹ��ʽΪ______________��
���ɱ�2��ͼ1�����ݵó�����7��13�β�����SCN���ڽ�ǿ���������±�ClO![]() (��ˮ��)������������________���˹����в�������ש��ɫ����(����������ɫ����)���Գ�������XPS����������Ԫ�ص����ʵ���������ͼ2��ʾ����֪SCN���ɱ�ijЩ������(��Cu2����)��������Ϊש��ɫ�ij���(SCN)x��һ���Ʋ���Ϊ��ʵ���в�����ש��ɫ����Ϊ(SCN)x��֧�ָ��Ʋ��֤���У�________��
(��ˮ��)������������________���˹����в�������ש��ɫ����(����������ɫ����)���Գ�������XPS����������Ԫ�ص����ʵ���������ͼ2��ʾ����֪SCN���ɱ�ijЩ������(��Cu2����)��������Ϊש��ɫ�ij���(SCN)x��һ���Ʋ���Ϊ��ʵ���в�����ש��ɫ����Ϊ(SCN)x��֧�ָ��Ʋ��֤���У�________��
���𰸡� 3Cl2 �� 6NaOH![]() NaClO3��5NaCl��3H2O 1��10��4 S2O
NaClO3��5NaCl��3H2O 1��10��4 S2O![]() (���������) ClClOHCl(��ClOHCl��ClOH�� ��7��9��11��13�μ���NaClO3ʱ��pH����������SCN���ѳ�����Ӧ����(��7��13�μ���NaClO3ʱSCN���ѳ��������������������ѳ�����������) SCN���ɱ�ijЩ������(��Cu2����)����Ϊש��ɫ�ij�����ClO
(���������) ClClOHCl(��ClOHCl��ClOH�� ��7��9��11��13�μ���NaClO3ʱ��pH����������SCN���ѳ�����Ӧ����(��7��13�μ���NaClO3ʱSCN���ѳ��������������������ѳ�����������) SCN���ɱ�ijЩ������(��Cu2����)����Ϊש��ɫ�ij�����ClO![]() ���н�ǿ����������SCN��Ҳ�ɱ�ClO
���н�ǿ����������SCN��Ҳ�ɱ�ClO![]() ������������N��S���ʵ���֮�ȼ���Ϊ1��1�һ���C
������������N��S���ʵ���֮�ȼ���Ϊ1��1�һ���C
��������(1)������ɵ�Cl2���ȵ�NaOH ��Һ��Ӧ�Ļ�ѧ����ʽΪ3Cl2+6NaOHNaClO3+ 5NaCl+3H2O��
(2)��֪C6H5OH��Ka=1��10-10����ӦC6H5O-+H2O![]() C6H5OH+OH -��ƽ�ⳣ��ΪK=
C6H5OH+OH -��ƽ�ⳣ��ΪK=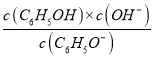 =
= 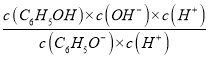 =
= ![]() = 1��10-4��
= 1��10-4��
(3) ���ɱ�-1���ݵı仯��֪���ô�����������Ҫ����ȥ����Ⱦ����S2O32-����������Σ�������Һ��ClO3-��Cl-��Ӧ������Cl2���뱽�ӷ�Ӧ�������ȱ��Ӱ�ɫ��������ṹ��ʽΪ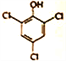 ������ͼ1��֪����NaClO3������pH����SCN-�ѳ��������������������ѳ�����������������SCN-�ڽ�ǿ���������±�ClO3-������������Ŀ������֪SCN-�ɱ�ijЩ����������Cu2+�ȣ�����Ϊש��ɫ�ij�����ClO3-���н�ǿ�������ԣ���ͼ��2��֪������N��S���ʵ���֮�ȼ���Ϊ1��1���һ�����CԪ�أ����Ը�ʵ���в�����ש��ɫ����Ϊ(SCN)x��
������ͼ1��֪����NaClO3������pH����SCN-�ѳ��������������������ѳ�����������������SCN-�ڽ�ǿ���������±�ClO3-������������Ŀ������֪SCN-�ɱ�ijЩ����������Cu2+�ȣ�����Ϊש��ɫ�ij�����ClO3-���н�ǿ�������ԣ���ͼ��2��֪������N��S���ʵ���֮�ȼ���Ϊ1��1���һ�����CԪ�أ����Ը�ʵ���в�����ש��ɫ����Ϊ(SCN)x��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Һ���������ʵ���Ũ�ȹ�ϵ��ȷ����
A. 25 ��ʱ����0.1 mol��L��1 NH4HSO4��Һ�еμ�NaOH��Һ�����ԣ�c(Na��)>c(NH)>c(SO![]() )>c(OH��)��c(H��)
)>c(OH��)��c(H��)
B. 25 ��ʱ��NaB��Һ��pH��8��c(Na��)-c(B��)��9.9��10��7 mol��L��1
C. 0.1![]()
![]() ��Һ��
��Һ��![]()
D. ��ͬ���ʵ���Ũ�ȵ�CH3COONa��NaClO�Ļ��Һ�У�������Ũ�ȵĴ�С��ϵ�ǣ�c(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʫ����û���̺���ѧ�仯����
A. ��������һ��� B. ˪Ҷ���ڶ��»� C. �����з�ź��� D. ���ɻƺӱ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ȼ��ﲻ���ý��������ᷴӦ�õ����ǣ� �� ��FeCl3��FeCl2��CuCl2��MgCl2 ��
A.�٢ڢ�
B.�٢�
C.�ڢ�
D.�٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������茶��������֯���ľ�ļӹ��ķ�����ȡ��ɶ������̵���ԭ����ȡ������茶��岽�����£�
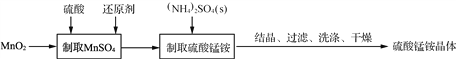
��1��ʵ��ǰ�������MnO2��������������Ϊ____________________________��
��2�� ����ȡMnSO4��ʱ������C6H12O6(������)��H2C2O4(����)����������ԭ����
����C6H12O6����ԭ��(������ΪCO2)ʱ��������Ӧ��n(MnO2)/n(C6H12O6)��________����
����H2C2O4����ԭ����������Ӧ�Ļ�ѧ����ʽΪ____________________________��
��3��һ�ֲⶨ������茶���[��Ϊ�� (NH4)xMny(SO4)z��wH2O]��ɵķ������£�
����ȡһ������������茶������250 mL��ҺA��
��ȡ25.00 mL��ҺA����������BaCl2��Һ��BaSO4 0.512 6 g��
����ȡ25.00 mL��ҺA����10 mL 20%�����Լ�ȩ��Һ��ҡ�ȡ�����5 min[4NH![]() ��6HCHO===3H����6H2O��(CH2)6N4H�����ζ�ʱ��1 mol(CH2)6N4H����1 mol H���൱]������1��2�η�̪��Һ����0.100 0 mol��L��1 NaOH����Һ�ζ����յ�(�ڸù�����Mn2��������)������NaOH��Һ22.00 mL��
��6HCHO===3H����6H2O��(CH2)6N4H�����ζ�ʱ��1 mol(CH2)6N4H����1 mol H���൱]������1��2�η�̪��Һ����0.100 0 mol��L��1 NaOH����Һ�ζ����յ�(�ڸù�����Mn2��������)������NaOH��Һ22.00 mL��
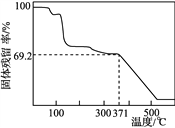
��ȡһ������Ʒ�ڿ����м�������Ʒ�Ĺ��������(������Ʒ��ʣ������/������Ʒ����ʼ������100%)���¶ȵı仯����ͼ��ʾ(��Ʒ��371 ��ʱ����ȫʧȥ�ᾧˮ)����������ʵ�����ݼ���ȷ��������茶���Ļ�ѧʽ(д���������)��__________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͨ�����·�Ӧ�ɻ��������Դ������(CH3OCH3)������˵������ȷ����
��C(s) + H2O(g)��CO(g) + H2(g) ��H1 = a kJmol-1
��CO(g) + H2O(g)��CO2 (g) + H2 (g) ��H2 = b kJmol-1
��CO2(g) + 3H2(g)��CH3OH(g) + H2O(g) ��H3= c kJmol-1
��2CH3OH(g)��CH3OCH3(g) + H2O(g) ��H4= d kJmol-1
A. ��Ӧ������Ϊ��Ӧ���ṩԭ����
B. ��Ӧ��Ҳ��CO2��Դ�����õķ���֮һ
C. ��ӦCH3OH(g)![]() 1/2 CH3OCH3 (g) +1/2H2O(l)����H=d/2kJ��mol1
1/2 CH3OCH3 (g) +1/2H2O(l)����H=d/2kJ��mol1
D. ��Ӧ 2CO(g) + 4H2 (g)![]() CH3OCH3 (g) + H2O(g)����H= ( 2b+ 2c+d)
CH3OCH3 (g) + H2O(g)����H= ( 2b+ 2c+d)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͨ����Ӧ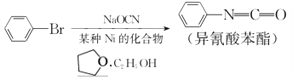 �����Ʊ��л��м��������ᱽ����
�����Ʊ��л��м��������ᱽ����
��1�� Ni3����̬��������Ų�ʽΪ________��
��2�������ᱽ��������̼ԭ���ӻ����������________��1 mol�����ᱽ�������к���������ĿΪ________��
��3��Na��O��C��N����Ԫ�صĵ�һ�����ܴӴ�С��˳��Ϊ_________________________��
��4�� C2H5OH�ķе����![]() ��������Ϊ__________________��
��������Ϊ__________________��
��5�� Ni��Al�γɵ�һ�ֺϽ����������ɻ�������ҶƬ���侧���ṹ����ͼ��ʾ���úϽ�Ļ�ѧʽΪ________��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���¶�ΪT1ʱ���������ݻ���Ϊ1L�ĺ����ܱ������н�������Ӧ:2NO2(g) =2NO(g)+O2(g) (����Ӧ����)��ʵ����:v��= v(NO2)����= k��c2(NO2) v��=v(NO)����=2v(O2)����=k��c2(NO)��c(O2)��k����k��Ϊ���ʳ��������¶�Ӱ�졣����˵������ȷ����
���� ��� | ���ʵ�ƽ��Ũ��(mol/L) | ���ʵ���ʼŨ��(mol/L) | ||
c(NO2) | c(NO) | c(O2) | c(O2) | |
�� | 0.6 | 0 | 0 | 0.2 |
�� | 0.3 | 0.5 | 0.2 | |
�� | 0 | 0.5 | 0.35 | |
A. �¶�ΪT1,��Ӧ��ƽ��ʱ���������е�ƽ�ⳣ��K=0.8
B. ��ƽ��ʱ�����ʳ����ͻ�ѧƽ�ⳣ���Ĺ�ϵK= k��/k��
C. ���¶ȸı�ΪT2ʱ����k��=k����T21
D. ��������Ӧ��ƽ��ǰ��v��>v��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��PEI [ ]��һ�ַǽᾧ�����ϡ���ϳ�·�����£�ijЩ��Ӧ�������Լ�����ȥ����
]��һ�ַǽᾧ�����ϡ���ϳ�·�����£�ijЩ��Ӧ�������Լ�����ȥ����

��֪��
��1��AΪ��״����A�Ļ�ѧ����Ϊ______��
��2��A��B�ķ�Ӧ����Ϊ______��
��3�����й���D��˵������ȷ����______������ĸ����
a��������̼̼˫��
b�������ۺ���ĵ���
c������������ˮ����
��4��F��4-��-1��2-���ױ��������Ƶá�F�����������У�Cl��______��
��5��C�ĺ˴Ź��������У�ֻ��һ�����շ塣����2-�����Ϊ�л�ԭ�ϣ�ѡ�ñ�Ҫ�����Լ�Ҳ�ܺϳ�Cд���йػ�ѧ����ʽ��______��
��6��F��K �ķ�Ӧ�������ж��ָ��������һ�ֺ���3�������л���Ľṹ��ʽ��___��
��7����E��KΪԭ�Ϻϳ�PEI��Ϊ������Ӧ��

д���м����1���м����2�Ľṹ��ʽ��______��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com