
【题目】下列离子方程式中正确的是:
A. 少量SO2通入NaOH溶液中:OH-+SO2→HSO3-
B. H2S通入氯水中:S2-+Cl2→S↓+2Cl-
C. 二氧化氮溶于水:3NO2+H2O →2H++2NO3-+NO↑
D. 少量NaHSO4与过量Ba(OH)2溶液反应:2H++SO42-+Ba2++2OH-→BaSO4↓+2H2O
科目:高中化学 来源: 题型:
【题目】与甲醇燃料电池相比,乙醇燃料电池具有毒性低、理论能量密度高等优点,因此被广泛认为是更有前途的燃料电池。如图是一个乙醇燃料电池工作时的示意图。乙池中的两个电极均为石墨电极,乙池中盛有100mL3.00mol·L-lCuSO4溶液。请回答下列问题:

(1)甲池为_________装置,M极是_________极。
(2)写出甲池中加入乙醇一极的电极反应式:________________________。
(3)N极的电极反应式为____________________________。
(4)在此过程中,乙池中某一电极析出金属铜6.4g时,甲池中理论上消耗氧气的体积为_________ L(标准状况下)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,ΔH1=-393.5 kJ·mol-1,ΔH2=-395.4 kJ·mol-1,下列说法或表示式正确的是( )
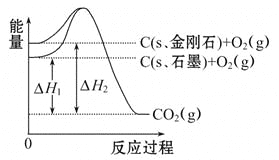
A. C(s、石墨)=C(s、金刚石)ΔH=+1.9 kJ·mol-1
B. 石墨和金刚石的转化是物理变化
C. 金刚石的稳定性强于石墨
D. 1 mol石墨的能量比1 mol金刚石的总能量大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是常温下部分短周期元素,最高价氧化物对应水化物的等物质的量浓度稀溶液的pH值与原子序数的关系图,其中H的氧化物是两性氧化物。下列说法正确的是

A. 元素B对应的氢化物比J对应的氢化物熔沸点更高,原因是B的氢化物中的键能比J中的大。
B. 根据图形分析可知,K、L两种元素最高价氧化物对应的水化物的酸性,前者较强。
C. 晶体IC2熔化时克服的化学键和晶体KC2与水反应时克服的化学键,类型相同。
D. 元素K、H、G分别形成的简单离子的半径逐渐减少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于硅及其化合物的叙述正确的是
A. 陶瓷、玻璃、水泥都是硅酸盐产品
B. 硅晶体可用于制造光导纤维
C. 二氧化硅在电子工业中是重要的半导体材料
D. 二氧化硅与氢氟酸和氢氧化钠均能反应,属于两性氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:下列描述正确的是( ) 
A.反应开始到10s,用Z表示的反应速率为0.158mol/(Ls)
B.反应开始到10s,X的物质的量浓度减少了0.79mol/L
C.反应开始到10s时,Y的转化率为79.0%
D.反应的化学方程式为:X(g)+Y(g)Z(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验兴趣小组用如下两种方法制取氮气。

已知:活性炭可用于吸附水中的絮状沉淀。
(1)方法一所发生反应的化学方程式为_________________。
(2)检验方法一反应后所得溶液中是否含有NH4+的实验方法是_________________。
(3)方法二被冰水冷却的U 型管中所得物质是_________________,用冰水冷却的目的是_________________。
(4)方法一与方法二相比所具有的优点是_________________。
(5)方法一和方法二中均需用到NH4Cl,NH4Cl的溶解度随温度变化的曲线如右图所示,工业NH4Cl固体中含有少量的FeCl2,可通过如下实验来提纯:将工业NH4Cl固体溶于水,_________,调节溶液的pH为4~5,向溶液中加入活性炭,将溶液加热浓缩,________获得纯净的NH4Cl固体。(实验中可供选择的试剂有:双氧水、KMnO4溶液)

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】与自然界中的许多变化一样,化学反应具有方向性。下列有关叙述中正确的是
A.原电池反应一定是自发进行的氧化还原反应,且△H<0
B.ΔH<0,ΔS<0的反应肯定能自发进行
C.体系能量增大和混乱度增大都有促使反应自发进行的倾向
D.CaCO3(s) =CaO(s)+CO2(g)的ΔH>0,ΔS<0,该反应在较高温度下能自发进行
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com