
科目:高中化学 来源: 题型:
对实验Ⅰ~Ⅳ的实验现象预测正确的是( )

A .实验Ⅰ:液体分层,下层呈无色
.实验Ⅰ:液体分层,下层呈无色
B.实验Ⅱ:烧杯中先出现白色沉淀,后溶解
C.实验Ⅲ:试管中立刻出现红色沉淀
D.实验Ⅳ:放置一段时间后,饱和CuSO4溶液中出现蓝色晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
燃烧热是指一定条件下1 mol可燃物完全燃烧生成稳定的氧化物时放出的热量。已知热化学方程式:①CO(g)+1/2 O2(g)====CO2(g)ΔH = -283.0 kJ·mol-1
②H2(g)+ 1/2O2(g)====H2O(g)ΔH = -241.8 kJ·mol-1
则下列说法正确的是( )
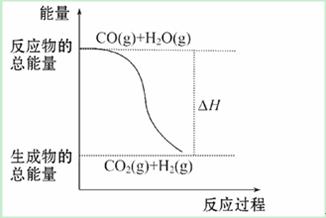
A. 由反应①、②可知如图所示的热化学方程式为CO(g)+H2O(g)==== CO2(g)+H2(g)ΔH = -41.2 kJ·mol-1
B. H2的燃烧热为241.8 kJ·mol-1
C.H2(g)转变成H2O(g)的化学反应一定要释放能量
D.根据②推知反应H2(g)+1/2O2(g)==== H2O(l)ΔH > -241.8 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
以惰性电极电解下列物质的水溶液(电解质均过量),电解后溶液pH升高的是
①盐酸 ②硫酸 ③氢氧化钾 ④氯化钾 ⑤硝酸银 ⑥硫酸钠
A.①②③ B.④⑤⑥ C.①③④ D.②⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液c ;
A、B是两块电极板,通过导线与直流电相连。请回答以下问题:
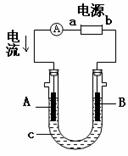 (1)若A、B都是惰性电极,c是饱和NaCl溶液,实验开始时,同时在U形管两边各滴入几滴酚酞试液,则:
(1)若A、B都是惰性电极,c是饱和NaCl溶液,实验开始时,同时在U形管两边各滴入几滴酚酞试液,则:
① B是 极(填“阴”或“阳”), B极逸出
(填:黄绿或无色)气体,同时B极附近溶液呈 色。
② 电解池中A极上的电极反应式为 。
B极上的电极反应式为 。
(2)如要进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,电解液c选用CuSO4溶液,则:
① A电极的材料是 ,电极反应式是 。
② B电极的材料是 ,电极反应式是 。
(说明:杂质发生的电极反应不必写出)
③下列说法正确的是________。
a.电能全部转化为化学能
b.在电解精炼过程中,电解液中伴随有Al3+、Zn2+产生
c.溶液中Cu2+向阳极移动
d.利用阳极泥可回收Ag、Pt、Au等金属
(3)用惰性电极电解CuSO4溶液。若阴极析出Cu的质量为12.8 g ,则阳极上产生的气体在标准状况下的体积为 L 。
(4)利用反应2Cu+O2+2H2SO4===2CuSO4+2H2O可制备CuSO4,若将该反应设计为电解池,其电解质溶液需用 ,阳极材料是用 ,阴极电极反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
按要求完成下列填空:
(1)已知在标准状况下的四种气体 ①8.96L CH4 ②3.01×1022个HCl分子 ③10.2克H2S ④0.5molNH3用相应的序号填写下列空白:体积最大的是 ④ ;含氢原子数最多的是 .
(2)等物质的量的氧气与臭氧质量之比为 2:3 ,分子个数之比为 1:1 ,电子个数之比为 .
(3)某金属氯化物MCl3 26.7g,含有0.600mol Cl﹣.则金属M的摩尔质量为 27g/mol .
(4)现有10克H218O中,中子数目为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ(5分)某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如右图所示。
(1)由图中所给数据进行分析,该反应的化学方程式为___________________________________;
(2)反应从开始至2分钟末,用Z的浓度变化表示的平均反应速率为v(Z)=__________________。
Ⅱ(7分)将2mol H2O和2mol CO置于1L容器中,加热至高温,发生如下可逆反应:
2H2O(g)  2H2(g)+O2(g),2CO(g)+O2(g)
2H2(g)+O2(g),2CO(g)+O2(g)  2CO2(g)。
2CO2(g)。
(3)当上述系统达到平衡时,欲求混合气体的平衡组成,至少还需要知道两种气体的平衡浓度,但这两种气体不能同时是________和________,或________和________(填分子式)。
(4)若平衡时O2和CO2的物质的量分别为a mol和b mol,则平衡时H2O的物质的量为_______________________ (用含a、b的代数式表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com