
【题目】如图是一种综合处理SO2废气的工艺流程.下列说法正确的是( )
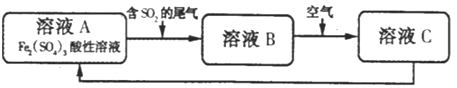
A.向B溶液中滴加KSCN溶液,溶液可能变为血红色
B.溶液B转化为溶液C发生的变化的离子方程式为4H+ + 2Fe2++O2=2Fe3++2H2O,
C.溶液酸性:A>B>C
D.加氧化亚铁可以使溶液C转化为溶液A
【答案】D
【解析】
试题分析:A.尾气中的二氧化硫气体,通入酸性硫酸铁溶液中发生2Fe3++2H2O+SO2=2Fe2+ +SO42-+4H+,B溶液中存在二价铁离子,二价铁离子与KSCN溶液不反应,溶液不会变为血红色,错误;B.溶液B中发生的反应是亚铁离子被氧气氧化为三价铁离子的反应:4Fe2++O2+4H+=4Fe3++2H2O,错误;C.反应过程中溶液的体积不变,溶液A为Fe2(SO4)3溶液中三价铁离子水解显酸性,溶液B为被二氧化硫还原生成的硫酸亚铁和二氧化硫被氧化生成的硫酸溶液,显酸性,溶液C为硫酸铁溶液和硫酸溶液,是发生反应4Fe2++O2+4H+=4Fe3++2H2O的结果,虽然消耗氢离子但溶液呈酸性,B>C>A,错误;D.溶液C为硫酸铁溶液和硫酸溶液,加氧化亚铁,氧化亚铁和硫酸反应生成硫酸亚铁、水,溶液C为硫酸铁溶液和硫酸亚铁溶液,被空气中的氧气氧化产生硫酸铁,正确。


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:
【题目】有一包白色固体粉末,已知除了含有 KNO3 以外,其中可能还含有 KCl、Ba(NO3)2、CuSO4、K2CO3、Na2SO4 中的一种或几种,现通过以下实验来确定该样品的组成:
①将部分粉末加入水中,振荡,有白色沉淀生成,过滤,溶液呈无色;
②向①的沉淀物中加入足量稀硝酸,固体完全溶解,并有气泡产生;
③取少量②的溶液,滴入稀硫酸,有白色沉淀产生;
④另取①中过滤后的溶液加入足量 AgNO3 溶液,产生白色沉淀; 根据上述实验事实,回答下列问题:
(1)原白色粉末中除 KNO3 以外一定还含有的物质是_________,一定不含有的物质 是_____,可能存在的物质是_____(填化学式);
(2)请写出第②步变化中所涉及的化学反应方程式:_____;
(3)A 同学为了确认该固体粉末中“可能存在的物质”是否存在, 他重新取了少量该样品于试管中加适量的蒸馏水溶解,请根据该同学设计的方案填空:
![]()
加入的试剂①_________试剂②_____(填化学式);当加入试剂②时,实验现 象为_____就可以确认该物质一定存在。
(4)B 同学为了进一步确定该样品的成份,他称取了 10.0 g 该固体,按如下方案进行实验: 说明:实验中产生的气体已经换算成标准状况下的体积。
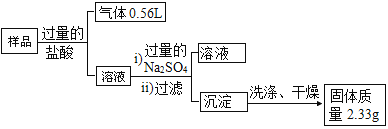
①请简述在实验室进行上述实验过程时如何洗涤沉淀_____。
②若按照 B 同学以上实验方案,还需对“溶液 2”中的溶质进一步分析,通过已有的实验数据分析,若该 样品中含 KNO3 的质量分数为_____时,可以确认样品中一定不含有“可能存在的物质”。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示是制取无水氯化铜的实验装置图,在A装置中将浓盐酸滴加到盛有二氧化锰粉末的圆底烧瓶中,烧瓶中发生反应的原理为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。
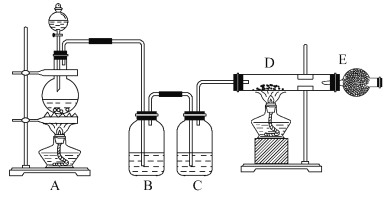
请回答下列问题:
(1)装置中盛放浓盐酸的仪器名称为_______。
(2)B瓶中试剂的作用是除去氯气中含有的氯化氢气体,C瓶中试剂的作用是______。
(3)玻璃管D中的反应方程式是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可用KMnO4和浓盐酸反应制取氯气。其变化可表述为:
2KMnO4+16HCl(浓) ===2KCl+2MnCl2+5Cl2↑+8H2O
(1)请将上述化学方程式改写为离子方程式________________。
(2)浓盐酸在反应中显示出来的性质是________________(填写编号,多选倒扣)。
①只有还原性 ②还原性和酸性
③只有氧化性 ④氧化性和酸性
(3)此反应中氧化产物是_________(填化学式),产生0.5 mol Cl2,则转移的电子的物质的量为______mol。
(4) 用双线桥法表示该反应的电子转移的方向和数目
_____
2KMnO4+16HCl(浓) ===2KCl+2MnCl2+5Cl2↑+8H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能存在Br-、CO![]() 、SO
、SO![]() 、Al3+、I-、Mg2+、Na+等7种离子中的某几种。现取该溶液进行实验,得到如下现象:
、Al3+、I-、Mg2+、Na+等7种离子中的某几种。现取该溶液进行实验,得到如下现象:
①向溶液中滴加足量氯水后,溶液变橙色,且有无色气泡冒出;
②向所得橙色溶液中加入足量BaCl2溶液,无沉淀生成;
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色。
已知:5Cl2+I2+6H2O===10HCl+2HIO3
据此可以判断:该溶液肯定不存在的离子组是
A. Al3+、Mg2+、SO![]() B. Mg2+、CO
B. Mg2+、CO![]() 、I-
、I-
C. Al3+、SO![]() 、I- D. Al3+、Br-、SO
、I- D. Al3+、Br-、SO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某二次电池放电时的化学方程式为:2K2S2+KI3=K2S4+3KI.与其它设备连接的电路如图示.当闭合开关K时,X附近溶液先变红.则下列说法正确的是( )

A. K+从右到左通过离子交换膜
B. A的电极反应式为:3I﹣﹣2e﹣=I3﹣
C. 当有0.1 mol K+通过离子交换膜,X电极上产生标准状况的气体1.12 L
D. 电池充电时,B电极要与外电源的正极相连,电极上发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KMnO4在实验室和工业上均有重要应用,其工业制备的部分工艺如下:
Ⅰ.将软锰矿(主要成分MnO2)粉碎后,与KOH固体混合,通入空气充分焙烧,生成暗绿色熔融态物质。
Ⅱ.冷却,将固体研细,用稀KOH溶液浸取,过滤,得暗绿色溶液。
Ⅲ.向暗绿色溶液中通入CO2,溶液变为紫红色,同时生成黑色固体。
Ⅳ.过滤,将紫红色溶液蒸发浓缩,冷却结晶,过滤,洗涤,干燥,得KMnO4固体。
资料:K2MnO4为暗绿色固体,在强碱性溶液中稳定,在近中性或酸性溶液中易发生歧化反应(Mn的化合价既升高又降低)。
(1)Ⅰ中,粉碎软锰矿的目的是___________________。
(2)Ⅰ中,生成K2MnO4的化学方程式是______________________________。
(3)Ⅱ中,浸取时用稀KOH溶液的原因是_________________。
(4)Ⅲ中,CO2和K2MnO4在溶液中反应的化学方程式是_____________________。
(5)将K2MnO4溶液采用惰性电极隔膜法电解,也可制得KMnO4,装置如图:

①b极是______极(填“阳”或“阴”),D是_______________。
②结合电极反应式简述生成KMnO4的原理:_______________________________。
③传统无膜法电解时,锰元素利用率偏低,与之相比,用阳离子交换膜可以提高锰元素的利用率,其原因是______。
(6)用滴定法测定某高锰酸钾产品的纯度,步骤如下:
已知:Na2C2O4+H2SO4=H2C2O4+Na2SO4,5H2C2O4+2MnO4-+6H+=2Mn2++10CO2↑+8H2O,摩尔质量:Na2C2O4134gmol-1、KMnO4158gmol-1。
ⅰ.称取ag产品,配成50mL溶液。
ⅱ.称取bgNa2C2O4,置于锥形瓶中,加蒸馏水使其溶解,再加入过量的硫酸。
ⅲ.将锥形瓶中溶液加热到75℃~80℃,恒温,用ⅰ中所配溶液滴定至终点,消耗溶液VmL(杂质不参与反应)。
滴定终点的现象为_______________,产品中KMnO4的质量分数的表达式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请回答下列问题
(1)向煮沸的蒸馏水中逐滴加入饱和FeCl3溶液,继续煮沸至溶液呈红褐色,停止加热,可制得Fe(OH)3胶体,制取Fe(OH)3胶体的离子方程式为_______________________。
(2)Ca(OH)2的电离方程式为_______________。
(3)现有下列物质:①干冰②NaHCO3晶体③氨水④纯醋酸⑤FeCl3溶液⑥铜⑦蔗糖⑧熔化的NaCl,其中属于非电解质的是___________(填序号,下同),属于强电解质的有____________,属于弱电解质的有________________,能导电的物质有________________。
(4)若有一表面光滑的塑料小球悬浮于Ba(OH)2溶液中央,如图所示。向该烧杯里缓缓注入与Ba(OH)2溶液等密度的稀H2SO4至恰好完全反应。在此实验过程中,此实验中观察到的现象有___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA代表阿伏加德罗常数的值,下列有关说法正确的是
A. 60g冰醋酸晶体中,含阴离子数目为NA
B. 标准状况下,22.4LCCl4中含有分子的数目为NA
C. 常温下,46gNO2与N2O4混合气体中含分子数为NA
D. 32gCu投入300mL10mol/L的浓硝酸中,充分反应后转移电子数为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com