
| A、一定温度和压强下,各种气体物质体积之比等于分子数之比 |
| B、一定温度和压强下,各种气体物质的密度之比等于摩尔质量之比 |
| C、一定体积和温度下,各种气体物质的物质的量之比等于压强之比 |
| D、气体摩尔体积是指1mol任何气体所占的体积约为22.4L |
| N |
| NA |
| M |
| Vm |
| N |
| NA |
| M |
| Vm |


科目:高中化学 来源: 题型:
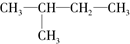 的叙述正确的是( )
的叙述正确的是( )| A、均能用CnH2n+2组成来表示 |
| B、与所有烷烃互为同素异形体 |
| C、因为它们结构相似,所以它们的化学性质相似,但物理性质不相同 |
| D、通常状况下它们都是气态烷烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1L 该溶液中含硝酸钾 202g |
| B、100mL 该溶液中含硝酸钾0.02mol |
| C、从 1L该溶液中取出500 mL 后,剩余溶液的浓度为0.1mol/L |
| D、1L水中溶解0.2mol硝酸钾,即可配得 0.2mol/L硝酸钾溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、180g |
| B、360 g |
| C、363.6g |
| D、365g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、阿伏加德罗常数 |
| B、摩尔质量 |
| C、一定质量气体的体积 |
| D、O2的相对分子质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,22.4LCO2中含有NA个CO2分子 |
| B、室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA |
| C、标准状况下,11.2L氦气中约含有NA个氦原子 |
| D、1L0.1mol?L-1Na2SO3溶液中含有0.1NA个SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳、硅都是较活泼的非金属,它们只能以化合态存在于自然界中 |
| B、等质量的Na2CO3、NaHCO3分别与足量盐酸反应,前者产生的CO2多 |
| C、一定条件下CO2、SiO2都能与NaOH、Na2CO3(或CaCO3)发生反应 |
| D、热稳定性:CH4<SiH4;酸性H2CO3>H2SiO3(H4SiO4) |
查看答案和解析>>
科目:高中化学 来源: 题型:

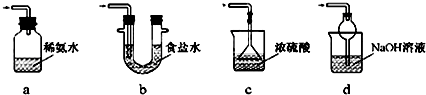
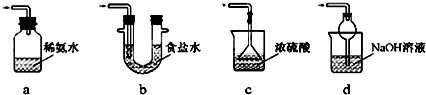
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com