
【题目】铁及其化合物在生产生活及科研中应用广泛。
(1)聚合硫酸铁的化学式为[![]() ]m,是常用的水处理剂。基态铁原子的核外电子排布式为___________,聚合硫酸铁中铁元素阳离子有_________个未成对电子。
]m,是常用的水处理剂。基态铁原子的核外电子排布式为___________,聚合硫酸铁中铁元素阳离子有_________个未成对电子。
(2)Fe3+、Co3+与N3-、CN-等可形成络合离子。
①K3[Fe(CN)6]可用于检验Fe2+,配体CN-中碳原子杂化轨道类型为_______,1mol [Fe(CN)6]3-离子中含有σ键的数目为__________。
②已知N3-与CS2为等电子体,则N3-的空间构型为_________。
(3)氟化亚铁晶胞属于四方晶系,其长方体结构如图所示,根据图中所示数据计算该晶体密度ρ=_________g·cm-3。(列出计算式即可)(1pm=10-12m)

【答案】 1s22s22p63s23p63d64s2或[Ar] 3d64s2 5 sp 12NA 直线型 ![]()
【解析】(1)铁原子的电子排布式为1s22s22p63s23p63d64s2或[Ar] 3d64s2;根据聚合硫酸铁的化学式知,聚合硫酸铁中铁元素的化合价为+3价,聚合硫酸铁中铁元素阳离子有5个未成对电子;(2)①CN-中C原子价层电子对个数=1+![]() (4+1-1×3)=2,所以采取sp杂化;中含有6
(4+1-1×3)=2,所以采取sp杂化;中含有6![]() 个σ键,1mol [Fe(CN)6]3-离子中含有σ键的数目为12NA;②N3-与CO2是等电子体,具有相同的价电子数,它们具有相似的化学结构,二氧化碳是直线型分子,所以N3-的空间构型是直线型; (4)由题图知,该晶胞中黑球个数为8×
个σ键,1mol [Fe(CN)6]3-离子中含有σ键的数目为12NA;②N3-与CO2是等电子体,具有相同的价电子数,它们具有相似的化学结构,二氧化碳是直线型分子,所以N3-的空间构型是直线型; (4)由题图知,该晶胞中黑球个数为8×![]() +1=2,白球个数为4×
+1=2,白球个数为4×![]() +2=4,则黑球代表Fe原子,白球代表F原子,故该晶体的密度ρ=
+2=4,则黑球代表Fe原子,白球代表F原子,故该晶体的密度ρ= =
=![]() g·cm-3。
g·cm-3。


科目:高中化学 来源: 题型:
【题目】下列有关气体体积的叙述中,正确的是
A. 一定温度和一定压强下,各种气态物质体积的大小由构成气体的分子间距离决定
B. 一定温度和一定压强下,各种气态物质体积的大小由构成气体的分子数决定
C. 不同的气体,若体积不同,则它们所含的分子数也不同
D. 气体摩尔体积是指1mol任何气体所占的体积约为22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列说法不正确的是( )
A.乙醇溶液的浓度越大,对新冠病毒杀灭效果越好
B.氨气易液化,可用来作制冷剂
C.常温下,铝制容器可以用来贮运浓硝酸
D.乙烯可用作水果的催熟剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A.Na2O2能与水反应,所以Na2O2可以作气体的干燥剂
B.钠可以从AgNO3溶液中置换出金属银
C.钠能与水反应,所以钠着火不能用水灭火,要用泡沫灭火器
D.Na2O、Na2O2、NaOH和NaHCO3均是强电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中,R、W、X、Y、Z为元素周期表中前四周期的部分元素,下列有关叙述正确的是

A. 五种元素中,只有Z为金属元素
B. W位于ⅥA族,有+6、-2两种常见化合价
C. X和Y的最高价氧化物对应水化物都是强酸
D. X、Y、Z的气态氢化物的稳定性:Y>X>Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸镧咀嚼片是一种不含钙和铝的磷酸盐结合剂,用于慢性肾衰患者高磷血症的治疗。碳酸镧可由 LaCl3 为原料来制备,整个反应在较低的pH条件下进行,避免生成碱式碳酸镧[La(OH)CO3]。
(1)化学兴趣小组利用下列装置在实验室中用碳酸氢铵制备碳酸镧。

①仪器 X 的名称为________;检验装置甲气密性良好的方法是___________。
②实验中 K1、 K2 打开的先后顺序为________;为保证碳酸镧的纯度,实验过程中需要注意的问题有____________。
(2)碳酸钠或碳酸氢钠与氯化镧反应均可生成碳酸镧。
①为了高磷血症患者的安全,通常选用碳酸氢钠溶液,过程中会发生两个平行反应,其离子方程式为_______和____________。
②选择碳酸氢钠溶液制备碳酸镧的优点是___________(任写一条)。
③T℃时,碳酸镧的溶解度为1.0×10-7 mol·L-1, HCO3-的电离平衡常数为 6.0×10-11。请计算反应 2LaCl3+3NaHCO3![]() La2(CO3)3↓+3NaCl+3HCl 的平衡常数 K=_________。
La2(CO3)3↓+3NaCl+3HCl 的平衡常数 K=_________。
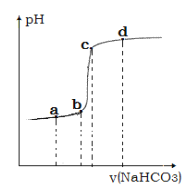
④利用手持技术测定溶液的 pH 从而监控反应过程,得到如图曲线。请说明 bc 段变化的原因__________。
(3)碳酸镧(式量为 458)质量分数的测定:准确称取15.0g产品试样,溶于10.0mL 稀盐酸中,加入 10mLNH3-NH4Cl 缓冲溶液,加入 0.2g 紫脲酸铵混合指示剂,用 0.5 mol·L-1EDTA(Na2H2Y)标准溶液滴定至呈蓝紫色(La3++H2Y2-= LaY-+2H+),消耗 EDTA 溶液 60.00mL。则产品中碳酸镧的质量分数 w=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】具有以下结构的原子,一定属于主族元素的是( )
A.最外层有1个电子的原子
B.最外层电子排布为ns2的原子
C.最外层有3个未成对电子的原子
D.次外层无未成对电子的原子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com