
【题目】研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,同温度下涉及如下反应:
a、2NO(g)+Cl2(g)2ClNO(g)△H1<0 其平衡常数为K1
b、2NO2(g)+NaCl(s)NaNO3(s)+ClNO(g)△H2<0 其平衡常数为K2
(1)4NO2(g)+2NaCl(s)2NaNO3(s)+2NO(g)+Cl2(g)△H3的平衡常数K=(用K1、K2表示).△H3=(用△H1、△H2表示).
(2)为研究不同条件对反应a的影响,在恒温条件下,向2L恒容密闭容器中加入0.2mol NO和0.1mol Cl2 , 10min时反应a达到平衡.测得10min内V(ClNO)=7.5×10﹣3molL﹣1min﹣1 , 则平衡后n(Cl2)=mol,NO的转化率α1= . 其它条件保持不变,反应(1)在恒压条件下进行,平衡时NO的转化率为α2 , α1α2(填“>”“<”或“=”),平衡常数K1(填“增大”“减小”或“不变”).若要使K1减小,可采用的措施是 .
【答案】
(1)![]() ;2△H2﹣△H1
;2△H2﹣△H1
(2)0.025;75%;<;不变;升高温度
【解析】解:(1)已知:a、2NO2(g)+NaCl(s)NaNO3(s)+ClNO(g)
b、4NO2(g)+2NaCl(s)2NaNO3(s)+2NO(g)+Cl2(g)
根据盖斯定律,a×2﹣b可得:2NO(g)+Cl2(g)2ClNO(g),该反应△=2△H1﹣△H2 , 平衡常数K3= ![]() ,
,
所以答案是: ![]() ;2△H1﹣△H2;(2)测得10min内v(ClNO)=7.5×10﹣3molL﹣1min﹣1 , 则△n(ClNO)=7.5×10﹣3molL﹣1min﹣1×10min×2L=0.15mol,
;2△H1﹣△H2;(2)测得10min内v(ClNO)=7.5×10﹣3molL﹣1min﹣1 , 则△n(ClNO)=7.5×10﹣3molL﹣1min﹣1×10min×2L=0.15mol,
由方程式可知,参加反应氯气的物质的量为0.15mol× ![]() =0.075mol,故平衡时氯气的物质的量为0.1mol﹣0.075mol=0.025mol;
=0.075mol,故平衡时氯气的物质的量为0.1mol﹣0.075mol=0.025mol;
参加反应NO物质的量为0.15mol,则NO的转化率为 ![]() ×100%=75%;
×100%=75%;
正反应为气体物质的量减小的反应,恒温恒容下条件下,到达平衡时压强比起始压强小,其他条件保持不变,a在恒压条件下进行,等效为在恒温恒容下的平衡基础上增大压强,平衡正向移动,NO转化率增大,故转化率α1<α2;
平衡常数只受温度影响,温度不变,平衡常数不变,正反应为放热反应,升高温度平衡逆向移动,平衡常数减小,
所以答案是:0.025;75%;<;不变;升高温度.
【考点精析】根据题目的已知条件,利用反应热和焓变和化学平衡的计算的相关知识可以得到问题的答案,需要掌握在化学反应中放出或吸收的热量,通常叫反应热;反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%.


 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案科目:高中化学 来源: 题型:
【题目】已知金属活动相差越大,形成原电池时越容易放电.请根据如图装置,回答下列问题: 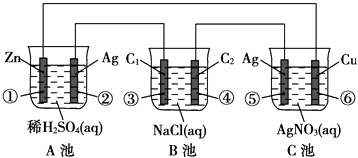
(1)各装置名称是:A池 , B池 .
(2)写出电极上发生的反应:① , ③ , ⑤ .
(3)当电路上有2mol电子流过时,①极上质量变化g,⑥极上质量变化g.
(4)反应进行一段时间后,A,B,C三池中电解质溶液浓度不变的是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于可逆反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g),下列叙述中正确的是
4NO(g)+6H2O(g),下列叙述中正确的是
A.达到化学平衡状态时,4v正(O2)= 5v逆(NO)
B.若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到化学平衡状态
C.达到化学平衡状态后,若增大容器容积,则正反应速率减小,逆反应速率增大
D.化学反应速率的关系为2v正(NH3)= 3v正(H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子,在所给的条件下,一定能够大量共存的是( )
A.在滴加酸碱指示剂酚酞试液后呈现红色的溶液中:Na+、Cl﹣、AlO2﹣、CO32﹣
B.在由水电离出的c(H+)=1×10﹣12mol/L的溶液中:HCO3﹣、Al3+、NH4+、ClO﹣
C.在 ![]() =1×1012的溶液中:Fe2+、Mg2+、CO32﹣、NO3﹣
=1×1012的溶液中:Fe2+、Mg2+、CO32﹣、NO3﹣
D.在AlCl3溶液中:K+、NO3﹣、S2﹣、Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将2 mol H2O和2 mol CO置于1 L容器中,在一定条件下,加热至高温,发生如下可逆反应: 2H2O(g)![]()
2H2+O2,2CO+O2![]() 2CO2。
2CO2。
(1)当上述系统达到平衡时,欲求其混合气体的平衡组成,则至少还需要知道两种气体的平衡浓度,但这两种气体不能同时是________和________,或________和________。(填它们的分子式)
(2)若平衡时O2和CO2的物质的量分别为:n平(O2)= a mol, n平(CO2)=bmol。试求n平(H2O)=________。(用含a、b的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在 A+2B3C+4D 反应中,表示该反应速率最快的是( )
A.v(A)=0.3 mol/(Ls)
B.v(B)=0.5 mol/(Ls)
C.v(C)=0.8 mol/(Ls)
D.v(D)=1 mol/(Lmin)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铬化学丰富多彩,由于铬光泽度好,常将铬镀在其他金属表面,同铁、镍组成各 种性能的不锈钢,CrO3大量地用于电镀工业中. 
(1)在如图装置中,观察到图 1 装置铜电极上产生大量的无色气泡,而图 2 装置中铜电 极上无气体产生,铬电极上产生大量有色气体.
图 2 装置中铬电极的电极反应式
(2)最近赣州酒驾检查特别严,利用 CrO3 具有强氧化性,有机物(如酒精)遇到 CrO3 时,猛烈反应,CrO3 被还原成绿色的硫酸铬[Cr2(SO4)3],另该过程中乙醇被氧化成乙酸,从而增强导电性,根据电流大小可自动换算出酒精含量.写出该反应的化学方程式为 .
(3)虽然铬加到铁中可将铁做成不锈钢可减少金属腐蚀,但 生产成本高,生活中很多情况下还是直接使用钢铁,但易腐蚀,利用右图装置 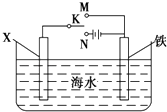 ,可以模拟铁的电化学防护.若 X 为碳棒,为减缓铁的腐蚀,开关 K 应置于处.若 X 为锌,开关K 置于处.
,可以模拟铁的电化学防护.若 X 为碳棒,为减缓铁的腐蚀,开关 K 应置于处.若 X 为锌,开关K 置于处.
(4)CrO3 和 K2Cr2O7 均易溶于水,这是工业上造成铬污染的主要原因.净化处理方法之一是将含+6 价 Cr 的废水放入电解槽内,用铁作阳极,加入适量的 NaCl 进行电解:阳极区生成的 Fe2+和 Cr2O72﹣发生反应,生成的 Fe3+和 Cr3+在阴极 区与OH﹣结合生成 Fe(OH)3和 Cr(OH)3 沉淀除去,已知某条件下的KspFe(OH)3=3.0×10﹣31 , KspCr(OH)3=6.0×10﹣38 . 已知电解后的溶液中 c(Fe3+)为 2.0×10﹣6 molL1 , 则溶液中 c(Cr3+)=molL﹣1 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于蒸馏操作的说法不正确的是
A. 烧瓶内放碎瓷片的目的是防止暴沸
B. 烧瓶不能直接加热,应垫上石棉网
C. 实验时发现烧瓶中没有放碎瓷片,应停止加热,马上加入
D. 在点燃酒精灯加热前,应先通冷却水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com