
【题目】某溶液中可能含有下列6种离子中的某几种:![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 。为确认溶液组成进行如下实验:
。为确认溶液组成进行如下实验:
(1)![]() 上述溶液,加入足量
上述溶液,加入足量![]() 溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀
溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀![]() ,向沉淀中加入过量的盐酸,有
,向沉淀中加入过量的盐酸,有![]() 沉淀不溶。
沉淀不溶。
(2)向(1)的滤液中加入足量的![]() 溶液,加热,产生能使湿润红色石蕊试纸变蓝的气体
溶液,加热,产生能使湿润红色石蕊试纸变蓝的气体![]() (已换算成标准状况,假定产生的气体全部逸出)。由此可以得出关于原溶液组成的正确结论是( )
(已换算成标准状况,假定产生的气体全部逸出)。由此可以得出关于原溶液组成的正确结论是( )
A.![]()
B.如果上述6种离子都存在,则![]()
C.一定存在![]() 、
、![]() 、
、![]() ,可能存在
,可能存在![]() 、
、![]() 、
、![]()
D.一定存在![]() 、
、![]() 、
、![]() 、
、![]() ,一定不存在
,一定不存在![]() 、
、![]()
【答案】B
【解析】
⑴![]() 上述溶液,加入足量
上述溶液,加入足量![]() 溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀
溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀![]() ,向沉淀中加入过量的盐酸,有
,向沉淀中加入过量的盐酸,有![]() 沉淀不溶,说明2.33g为硫酸钡,物质的量为0.01mol,说明原溶液中含有
沉淀不溶,说明2.33g为硫酸钡,物质的量为0.01mol,说明原溶液中含有![]() ,沉淀还有碳酸钡沉淀4.30g2.33g = 1.97g即物质的量为0.01mol,原溶液含有
,沉淀还有碳酸钡沉淀4.30g2.33g = 1.97g即物质的量为0.01mol,原溶液含有![]() 。
。
⑵向(1)的滤液中加入足量的![]() 溶液,加热,产生能使湿润红色石蕊试纸变蓝的气体
溶液,加热,产生能使湿润红色石蕊试纸变蓝的气体![]() 即物质的量为0.5mol氨气,说明原溶液中含有0.05mol
即物质的量为0.5mol氨气,说明原溶液中含有0.05mol![]() ,根据电荷守恒,肯定还含有
,根据电荷守恒,肯定还含有![]() ,而可能含有
,而可能含有![]() 、
、![]() 。
。
A. ![]() ,虽然
,虽然![]() 要水解,但浓度大,
要水解,但浓度大,![]() ,故A错误;
,故A错误;
B. 根据电荷守恒,n(Cl-)=0.01mol,如果上述6种离子都存在,n(Cl-)>0.01mol,因此![]() ,故B正确;
,故B正确;
C. 根据分析得出一定存在![]() 、
、![]() 、
、![]() 、
、![]() ,可能存在
,可能存在![]() 、
、![]() ,故C错误;
,故C错误;
D. 根据C可以得出D错误,故D错误。
综上所述,答案为B。


科目:高中化学 来源: 题型:
【题目】亚硝酰氯(NOCl)是有机物合成中的重要试剂,为红褐色液体或黄色气体,具有刺鼻恶臭味,遇水反应生成一种烈化物和两种氧化物。某学习小组在实验用C12和NO制备NOCl并测定其纯度,相关实验(装置略去)如下。请回答:
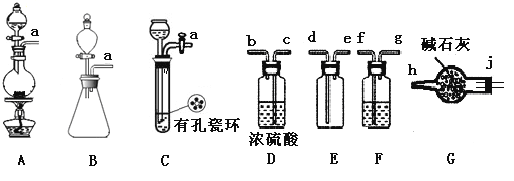
(1)制备Cl2发生装置可______ (填大写字母),反应的离子方程式为_______。
(2)欲收集一瓶干燥的氯气,选择装置,其连接顺序为:a→________(按气流方向,用小写字母表示),若用到F,其盛装药品为_________。
(3)实验室可用下图装置制备亚硝酰氯(NOCl)
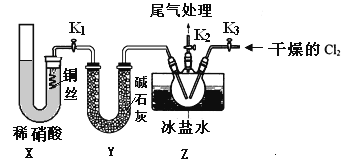
①实验室也可用B装置制备NO,上图X装置的优点为__________(至少写出两点)
②检验装置气密性并装入药品,打开k2,然后再打开____(填“k1”或“k3”),通入一段时间气体,其目的为________,然后进行其他操作,当Z有一定量液体生成时,停止实验。
③若无装肖Y,则Z中NOCl可能发生反应的化学方程式为_________
(4)取Z中所得液体mg溶于水,配制成250mL溶液,取出25.00mL,以K2CrO4溶液为指示剂,用cmol/LAgNO3标准溶液滴定至终点,消耗标准溶液的体积为22.50mL.已知:Ag2CrO4为砖红色固体;Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=1×10-12,则亚硝酰氯(NOC1)的质量分数为____(用代数式表示,不必化简)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,下列反应中水蒸气含量随反应时间的变化趋势符合题图10 的是
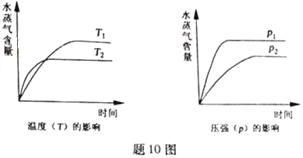
A. CO2(g)+2NH3(g)![]() CO(NH2)2(s)+H2O(g);△H<0
CO(NH2)2(s)+H2O(g);△H<0
B. CO2(g)+H2(g)![]() CO(g)+H2O(g);△H>0
CO(g)+H2O(g);△H>0
C. CH3CH2OH (g)![]() CH2=CH2(g)+H2O(g);△H>0
CH2=CH2(g)+H2O(g);△H>0
D. 2C6H5CH2CH3(g)+O2(g)![]() 2 C6H5CH=CH2(g)+2H2O(g);△H<0
2 C6H5CH=CH2(g)+2H2O(g);△H<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,充分燃烧一定量的丁烷放出热量161.9kJ,经测定完全吸收生成的CO2需消耗5mol/L的KOH溶液100ml,恰好生成正盐,则此条件下热化学方程式:C4H10(g)+![]() O2(g)→4CO2(g)+5H2O(g)的△H为( )
O2(g)→4CO2(g)+5H2O(g)的△H为( )
A. +2590.4kJ/mol B. ﹣2590.4kJ/mol C. +1295.2kJ/mol D. ﹣1295.2kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,属于消去反应的是
A.CH2=CH2+HCl 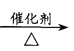 CH3CH2Cl
CH3CH2Cl
B.CH4+Cl2![]() CH3Cl+HCl
CH3Cl+HCl
C.![]() +Br2
+Br2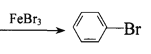 +HBr
+HBr
D.CH3CH2Br+NaOH![]() CH2=CH2+NaBr+H2O
CH2=CH2+NaBr+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室利用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁(碱式硫酸铁的聚合物)和绿矾(FeSO4·7H2O),过程如下:
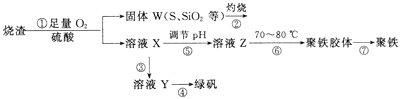
(1)将过程②中产生的气体通入下列溶液中,溶液不会褪色的是_____(填标号)。
A.品红溶液 B.紫色石蕊溶液 C.酸性KMnO4溶液 D.溴水
(2)过程①中,FeS和O2、H2SO4反应的离子方程式为_________。
(3)过程③中,需加入的物质是__________。
(4)实验室为测量所得到的聚铁样品中铁元素的质量分数,进行下列实验。①用分析天平称取2. 800 g样品;②将样品溶于足量的盐酸后,加入过量的氯化钡溶液;③过滤、洗涤、干燥,称量,得固体质量为3. 495 g。若该聚铁主要成分为[Fe(OH) (SO4)]n,则该聚铁样品中铁元素的质量分数为____________(假设杂质中不含铁元素和硫元素)。
(5)如图是将过程②产生的气体SO2转化为重要的化工原料H2SO4的原理示意图,若得到的硫酸浓度仍为49%,则理论上参加反应的SO2与加入的H2O的质量比为______。
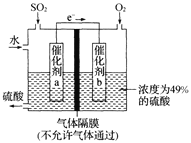
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z四种短周期元素的原子序数依次增大,W的某种原子无中子,X、Y可形成原子个数比为1∶1的具有漂白性的物质,工业上常用电解饱和YZ溶液来获得Z的单质及其他产品。下列说法正确的是
A. W和X、Y、Z均能形成18电子的分子
B. 上述四种元素的原子半径大小顺序为r(Z)>r(Y)>r(X)>r(W)
C. X、Y之间形成的化合物可能同时含有离子键和非极性共价健
D. W、X、Z三种元素形成的化合物一定是弱酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验或操作的叙述正确的是
A.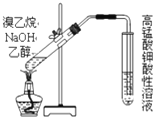 检验溴乙烷与NaOH水溶液共热产生的乙烯
检验溴乙烷与NaOH水溶液共热产生的乙烯
B.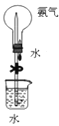 做喷泉实验时先挤压胶头滴管,后松开止水夹
做喷泉实验时先挤压胶头滴管,后松开止水夹
C.酸碱中和滴定前,滴定管和锥形瓶在用蒸馏水洗涤后均需用待装溶液润洗
D.用托盘天平称取1.06g无水碳酸钠,溶于250mL水,配制0.04molL-1 Na2CO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲胺(CH3NH2)是一种应用广泛的一元弱碱,其电离方程式为:CH3NH2+H2O![]() CH3NH3++OH-常温下,向20.0mL0.10mol/L的甲胺溶液中滴加VmL0.10mol/L的稀盐酸,混合溶液的pH与相关微粒浓度的关系如图所示。下列说法中错误的是( )
CH3NH3++OH-常温下,向20.0mL0.10mol/L的甲胺溶液中滴加VmL0.10mol/L的稀盐酸,混合溶液的pH与相关微粒浓度的关系如图所示。下列说法中错误的是( )

A. b点对应加入盐酸的体积V<20.00mL
B. 常温下,甲胺的电离常数为Kb,则Kb=10-3.4
C. b点可能存在关系:c(Cl-)>c(CH3NH3+)>c(H+)>cOH-)
D. V=20.00mL时,溶液中水电离的c(H+)>10-7mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com