
【题目】我国化学家侯德榜创立了著名的“侯氏制碱法”(流程简图如图所示),促进了世界制碱技术的发展.下列有关说法正确的是( )
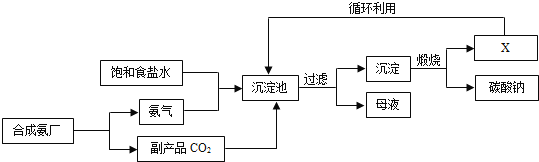
A.沉淀池中的反应物共含有五种元素
B.过滤得到的“母液”中一定只含有两种溶质
C.图中X可能是氨气
D.通入氨气的作用是使溶液呈碱性,促进二氧化碳的吸收,更多地析出沉淀
科目:高中化学 来源: 题型:
【题目】根据以下反应:
KMnO4+ Na2SO3+ H2SO4= MnSO4+ Na2SO4+ K2SO4+ H2O
回答下列问题:
I.请配平该反应方程式___,该反应还原剂是___,还原产物是___。
II.当反应转移1mol电子时,被氧化的物质的质量为___g。
Ⅲ.用单线桥法标出反应中电子转移的方向和数目___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如图的转化关系判断下列说法正确的是
反应②:2Cl2+2Ca(OH)2==CaCl2+Ca(ClO)2+2H2O;⑤为置换反应(反应条件已略去,漂白粉主要成分为Ca(ClO)2;)。

A.反应①②③④⑤均可写出离子方程式
B.相同条件下生成等量的O2,反应③和④转移的电子数之比为1: 1
C.反应①中氧化剂与还原剂的物质的量之比为1: 4
D.反应⑤说明该条件下铝的还原性强于锰
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组设计实验探究CuSO4分解产物
Ⅰ.甲同学选择下列装置设计实验探究硫酸铜分解的气态产物SO3、SO2和O2,并验证SO2的还原性。
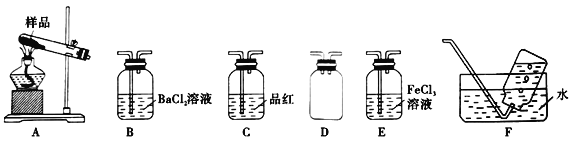
回答下列有关问题:
(1)上述装置按气流从左至右排序为A、D、___E、F(填代号)。
(2)装置D的作用是____;能证明有SO3生成的实验现象是____。
(3)在实验过程中C装置中红色溶液逐渐变为无色溶液,说明A中分解产物有:___;待C中有明显现象后,F开始收集气体,F装置中集气瓶收集到了少量气体,该气体是___(填化学式)。
(4)为了验证SO2的还原性,取E装置中反应后的溶液于试管中,设计如下实验:
a.滴加少量的NH4SCN溶液 b.滴加少量的K3[Fe(CN)6]溶液
c.滴加酸性KMnO4溶液 d.滴加盐酸酸化的BaCl2溶液
其中,方案合理的有____(填代号),写出E装置中可能发生反应的离子方程式:___。
Ⅱ.乙同学利用A中残留固体验证固体产物(假设硫酸铜已完全分解)查阅资料知,铜有+2、+1价,且分解产物中不含0价的铜。Cu2O在酸性条件下不稳定,发生反应:Cu2O+2H+ =Cu+Cu2++H2O。
(5)为了验证固体产物中是否有Cu2O,设计了下列4种方案,其中能达到实验目的的是____。
甲:取少量残留固体于试管,滴加足量的稀硝酸,观察溶液颜色是否变为蓝色
乙:取少量残留固体于试管,滴加足量的稀硫酸,观察溶液颜色是否变为蓝色
丙:取少量残留固体于试管,滴加足量的稀盐酸,观察是否有红色固体生成
丁:取少量残留固体于试管,通入氢气,加热,观察是否生成红色固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国传统文化中包括许多科技知识。下列古语中不涉及化学变化的是
千淘万漉虽辛苦,吹尽狂沙始到金 |
熬胆矾(CuSO4·5H2O) 铁釜,久之亦化为铜 |
凡石灰(CaCO3), 经火焚炼为用 |
丹砂(HgS)烧之成水银,积变又成丹砂 |
A | B | C | D |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以废旧锌锰电池初步处理分选出的含锰废料(MnO2、MnOOH、MnO及少量Fe、Pb等)为原料制备高纯MnCl2·xH2O,实现锰的再生利用。其工作流程如下:
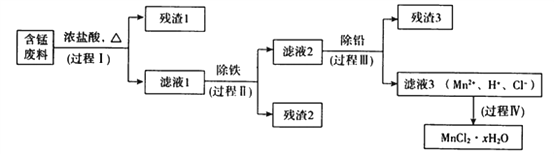
资料a.Mn的金属活动性强于Fe;Mn2+在酸性条件下比较稳定,pH高于5.5时易被O2氧化。
资料b.生成氢氧化物沉淀的pH
Mn(OH)2 | Pb(OH)2 | Fe(OH)3 | |
开始沉淀时 | 8.1 | 6.5 | 1.9 |
完全沉淀时 | 10.1 | 8.5 | 3.2 |
注:金属离子的起始浓度为0.1 mol·L-1
(1)过程Ⅰ的目的是浸出锰。经检验滤液1中含有的阳离子为Mn2+、Fe3+、Pb2+和H+。
①MnOOH与浓盐酸反应的离子方程式是_______________________________。
②检验滤液1中只含Fe3+不含Fe2+的操作和现象是:_________________________________________。
③Fe3+由Fe2+转化而成,可能发生的反应有:
a.2Fe2++Cl2=2Fe3+2Cl-
b.4Fe2++O2+4H+=2Fe3++2H2O
c.……
写出c的离子方程式:____________________。
(2)过程Ⅱ的目的是除铁。有如下两种方法,
ⅰ.氨水法:将滤液1先稀释,再加适量10%的氨水,过滤。
ⅱ.焙烧法:将滤液1浓缩得到的固体于290℃焙烧,冷却,取焙烧物,加水溶解,过滤,再加盐酸酸化至pH小于5.5。
已知:焙烧中发生的主要反应为2FeCl3+3O2=2Fe2O3+3Cl2,MnCl2和PbCl2不发生变化。
①氨水法除铁时,溶液pH应控制在_____________之间。
②两种方法比较,氨水法除铁的缺点是____________。
(3)过程Ⅲ的目的是除铅。加入的试剂是____________。
(4)过程Ⅳ所得固体中的x的测定如下,取m1g样品,置于氯化氢氛围中加热至失去全部结晶水时,质量变为m2g。则x=____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】填空:
(1)同温同压下,同体积的甲烷和二氧化碳物质的量之比为____,质量比为____;
(2)在标准状况下,4 g H2,11.2 L O2,1 mol H2O中,所含分子数最多的是______,体积最小的是________;
(3)硫酸钾和硫酸铝的混合溶液中,已知其中Al3+的浓度为0.4 mol/L,SO42-的浓度为0.7 mol/L,则K+的浓度为________mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】300mLAl2(SO4)3溶液中,含有Al3+为1.62 克,在该溶液中加入0.1mol/LBa(OH)2溶夜300ml,反应后溶液中SO42-的物质的量浓度约为
A. 0.4 mol/L B. 0.3 mol/L C. 0.1 mol/L D. 0.2mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是工业利用菱镁矿(主要含MgCO3,还含有Al2O3、FeCO3杂质)制取氯化镁的工艺流程。
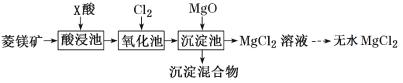
下列说法不正确的是
A.酸浸池中加入的X酸是硝酸
B.氧化池中通入氯气的目的是将Fe2+氧化为Fe3+
C.生成的沉淀物为Fe(OH)3和Al(OH)3
D.在工业上常利用电解熔融氯化镁的方法制取金属镁
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com