
【题目】氮气可以作食品包装、灯泡等的填充气,也是合成纤维、合成橡胶的重要原料。实验室制备氮气的反应式:NH4Cl+NaNO2![]() NaCl+N2↑+2H2O。下列说法正确的是( )
NaCl+N2↑+2H2O。下列说法正确的是( )
A.元素的电负性:N>O>H
B.氮气分子的电子式:![]()
C.钠电离最外层一个电子所需要的能量:①>② ![]()
D.水中的氢键可以表示为:O—H…O,其中H…O之间的距离即为该氢键的键长
科目:高中化学 来源: 题型:
【题目】如图所示,纵轴表示导电能力,横轴表示所加溶液的量,下列说法正确的是( )
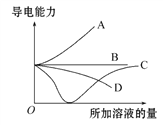
A. 曲线A表示NaOH溶液中滴加稀盐酸
B. 曲线B表示CH3COOH溶液中滴加KOH溶液
C. 曲线C表示Ba(OH)2溶液中滴加稀硫酸
D. 曲线D表示Cu(OH)2悬浊液中滴加HNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有以下物质:①NaCl固体;②液态CO2;③液态氯化氢;④汞;⑤固体BaSO4;⑥蔗糖;⑦酒精;⑧熔融的Na2CO3,请回答下列问题:
(1)以上物质中能导电的是________;
(2)以上物质属于电解质的是________;
(3)以上物质属于非电解质的是_______;
(4)以上物质溶于水后形成的溶液能导电的是______;
(5)属于盐的有________;
(6)写出⑧溶于水中的电离方程式_____;
(7)分离胶体和溶液常用的方法叫__________;
(8)等质量的O2和O3所含原子个数比为______;
(9)设NA为阿伏加德罗常数的数值,若ag某气体中含有的分子数为b,则c g该气体在标准状况下的体积是___________。(用含有NA的式子表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2 L密闭容器内,800 ℃时反应:2NO(g)+O2(g)![]() 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.011 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)写出该反应的平衡常数表达式:K= 。
(2)如图中表示NO2的变化的曲线是 。用O2表示从0~2s内该反应的平均速率v=

(3)能说明该反应已达到平衡状态的是 。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆 (NO)=2v正 (O2) d.容器内密度保持不变
(4)某同学查阅资料得知,该反应![]() >
>![]() ;25 ℃时,生成1 mol NO2,热量变化为56.4 kJ。但是该同学由于疏忽,忘记注明“+”、“-”。根据题目信息,该反应的热化学方程式为 。
;25 ℃时,生成1 mol NO2,热量变化为56.4 kJ。但是该同学由于疏忽,忘记注明“+”、“-”。根据题目信息,该反应的热化学方程式为 。
(5)为使该反应的反应速率增大,且平衡向正反应方向移动的是 。
a.及时分离除NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g),下列叙述正确的是( )
4NO(g)+6H2O(g),下列叙述正确的是( )
A. 若单位时间内生成xmolNO的同时消耗xmolNH3,则反应达到平衡状态
B. 化学反应速率关系是:2v正(NH3)=3v正(H2O)
C. 达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大
D. 达到化学平衡时,4v正(O2)=5v逆(NO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了提纯氯化钠固体(混有硫酸钠、碳酸铵杂质),设计了如下实验方案,请回答:
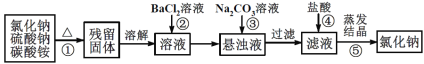
(1)操作①在加热时盛装混合物的仪器可选择__________。
(2)操作②若改为加硝酸钡溶液,对本实验的影响是__________。
(3)进行操作②后,判断SO42-已除尽的方法是__________。
(4)操作③的目的是_____________。
(5)操作⑤蒸发结晶的具体操作为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二硫代磷酸锌( ![]() )是一种表面活性剂,能够提高橡胶的抓着力、耐磨性。请回答下列问题:
)是一种表面活性剂,能够提高橡胶的抓着力、耐磨性。请回答下列问题:
(1)二硫代磷酸锌结构中,P的杂化方式为__________________,C1、P、S的第一电离能由大到小的顺序为_____________________。
(2)Zn2+的价层电子排布式为________________,锌能够跟强碱溶液反应生成[Zn(OH)4]2-,不考虑空间构型,[Zn(OH)4]2-的结构可用示意图表示为__________________。
(3)硫元素能形成多种含氧酸,两分子硫酸脱去一分子水生成焦硫酸(H2S2O7),则1mol焦硫酸中含有硫氧键的数目为____________;用价层电子互斥理论判断并解释SO32-与SO42-键角的相对大小。
(4)纤锌矿的六方晶体结构如图所示,该晶胞的化学式为___________,其晶胞参数分别为a pm和b pm,则该晶体的密度为____________________g·cm-3(用含a、b、NA的代数式表示)。
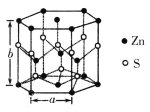
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浓度均为0.1 mol/L、体积均为V0的HX、HY溶液,分别加水稀释至体积V,pH随![]() 的变化关系如图所示。下列叙述正确的是
的变化关系如图所示。下列叙述正确的是

A.HX、HY都是弱酸,且HX的酸性比HY的弱
B.常温下,由水电离出的c(H+)·c(OH -):a<b
C.相同温度下,电离常数K( HX):a>b
D.![]() =3,若同时微热两种溶液(不考虑HX 、HY和H2O的挥发),则
=3,若同时微热两种溶液(不考虑HX 、HY和H2O的挥发),则![]() 减小
减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com