
(14分)实验题:
某实验小组拟验证CO2与Na2O2反应的产物,现设计以下实验装置进行实验:

(1)写出装置A中反应的化学方程式__________________________________;
写出装置B中反应的化学方程式__________________________________。
(2)拟用装置D收集气体产物,请在方框中将装置补充完整。

(3)产物检验:
①检验气体产物的方法:________________________________________;
检验固体产物的方法:从B装置中取少量固体,溶于水配成溶液,____________________________________________________________。
(4)有同学认为该实验装置存在明显缺陷,你认为该缺陷是什么____________。
(1)2NaHCO3 === Na2CO3 + CO2↑ + H2O 2Na2O2 + 2CO2 = 2Na2CO3 + O2 (2×2=4分)
(2)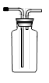 (2分)
(2分)
(3)①打开集气瓶,用带火星的木条伸入瓶内,木条复燃(2分)
②滴加盐酸,将产生的气体通入澄清石灰水,石灰水变浑浊(3分)
(4)碳酸氢钠受热分解产物中有水,水也与过氧化钠反应,干扰二氧化碳与过氧化钠反应产物的检验。(3分)
【解析】
试题分析:(1)碳酸氢钠受热分解生成碳酸钠和水和二氧化碳,方程式为:2NaHCO3 === Na2CO3 + CO2↑ + H2O, 过氧化钠和二氧化碳反应生成碳酸钠和氧气,方程式为:2Na2O2 + 2CO2 = 2Na2CO3 + O2 。(2)收集氧气应该用向上排气法收集。(3)①检验的气体为氧气,利用氧气助燃的性质,所以可以打开集气瓶,用带火星的木条伸入瓶内,木条复燃。②反应生成的固体为碳酸钠,所以检验碳酸钠可以降固体溶于水,滴加盐酸,碳酸钠和盐酸反应生成氯化钠和二氧化碳,将产生的二氧化碳气体通入澄清石灰水,石灰水会生成碳酸钙,溶液变浑浊。(4)因为碳酸氢钠受热分解产物中有水,水也与过氧化钠反应,干扰二氧化碳与过氧化钠反应产物的检验。
考点:碳酸氢钠的性质,过氧化钠的性质。


 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:高中化学 来源:2014-2015学年湖南省五市十校高三下学期3月模拟考试理综化学试卷(解析版) 题型:选择题
乙酸橙花酯是一种食用香料,其结构简式如图所示,关于该有机物的下列叙述中正确的是
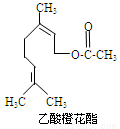
①分子式为C12H20O2
②能使酸性KMnO4溶液褪色
③能发生加成反应,但不能发生取代反应
④它的同分异构体中可能有芳香族化合物,且属
于芳香族化合物的同分异构体有8种
⑤1mol该有机物水解时只能消耗1molNaOH
⑥1mol该有机物在一定条件下和H2反应,共消耗H2为3mol
A.①②③ B.①②⑤ C.①②⑤⑥ D.①②④⑤⑥
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省肇庆市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列有关离子的检验方法和判断正确的是
A.向某溶液中滴加KSCN溶液,若溶液出现血红色则说明原溶液中含Fe3+
B.向某溶液中滴加BaCl2溶液,若有白色沉淀,再滴加足量稀HNO3,若沉淀不溶解,则说明原溶液中一定含Ag+
C.向某溶液中滴加足量稀HCl,产生气体能使澄清石灰水变浑浊,则说明原溶液中一定含CO32-
D.用铂丝蘸取某溶液在酒精灯火焰上灼烧直接观察火焰颜色,未见紫色,说明原溶液中不含K+
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省肇庆市高二上学期期末考试化学试卷(解析版) 题型:选择题
下列电离或离子方程式正确的是
A.亚硫酸的电离方程为:H2SO3H++HSO3-
B.NaHS水解的离子方程式为:HS-+H2OH3O++S2-
C.氯化铵水解的离子方程式为: NH4+ +H2ONH3·H2O+H+
D.Na2CO3水解的离子方程式为:CO32-+2H2OH2CO3+2OH-
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省肇庆市高二上学期期末考试化学试卷(解析版) 题型:选择题
下列关于中和滴定的操作错误的是
A.滴定前需要检查滴定管是否漏水
B.用对应加入的溶液润洗的仪器有:酸式滴定管、锥形瓶
C.用标准盐酸测定氨水的浓度,最适宜使用的指示剂是甲基橙
D.已知浓度滴定未知溶液,终点读数时俯视滴定管的刻度,会造成计算值偏低
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省广州市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列离子方程式书写正确的是
A.AlCl3溶液中加入过量氨水 Al3++4NH3·H2O= AlO2ˉ + 4NH4+ + 2H2O
B.Ba(OH)2溶液中加入稀硫酸 Ba2+ + OHˉ + H+ + SO42-= BaSO4↓+ H2O
C.Cu(OH) 2浊液中滴加盐酸 Cu(OH) 2+2H+ = Cu2++2H2O
D.NaHCO3溶液与硫酸溶液的反应 HCO3-+H+ = H2O + CO2↑
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省广州市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列除杂质的方法不可行的是
A.除去NaHCO3溶液中少量的Na2CO3:通入过量的CO2
B.除去FeCl2溶液中少量的FeCl3:加入稍过量铁粉,过滤
C.除去K2CO3固体中少量NaHCO3:置于坩埚中加热
D.用盐酸除去AgCl中少量的Ag2CO3
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省广州市五校高二上学期期末联考化学试卷(解析版) 题型:选择题
下图表示反应X(g) 4Y(g)+Z(g),△H<0,在某温度时X的浓度随时间变化的曲线:下列有关该反应的描述正确的是
4Y(g)+Z(g),△H<0,在某温度时X的浓度随时间变化的曲线:下列有关该反应的描述正确的是
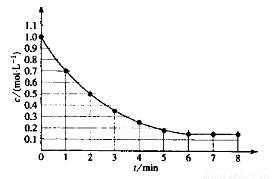
A.X的平衡转化率为85%
B.第6 min 后,反应就终止了
C.第6 min 后,若降低温度,正速率增大,逆速率减少,平衡向正方向移动
D.若升高温度,X的平衡转化率将小于85%
查看答案和解析>>
科目:高中化学 来源:2014-2015学年云南省高三上学期期中考试化学试卷(解析版) 题型:填空题
(8分)无色透明溶液中可能含有下列离子:K+、Al3+、Fe3+、Ba2+、NO3-、SO42-、HCO3-、Cl-,取该溶液进行如下实验:①用蓝色石蕊试纸检测该溶液,试纸显红色;
②取原溶液少许,加铜片和稀硫酸共热,产生无色气体,该气体遇空气立即变为红棕色;
③取原溶液少许,加入氨水有白色沉淀生成,继续加入过量氨水,沉淀不消失;
④取原溶液少许,滴入氯化钡溶液产生白色沉淀;
⑤取实验④后的澄清溶液,滴入硝酸银溶液产生白色沉淀,再加入过量的稀硝酸,沉淀不消失。请回答下列问题:
(1)根据上述实验判断原溶液中上述离子肯定存在的是 ,
肯定不存在的是 。
(2)写出与②③两个实验有关的离子方程式:
② ,
③ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com