
【题目】下列几种物质:
①CO2 ②Cu ③FeCl3溶液 ④H2SO4 ⑤氢氧化铁胶体 ⑥Al2(SO4)3固体 ⑦乙醇 ⑧氨水 ⑨BaSO4固体 ⑩盐酸
(1)上述物质中属于电解质的是__________,属于非电解质的是__________。(填写编号)
(2)下列关于③和⑤的说法正确的是____________(填字母序号)。
a.都不稳定,密封静置会产生沉淀 b.⑤能产生丁达尔效应,而③不能
c.分散质微粒都可以通过滤纸 d.加入盐酸都会先产生沉淀,后溶解
(3)②与④的浓溶液反应的化学反应方程式为________________________________。
(4)写出制备⑤的离子反应方程式 ________________________________________。
【答案】④⑥⑨ ①⑦ bc Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O Fe3++3H2O
CuSO4+SO2↑+2H2O Fe3++3H2O ![]() Fe(OH)3(胶体)+3H+
Fe(OH)3(胶体)+3H+
【解析】
根据含有自由移动的带电微粒(如离子、电子)的物质能导电;电解质是熔融态或水溶液状态下能导电的化合物,该定义的前提必须是化合物;非电解质是在水溶液里或熔融状态下都不能导电的化合物,该定义的前提必须是化合物。
(1)①CO2 本身不能电离出自由移动的离子,是化合物,属于非电解质;
②Cu是单质,既不是电解质,也不是非电解质;
③FeCl3溶液属于混合物,既不是电解质,也不是非电解质;
④H2SO4溶于水能导电,属于电解质;
⑤氢氧化铁胶体属于混合物,既不是电解质也不是非电解质;
⑥Al2(SO4)3固体溶于水或熔融状态下能导电,是电解质,
⑦酒精是非电解质,不导电;
⑧氨水是混合物,可以导电,不是电解质,也不是非电解质;
⑨BaSO4固体是电解质,固体不导电;
⑩盐酸溶液中含有离子,可以导电,但溶液是混合物,不是电解质,也不是非电解质;
故上述物质中属于电解质的是④⑥⑨,属于非电解质的是①⑦;
(2)a.溶液很稳定,胶体具有介稳性,故a错误;
b.胶体具有丁达尔效应,溶液不具备,故b正确;
c.溶液与胶体均可以透过滤纸,胶体不能透过半透膜,故c正确;
d.加入盐酸,胶体先聚沉,后溶解,溶液无现象,故d错误;
答案选bc;
(3)②与④的浓溶液反应是铜墙铁壁与浓硫酸在加热条件下反应生成硫酸铜、二氧化硫和水,反应的化学反应方程式为Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O;
CuSO4+SO2↑+2H2O;
(4)将饱和氯化铁溶液滴加到沸水中制备⑤,反应的离子反应方程式Fe3++3H2O ![]() Fe(OH)3(胶体)+3H+。
Fe(OH)3(胶体)+3H+。


科目:高中化学 来源: 题型:
【题目】某一定量的苯的同系物A完全燃烧,生成的气体通过浓硫酸后,浓硫酸增重5.4克,再通过KOH溶液后,KOH溶液增重19.8克,(设浓硫酸和KOH溶液的吸收率为100%)。
(1)通过计算确定A的分子式。(写出计算过程)_________________
(2)若0.1molA的氧化产物(被酸性高锰酸钾氧化)恰好被2mol/L100mL的NaOH溶液完全中和。写出A可能的的结构简式。_________________________
(3)若A的核磁共振氢谱中只有2种峰,则写出A的结构简式。_____________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】方铅矿的主要成分为PbS,含铅可达86.6%。以方铅矿为原料制备铅蓄电池的电极材料PbO2的工艺流程如图所示:
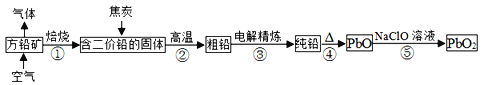
(1)方铅矿焙烧后排出气体的主要成分是______(填化学式),可用于工业制备________。
(2)步骤②中焦炭的作用是________。
(3)“粗铅”的杂质主要有锌、铁、铜、银等。电解精炼时,________作阴极,阴极反应式为________,阳极泥的主要成分是________。
(4)步骤⑤中制备PbO2的离子方程式________。
(5)已知:常温下,Ksp(PbS)=8×10-28、Ka1(H2S)=1.3×10-7、Ka2(H2S)=7.1×10-15。常温下,向Pb(NO3)2溶液中通入H2S气体,发生反应的离子方程式是________;结合数据分析,该反应能否进行得基本完全?________(写出计算推理过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是

选项 | a中的物质 | b中的物质 | c中收集的气体 | d中的物质 |
A | 浓氨水 | CaO | NH3 | H2O |
B | 浓硫酸 | Na2SO3 | SO2 | NaOH溶液 |
C | 稀硝酸 | Cu | NO2 | H2O |
D | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现在污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚( ![]() ),其原理如图所示,下列说法正确的是( )
),其原理如图所示,下列说法正确的是( )

A. 当外电路中有0.2mole―转移时,A极区增加的H+个数为0.2NA
B. A极的电极反应式为 ![]()
C. 该装置为电解池,电流方向从A极沿导线经小灯泡流向B极
D. B 极接电池的正极,发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验操作、现象和结论都正确的是
选项 | 实验操作 | 现象 | 结论 |
A | 向BaCl2溶液中通入CO2 | 产生白色沉淀 | 白色沉淀为BaCO3 |
B | 向 NaHCO3溶液中先加入CaCl2溶液,再加入NaOH溶液 | 产生白色沉淀 | 白色沉淀为CaCO3 |
C | 向某溶液加入NaOH溶液,用湿润的红色石蕊试纸检验产生的气体 | 湿润的红色石蕊试纸未变蓝 | 该溶液中一定不含有 |
D | 向某溶液中先加入HNO3溶液,再加入BaCl2溶液 | 产生白色沉淀 | 该溶液中一定含有 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气是一种重要的工业原料,可以制备如下图所示的一系列物质(部分产物未标出)
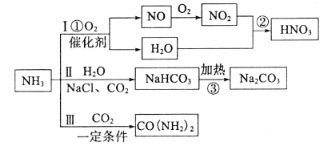
(1)线路Ⅰ为硝酸的制备
写出反应①的化学方程式________;反应②中氧化剂与还原剂的物质的量之比为_______,工业尾气中的氮氧化物常采用碱液法吸收,若NO与NO2按物质的量之比1:1被足量NaOH溶液完全吸收后只得到一种钠盐,该钠盐的化学式是_______。
(2)路线为Ⅱ纯碱的制备
写出反应③的化学方程式________,最终得到的纯碱中可能含有NaCl,检验是否存在NaCl的实验方案是________
(3)路线Ⅲ为尿素的制备
写出合成尿素的化学方程式________
(4)实验室中需要少量氨气,写出制备氨气的化学方程式________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通常情况下,NCl3是一种油状液体,其分子空间构型与NH3相似,下列对NCl3和NH3的有关叙述正确的是( )
A. 分子中N—Cl键键长与CCl4分子中C—Cl键键长相等
B. 在氨水中,大部分NH3与H2O以氢键(用“…”表示)结合形成NH3·H2O分子,则NH3·H2O的结构式为: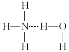
C. NCl3分子是非极性分子
D. NBr3比NCl3易挥发
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】榴石矿石可以看作CaO、FeO、Fe2O3、Al2O3、SiO2组成。工业上对其进行综合利用的流程如下:

(1)用方程式表示盛放氢氧化钠溶液的试剂瓶不能用玻璃塞的原因________;
(2)溶液Ⅰ中除了Ca2+外,还可能含有的金属阳离子有_______________;
(3)步骤③中NaOH参加反应的离子方程式是________________,鼓入空气并充分搅拌的目的是_____________________。
(4)在工业生产中,步骤④通入过量CO2而不加入盐酸的原因是___________;写出步骤④通入过量CO2的离子方程式 _________________________________。
(5)试设计实验证明榴石矿中含有FeO(试剂任选,说明实验操作与现象)_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com