
【题目】如图所示的图解表示构成生物体的元素,化合物及其作用,其中a、b、d、e、f代表小分子,A、B、E代表不同的生物大分子,请据图回答下列问题。

(1)物质a表示_______,其在原核细胞中共有______种。
(2)若E是动物细胞中特有的储能物质,则E是_______,其在人体中主要分布于______细胞。
(3)物质d是_____,物质f是_______,其在动植物细胞中均可含有,并且由于含能量多而且占体积小被生物作为长期储备能源的物质。
(4)物质b的名称是______,图中的“?”是指______元素。若某种B分子由n个b(平均相对分子质量为m)形成的两条链组成,则该B分子的相对分子质量大约为_________。
【答案】核苷酸 8 糖原 肝脏细胞和肌肉 雌性激素 脂肪 氨基酸 N mn-18(n-2)
【解析】
根据题意和图示分析可知:abde小分子分别表示核苷酸、氨基酸、性激素、葡萄糖;ABEF生物大分子分别表示核酸、蛋白质、糖原或淀粉、脂肪.明确知识点,梳理相关的基础知识,分析题图,结合问题的具体提示综合作答。
(1)物质a由C、H、O、N、P五种元素组成,又是病毒的主要成分,所以A表示核酸,a表示核苷酸.由于原核细胞中含DNA和RNA,所以共有8种核苷酸。
(2)细胞中的储能物质有脂肪、淀粉和糖原,其中淀粉是植物细胞中特有的储能物质,糖原是动物细胞中特有的储能物质,分布在人体的肝脏细胞和肌肉细胞,分别为肝糖原和肌糖原。
(3))物质d能促进生殖器官的发育,激发并维持雌性第二性征的是雌性激素。生物体作为长期备用能源物质的是脂肪,其碳氢比例高,在动植物细胞中均可含有,并且由于含能量多而且占体积小,从进化的角度这是经过长期的自然选择的结果。
(4)病毒的主要成分是核酸和蛋白质,由于A中含P元素,所以B只能是蛋白质,因此图中的?是指N元素,物质b是氨基酸。根据蛋白质相对分子质量=氨基酸平均相对分子质量×氨基酸数量-失去水分子数×水的相对分子质量,B分子的相对分子质量大约为mn-(n-2)×18。


 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】扁桃酸衍生物是重要的医药中间体。以A和B为原料合成扁桃酸衍生物F的路线如下:
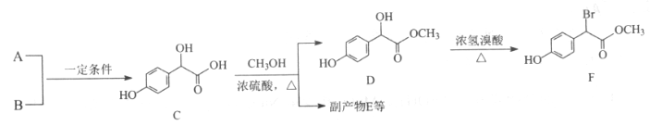
(1)A分子式为C2H2O3,可发生银镜反应,且具有酸性,A所含官能团名称为______。写出A+B→C的化学反应方程式:__________________。
(2)C( )中①、②、③3个一OH的酸性由弱到强的顺序是_____。
)中①、②、③3个一OH的酸性由弱到强的顺序是_____。
(3)E是由2分子C生成的含有3个六元环的化合物,E分子中不同化学环境的氢原子有______种。
(4)D→F的反应类型是_____,1molF在一定条件下与足量NaOH溶液反应,最多消耗NaOH的物质的量为______mol。写出符合下列条件的F的所有同分异构体(不考虑立体异构)的结构简式:__________。
①属于一元酸类化合物:②苯环上只有2个取代基且处于对位,其中一个是羟基。
(5)已知:R一CH2COOH![]() R一
R一![]() 一COOH A有多种合成方法,在方框中写出由乙酸合成A的路线流程图(其他原料任选)。合成路线流程图示例如下:______________________
一COOH A有多种合成方法,在方框中写出由乙酸合成A的路线流程图(其他原料任选)。合成路线流程图示例如下:______________________
CH2=CH2![]() CH3CH2OH
CH3CH2OH![]() CH3COOC2H5
CH3COOC2H5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用CO和H2生产燃料甲醇(CH3OH)。一定条件下密闭容器中发生反应,测得数据曲线如图所示(反应混合物均呈气态)。下列说法错误的是
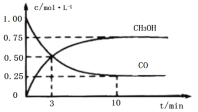
A.反应的化学方程式:CO+2H2CH3OH
B.反应进行至3分钟时,正、逆反应速率相等,反应达到平衡状态
C.反应至10分钟,CO的转化率为75%
D.反应至3分钟,用甲醇来表示反应的平均速率为![]() mol/(L·min1)
mol/(L·min1)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示装置,电流表指针发生偏转,同时A极逐渐变粗,B极逐渐变细,C为电解质溶液,则A、B、C应是下列各组中的( )。
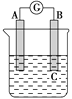
A. A是Zn,B是Cu,C为稀硫酸
B. A是Cu,B是Zn,C为稀硫酸
C. A是Fe,B是Ag,C为稀AgNO3溶液
D. A是Ag,B是Fe,C为稀AgNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,相同pH的盐酸和醋酸溶液分别加水稀释,pH随溶液体积变化的曲线如图所示。据图判断正确的是 ( )

A. Ⅱ为盐酸稀释时的pH变化曲线
B. b点溶液的导电性比c点溶液的导电性强
C. a点Kw的数值比c点Kw的数值大
D. b点H+的浓度大于a点H+的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组利用反应4HCl(浓)+MnO2![]() MnCl2+2H2O+Cl2↑。制取纯净、干燥的氯气,装置如图所示:
MnCl2+2H2O+Cl2↑。制取纯净、干燥的氯气,装置如图所示:

请回答下列问题:
(1)a装置的名称________
(2)收集氯气的方法有________
(3)烧瓶中发生反应的离子方程式为___________
(4)装置B中饱和食盐水的作用是_______,装置E的作用是______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A.锌粒与稀醋酸反应:Zn+2H+=Zn2++H2↑
B.铜和氯化铁溶液反应:Fe3++Cu=Fe2++Cu2+
C.实验室制备氯气的反应:MnO2+2Clˉ+4H+![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
D.硫酸氢铵溶液和少量氢氧化钠溶液反应:OHˉ+NH4+=NH3·H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. 25℃时 NH4Cl 溶液的 KW 大于 100℃时 NaCl 溶液的 KW
B. 常温下,pH 均为 5 的醋酸和硫酸铝两种溶液中,由水电离出的氢离子浓度之比为 1:104
C. 根据溶液的 pH 与酸碱性的关系,推出 pH=6.8 的溶液一定显酸性
D. 100℃时,将 pH=2 的盐酸与 pH=12 的 NaOH 溶液等体积混合,溶液显中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.在任何条件下,1mol任何气体的体积都是22.4L
B.同温同压下,相同体积的两种气体物质,其物质的量一定相等
C.在相同温度下,气体分子间的平均距离几乎相等
D.测得1mol某气体的体积为22.4L,则测定条件一定是标准状况
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com