
【题目】碳、氮、硫是中学化学重要的非金属元素,在工农业生产中有广泛的应用。
(1)用于发射“天宫一号”的长征二号火箭的燃料是液态偏二甲肼(CH3)2N-NH2,氧化剂是液态四氧化二氮。二者在反应过程中放出大量能量,同时生成无毒、无污染的气体。已知室温下,1 g燃料完全燃烧释放出的能量为42.5kJ,请写出该反应的热化学方程式_________________。
(2)298 K时,在2L恒容密闭容器中发生反应:2NO2(g)![]() N2O4(g)ΔH=-a kJ·mol-1 (a>0)。N2O4的物质的量浓度随时间变化如图1。达平衡时,N2O4的浓度为NO2的2倍,回答下列问题。
N2O4(g)ΔH=-a kJ·mol-1 (a>0)。N2O4的物质的量浓度随时间变化如图1。达平衡时,N2O4的浓度为NO2的2倍,回答下列问题。

①298k时,该反应的平衡常数为________。
②在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图2所示。
下列说法正确的是( )
a.A、C两点的反应速率:A>C
b.B、C两点的气体的平均相对分子质量:B<C
c.A、C两点气体的颜色:A深,C浅
d.由状态B到状态A,可以用加热的方法
③若反应在398K进行,某时刻测得n(NO2)=0.6 mol 、n(N2O4)=1.2mol,则此时V(正) V(逆)(填“>”“<”或“=”)。
(3)NH4HSO4在分析试剂、医药、电子工业中用途广泛。现向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图3所示。试分析图中a、b、c、d、e五个点,
①水的电离程度最大的是__________(填“a”“b”“c”“d”或“e”,下同)
②其溶液中c(OH-)的数值最接近NH3·H2O的电离常数K数值的是 ;
③在c点,溶液中各离子浓度由大到小的排列顺序是_______。
【答案】(1)C2H8N2(l)+2N2O4(l)=2CO2(g)+3N2(g)+4H2O(l) ΔH=-2550 kJ·mol-1
(2)①6.67;②d;③<
(3)①b;②d;③c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+)
【解析】
试题分析:(1)1g燃料完全燃烧释放出的能量为42.5kJ,则1mol偏二甲肼完全燃烧释放出的能量为42.5kJ×60=2550kJ,其热化学方程式为:C2H8N2(l)+2N2O4(l)═2CO2(g)+3N2(g)+4H2O(l)△H=-2550 kJ/mol;
故答案为:C2H8N2(l)+2N2O4(l)═2CO2(g)+3N2(g)+4H2O(l)△H=-2550 kJ/mol;
(2)①有图可知N2O4的平衡浓度为0.6mol/L,达到平衡时,N2O4的浓度为NO2的2倍,则NO2的平衡浓度为0.3mol/L,则K=![]() =
=![]() =6.67L/mol。
=6.67L/mol。
故答案为:6.67L/mol;
②a.压强越大,反应速率越快,所以A、C两点的反应速率:A<C,故a错误;b.混合气体的平均相对分子质量=![]() ,BC两点混合气体的质量和物质的量都相等,所以混合气体的平均相对分子质量B=C,故b错误;c.NO2的含量越高,混合气体的颜色越深,C点压强大于A点,加压平衡向生成N2O4的方向移动,但NO2的浓度比原平衡大,所以混合气体的颜色A点浅C点深,故c错误;d.可逆反应2NO2(g)N2O4(g)△H=-a kJmol-1 (a>0)放热,温度升高平衡逆向移动,二氧化氮含量增大,所以由状态B到状态A,可以用加热的方法,故d正确。
,BC两点混合气体的质量和物质的量都相等,所以混合气体的平均相对分子质量B=C,故b错误;c.NO2的含量越高,混合气体的颜色越深,C点压强大于A点,加压平衡向生成N2O4的方向移动,但NO2的浓度比原平衡大,所以混合气体的颜色A点浅C点深,故c错误;d.可逆反应2NO2(g)N2O4(g)△H=-a kJmol-1 (a>0)放热,温度升高平衡逆向移动,二氧化氮含量增大,所以由状态B到状态A,可以用加热的方法,故d正确。
故答案为:d;
③反应为放热反应,升高温度,K值减小,密闭容器的体积为2L,因此的N2O4的浓度为0.6mol/L,N2O4的浓度为0.3mol/L,浓度商Q=![]() =
=![]() =6.67L/mol=K(298K)>K(398K),反应向逆反应方向移动,因此V(正)<V(逆)。
=6.67L/mol=K(298K)>K(398K),反应向逆反应方向移动,因此V(正)<V(逆)。
故答案为:<;
(3)①a、b、c、d、e五个点,根据反应量的关系,b点恰好消耗完H+,溶液中只有(NH4)2SO4与Na2SO4;c、d、e三点溶液均含有NH3H2O,(NH4)2SO4可以促进水的电离,而NH3H2O抑制水的电离,因此水的电离程度最大的是b点,溶液中c(OH-)的数值最接近NH3H2O的电离常数K数值。
故答案为:b;
②氨水为弱碱,溶液呈碱性,c点溶液呈中性,铵根离子浓度过大,e点溶液碱性过强,一水合氨浓度过大,相对而言d点溶液中铵根离子浓度与一水合氨浓度最接近,溶液中c(OH-)的数值最接近NH3H2O的电离常数K数值。
故答案为:d;
③c点溶液呈中性,即溶液含有(NH4)2SO4、Na2SO4、NH3H2O三种成分,b点时c(Na+)=c(SO42-),c点时c(Na+)>c(SO42-),根据N元素与S元素的关系,可以得出c(SO42-)>c(NH4+),故c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+)。
故答案为:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+)。


科目:高中化学 来源: 题型:
【题目】化学与材料、生活和环境密切相关。下列有关说法中错误的是( )
A. 某新型航天服材料主要成分是由碳化硅、陶瓷和碳纤维复合而成,它是一种新型无机非金属材料
B. 玛瑙饰品的主要成分与建筑材料砂子相同
C. 明矾净水时发生了化学及物理变化,能起到净水作用,而没有杀菌、消毒的作用
D. 医用酒精是利用了乙醇的氧化性来杀菌消毒的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙二醛(OHC-CHO)是一种重要的精细化工产品。
Ⅰ.工业生产乙二醛
(1)乙醛(CH3CHO)液相硝酸氧化法
在Cu(NO3)2催化下,用稀硝酸氧化乙醛制取乙二醛,反应的化学方程式为 。该法具有原料易得、反应条件温和等优点,但也存在比较明显的缺点是 。
(2)乙二醇(HOCH2CH2OH)气相氧化法
① 已知:OHC-CHO(g)+2H2(g)![]() HOCH2CH2OH(g) ΔH=-78 kJ·mol-1 K1
HOCH2CH2OH(g) ΔH=-78 kJ·mol-1 K1
2H2(g)+O2(g)![]() 2H2O(g) ΔH=-484 kJ·mol-1 K2
2H2O(g) ΔH=-484 kJ·mol-1 K2
乙二醇气相氧化反应HOCH2CH2OH(g)+O2(g)![]() OHC—CHO(g)+2H2O(g)的ΔH= kJ·mol-1。相同温度下,该反应的化学平衡常数K= (用含K1、K2的代数式表示)。
OHC—CHO(g)+2H2O(g)的ΔH= kJ·mol-1。相同温度下,该反应的化学平衡常数K= (用含K1、K2的代数式表示)。

② 当原料气中氧醇比为1.35时,乙二醛和副产物CO2的产率与反应温度的关系如下图所示。反应温度在450~495℃之间和超过495℃时,乙二醛产率降低的主要原因分别是 、
Ⅱ.乙二醛电解氧化制备乙醛酸(OHC—COOH)的生产装置如下图所示,通电后,阳极产生的Cl2 与乙二醛溶液反应生成乙醛酸。

(3)阴极电极式为
(4)阳极液中盐酸的作用,除了产生氯气外,还有
(5)保持电流强度为a A,电解t min,制得乙醛酸m g,列式表示该装置在本次电解中的电流效率η=
(设:法拉第常数为f C·mol-1;η=![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(I)有机物M(分子式:C6H4S4)是隐形飞机上吸波材料的主要成分。某化学兴趣小组为验证其组成元素,进行了如下实验:将少量样品放入A的燃烧管中,通入足量O2,用电炉加热使其充分燃烧,并将燃烧产物依次通入余下装置。(右图中的夹持仪器的装置已略去)
(1)装置B的目的是验证有机物中含氢元素,则B中盛装的试剂名称为 ________;
(2)能证明有机物含碳元素的现象是__________;
(3)指出装置F中的错误: ________。
(II)苯甲酸的重结晶实验基本操作如下:①将粗苯甲酸1g加到100mL的烧杯中,再加入50mL蒸馏水,在石棉网上边搅拌边加热,使粗苯甲酸溶解,②全溶后再加入少量蒸馏水并搅拌.③然后,使用短颈玻璃漏斗趁热将溶液过滤到另一100mL烧杯中,将滤液静置,使其缓慢冷却结晶.④滤出晶体。
回答下列问题:
(1)上述四步操作过程中需用到玻璃棒的步骤有____________;
(2)步骤②的目的是____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示几种无机物之间的转换关系。其中A、B均为黑色粉末,B为非金属单质,C为无色无毒气体,D为金属单质,E是红棕色气体,G是具有漂白性的气体,H的水溶液呈蓝色。

请回答下列问题:
(1)A的化学式是 ,C的电子式是 ,Y的名称是 。
(2)反应1的化学方程式为 。
(3)19.2g的D与足量的一定浓度X的溶液反应,将所得到的气体与 LO2(标准状况下)混合,恰好能被水完全吸收。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y和W为原子序数依次递增的短周期元素,X和Y同主族,Y和W的气态氢化物具有相同的电子数,一般情况下X的单质只有氧化性:
(1)写出实验室制取W2反应的离子方程式: 。
(2)某小组设计如图所示的实验装置(图中夹持和加热装置略去),分别研究YX2、W2的性质。

①分别通入YX2和W2,在装置A中观察到的现象是否相同 (填“相同”、“不相同”);若装置D中装的是铁粉,当通入W2时D中观察到的现象为 ;若装置D中装的是五氧化二钒,当通入YX2时,打开K通入适量X2,化学方程式为 。
②若装置B中装入5.0mL1.0×10-3mol/L的碘水,当通入足量W2完全反应后,转移了5.0×10-5mol电子,则该反应的化学方程式为 。
(3)某同学将足量的YX2通入一支装有氯化钡溶液的试管,未见沉淀生成,向该试管中加入过量 (填字母)可以看到白色沉淀生成。
A.氨水 | B.稀盐酸 | C.稀硝酸 | D.氯化钙 |
(4)如由元素Y和X组成-2价酸根Z,Z中Y和X的质量比为Y:X=4:3,当W2与含Z的溶液完全反应后,有浅黄色沉淀产生,取上层清液加入足量氯化钡溶液,有白色沉淀产生,且两种沉淀物质量相等。写出W2与Z的溶液完全反应产生浅黄色沉淀的离子方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种以黄铜矿和硫磺为原料制取铜和其他产物的新工艺,原料的综合利用率较高。其主要流程如下。请回答下列问题:
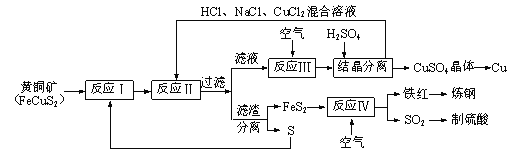
(1)反应Ⅲ的离子方程式为4CuCl2-+O2+4H+=4Cu2++8Cl-+2H2O,CuCl2-中铜元素的化合价为______,该反应中的氧化剂是___________。
(2)一定温度下,在反应Ⅲ所得的溶液中加入硫酸,可以析出硫酸铜晶体而不析出氯化铜晶体,其原因可能是____________________________________________________。
(3)炼钢时,可将铁红投入熔融的生铁中,以降低生铁的含碳量,该过程中主要反应的化学方程式是______________________________________________________________。
(4)SO2尾气直接排放到大气中造成环境污染的后果是_____________________________。
(5)已知反应Ⅱ的离子方程式为Cu2++CuS+4Cl—=2CuCl2-+S,反应Ⅰ的产物为_____________和_____________。(填化学式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜、铁、铝都是日常生活中常见的金属,具有广泛用途。请回答:
(1)铜元素在元素周期表中位于 ,其原子基态价层电子排布式为 。
(2)Cu2O的熔点比Cu2S的高,原因为 。
(3)Fe(CO)5是一种常见的配合物,可代替四乙基铅作为汽油的抗爆震剂。
①写出CO的一种常见等电子体分子的结构式 ;
两者相比较沸点较高的为 (填分子式)。
②Fe(CO)5在一定条件下发生反应:
Fe(CO)5(s)=Fe(s)+5CO(g),已知:反应过程中,断裂的化学键只有配位键,由此判断该反应所形成的
化学键类型为 。
(4)已知AlCl3·NH3有配位键。在AlCl3·NH3中,提供空轨道的原子是 ;在NH4+中N原子的杂化轨道类型为 。
(5)金属铝的晶胞结构如图甲所示,原子之间相对位置关系的平面图如图乙所示。则晶体铝中原子的堆积方式为 。已知:铝原子半径为d cm,摩尔质量为M g·mol-1,阿伏加德罗常数的值为NA,则晶体铝的密度ρ= (表达式)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机合成中常用的钯/活性炭催化剂若长期使用,会被铁、有机化合物等杂质污染而失去活性,成为废催化剂,一种由废催化剂制取PdCl2的工艺流程如下:

请回答下列问题:
(1)“焙烧1”的目的是___________________________。
(2)写出甲醇(HCOOH)与PdO反应的化学方程式______________________。
(3)在“调pH为8-9”是为了除去铁元素,写出除铁的离子方程式为______________________。
(4)加入浓盐酸酸洗的目的是___________________。
(5)写出证明“焙烧2”中固体已分解完全的实验操作___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com