
����Ŀ����֪�缫��ÿͨ��96500 C�ĵ����ͻ���1 mol���ӷ���ת�ơ���ȷ�������������ڶ��Ե缫���ԶƲ���ʽ�����Ľ�������������ȷ����������ͨ�����صĵ�����ʵ�ʲ����У������������ƣ���ͼ��ʾ������˵������ȷ����
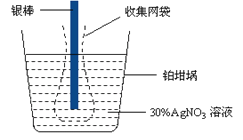
A. ��Ҫ�ⶨ��ⱥ��ʳ��ˮʱͨ���ĵ������ɽ������������е������������ص��������������������Դ�ĸ���������
B. �������ǰ�������������仯���ý������ij�����Ϊ108.0 mg�����������ͨ�����صĵ���Ϊ96.5 C
C. ʵ���У�Ϊ�˱������ܽ�����п��ܲ����Ľ����������������������²������������缫��������һ���ռ���������û���ռ����������������ƫ�ߡ�
D. �������е�����Ӧ���Դ�����������������������ĵ缫��Ӧ�ǣ�Ag+ + e- = Ag
���𰸡�A
���������õ������൱�ڲ��϶��������Ը����������е������������ص��������������������Դ�ĸ�����������A��������Ag�����ʵ���Ϊ![]() ������Ag++e-=Ag��֪ͨ���ĵ������ʵ���Ϊ0.001mol��ͨ������Ϊ96.5C����B��ȷ�����ܽ�ʱ��Щ��ԭ�ӿ���δʧ���ӱ�������ӣ�����ֱ�ӵ��䵽�������У���ɲ��������ؽ϶࣬���¼�����ĵ���ƫ�����Ա��������ռ�������C��ȷ���õ������൱�ڲ��϶�����������Pt����Ag++e-�TAg����D��ȷ��
������Ag++e-=Ag��֪ͨ���ĵ������ʵ���Ϊ0.001mol��ͨ������Ϊ96.5C����B��ȷ�����ܽ�ʱ��Щ��ԭ�ӿ���δʧ���ӱ�������ӣ�����ֱ�ӵ��䵽�������У���ɲ��������ؽ϶࣬���¼�����ĵ���ƫ�����Ա��������ռ�������C��ȷ���õ������൱�ڲ��϶�����������Pt����Ag++e-�TAg����D��ȷ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ȼҵ�Ե�⾫�Ʊ���ʳ��ˮ�ķ�����ȡ�������������ռ���ȵĺ������ε�ϵ�л�����Ʒ����ͼ�����ӽ���Ĥ�����ʳ��ˮ��ʾ��ͼ��ͼ�е����ӽ���Ĥֻ����������ͨ����
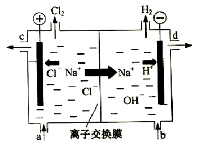
���������գ�
��1��д����ⱥ��ʳ��ˮ�����ӷ���ʽ��
��2�����ӽ���Ĥ������Ϊ�� ��
��
��3�����Ʊ���ʳ��ˮ��ͼ�� λ�ò��䣬����������Һ��ͼ�� λ����������ѡ�a������b������c����d����
��4��KClO3���ԺͲ��ᣨH2C2O4�������ᷴӦ���ɸ�Ч������ɱ����ClO2��������CO2��KHSO4�����ʡ�д���÷�Ӧ�Ļ�ѧ����ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ��о�����ػ��ͻ�ƣ���ص��ܷ�Ӧ��16Li+S8 ![]() 8Li2S ����ŵ�������ͼ��ʾ������˵������ȷ����( )
8Li2S ����ŵ�������ͼ��ʾ������˵������ȷ����( )
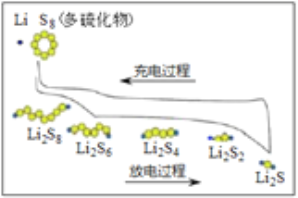
A. ���ʱ������ת��Ϊ��ѧ��
B. �ŵ�ʱ��������������ƶ�
C. �ŵ�ʱ��1mol Li2S6ת��ΪLi2S4�õ�2mole-
D. ���ʱ�������ܵ缫��Ӧʽ��8S2- -16e- = S8
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������[Co(H2PO2)2��6H2O]�����ڻ�ѧ��ƣ���������Һ��pHԼΪ6�����õ����������ڲ�Ʒ�������ߴ�[Co(H2PO2)2��6H2O]������ԭ����ͼ��ʾ���������ӽ���Ĥ��
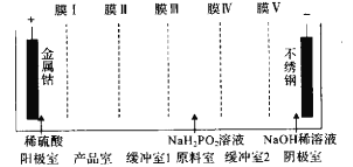
A. 1�� B. 2�� C. 3�� D. 4��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2SO2(g)+O2(g)=2SO3(g) ��H=-198kJ/mol����V2O5����ʱ���÷�Ӧ�Ļ���Ϊ:V2O5+SO2![]() 2VO2+SO3(��) 4VO2+O2
2VO2+SO3(��) 4VO2+O2![]() 2V2O5(��)
2V2O5(��)
����˵����ȷ����
A. ��Ӧ������Ҫȡ����V2O5������ B. VO2�Ǹ÷�Ӧ�Ĵ���
C. �淴Ӧ�Ļ�ܴ���198kJ/mol D. ����SO2��Ũ�ȿ�������߷�Ӧ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ԫ��W��X��Y��Z��ԭ����������������W��X��Y��Z��ɵĵ��ʿɷ�����ͼ��ʾ�Ļ�ѧ��Ӧ��B�������������Һ�壻������Y��Z��ɵĶ�Ԫ�������ˮ��ҺpH=7������˵���������
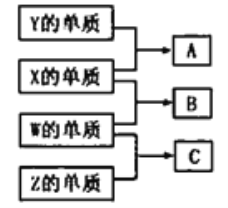
A. A��B�ķ�Ӧһ���ǻ��Ϸ�Ӧ
B. ���Ӱ뾶:Z>X>Y>W
C. W��Y��Z���������ֻ��������ϵ�������
D. �������ʵ�����A��C����ͬһ�ձ�ˮ�У�������Һ��pHһ������7
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����ijԭ���ڴ����������״̬ʱ����Χ�����Ų�Ϊ4d15s2,������˵����ȷ����___(����)
A.��Ԫ��ԭ�Ӵ����������״̬ʱ��ԭ���й���3��δ�ɶԵ���
B.��Ԫ��ԭ�Ӻ����5�����Ӳ�
C.��Ԫ��ԭ�ӵ�M�ܲ㹲��8������
D.��Ԫ��ԭ�����������3������
��2������˵����ȷ����_______(����)
A.���ۼ��ļ���Խ���ۼ�Խ�ι̣��ɸü��γɵķ���Խ�ȶ�
B.H2O��һ�ַdz��ȶ��Ļ�������������������
C.H2O����������O-H���ļ���Ϊ180��
D.���з����ж����й��ۼ�
��3�����ݼ۲���ӶԻ������ۼ�ԭ�ӵ��ӻ������ж�NF3���ӵĿռ乹�ͺ�����ԭ�ӵ��ӻ���ʽΪ____(����)
A.ֱ���� sp�ӻ� B.������ sp2�ӻ�
C.������ sp2�ӻ� D.������ sp3�ӻ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������Է�������Ϊ56��
(1)�����ķ���ʽΪ_________________________��
(2)����ʹ����KMnO4��Һ��ɫ������ܵĽṹ��ʽΪ__________________________��
(3)����(2)�еĻ����������H2��Ӧ�����ò��ﹲ��__________�֡�
(4)����(2)�еĻ������������HBr��Ӧ�����ò��ﹲ��______�֡�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о���ѧϰС������ʦָ������������װ��̽�������백��֮��ķ�Ӧ���������A��F�ֱ�Ϊ��������������ȡ����װ�ã�CΪ������������������İ���������Ӧ��װ�á���ش������й����⣺
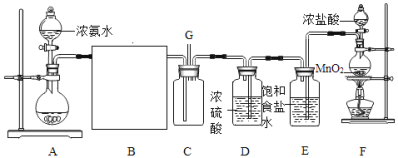
(1)ʵ�����ռ��Ʊ��õ��İ������õķ�����________________��
(2)��ΪB�����߿���ѡ����ܺ��ʵ�װ���Լ���Ӧ���Լ�����__________������ţ���
�����θ����װ��ʯ�� ��ϴ��ƿװŨ���� �����θ����װ�Ȼ��� �����θ����װ��������
(3)װ��F�з�����Ӧ�Ļ�ѧ����ʽΪ��_______________________________����һ�������Ũ�����к���4mol HCl ���ʣ�������������������������̳�ַ�Ӧ�����յõ����������ʵ���_______l mol(�������)��
(4)��D��������________________________��װ��E�������dz�ȥHCl��ʹ�ñ���ʳ��ˮ����ֱ��������ˮ��ԭ����__________________________________________________��
(5)��(CN)2�Ļ�ѧ������±�ص�����Cl2����,��д��(CN)2������KOH��Һ������Ӧ�Ļ�ѧ����ʽ��__________________________________________________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com