
【题目】设NA为阿伏加德罗常数的值。下列有关叙述正确的是
A. 标准状况下,2.24 L苯中含有碳碳双键数为0.3NA
B. 14g由乙烯和丙烯组成的混合气体中含氢原子数为2NA
C. 0.1molCH4与0.1molCl2混合充分光照,生成CH3Cl分子数为0.1 NA
D. 0.1molN2和0.3molH2在高温、高压及催化剂下充分反应,产物的分子数为0.2NA
【答案】B
【解析】A、标准状况下,苯是液体,不能用![]() 求其物质的量,且苯分子中只含有介于C—C键和C=C键之间的特殊共价键,不含碳碳双键,选项A错误;B、乙烯和丙烯的最简式相同,均是CH2,14 g乙烯和丙烯混合气体中的氢原子数为
求其物质的量,且苯分子中只含有介于C—C键和C=C键之间的特殊共价键,不含碳碳双键,选项A错误;B、乙烯和丙烯的最简式相同,均是CH2,14 g乙烯和丙烯混合气体中的氢原子数为![]() =2NA,选项B正确;C、烷和氯气在光照下,会发生四步取代反应,而反应进行到哪一步不是由反应物甲烷和氯气的物质的量之比来决定的,即使甲烷和氯气的物质的量之比是1:1的情况,也不会仅生成CH3Cl,选项C错误;D、N2与H2反应生成的NH3的反应是可逆反应,反应物不能完全转化为生成物, 0.1 molN2与0.3 mol H2反应生成的NH3分子数小于2NA,选项D错误。答案选B。
=2NA,选项B正确;C、烷和氯气在光照下,会发生四步取代反应,而反应进行到哪一步不是由反应物甲烷和氯气的物质的量之比来决定的,即使甲烷和氯气的物质的量之比是1:1的情况,也不会仅生成CH3Cl,选项C错误;D、N2与H2反应生成的NH3的反应是可逆反应,反应物不能完全转化为生成物, 0.1 molN2与0.3 mol H2反应生成的NH3分子数小于2NA,选项D错误。答案选B。


 单元期中期末卷系列答案
单元期中期末卷系列答案科目:高中化学 来源: 题型:
【题目】化石燃料是不可再生的,最终将会枯竭.基于我国目前的技术水平和管理水平,能源从开采、运输、加工到终端的利用效率都很低,浪费很大.据统计,开采效率为32%,加工运输效率为70%,终端利用率为41%,则总效率近似为( )
A.1.43%
B.14.3%
C.9.18%
D.91.8%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列排列顺序不正确的是( )
A.热稳定性:H2O>NH3>PH3
B.原子半径:Si>Na>O
C.碱性:CsOH>KOH>NaOH
D.失电子能力:K>Na>Mg
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】辉铜矿的主要成分是Cu2S,可用于制取金属铜和铜盐。
(1)己知部分反应的热化学方程式如下:
C(s)+S2(g)=CS2(g) ΔH1=akJ·mol-1
Cu2S(s)+H2(g)=2Cu(s)+H2S(g) ΔH2=bkJ·mol-1
2H2S(g)=2H2(g)+S2(g) ΔH3=ckJ·mol-1
则C(s)+2Cu2S(s)=4Cu(s)+CS2(g)的ΔH=_________kJ·mol-1(用含 a、b、c 的代数式表示)。
(2)从辉铜矿中浸取铜元素,可用FeCl3作浸取剂。
①反应Cu2S+4FeCl3=2CuCl2+4FeCl2+S,每生成1mol CuCl2,反应中转移电子的数目为_______;浸取时,在有氧环境下可维持Fe3+较高浓度。有关反应的离子方程式是______________。
②浸取过程中加入洗涤剂溶解硫时,铜元素的浸取率的变化见如图。其原因是_____________。


③353K时,向FeCl3浸取液中加入CuCl2,能加快铜元素的浸取速率,其反应原理可用化学方程式表示为:__________,CuCl+FeCl3=CuCl2+FeCl2。
(3)辉铜矿可由黄铜矿(主要成分为CuFeS2)通过电化学反应转变而成,有关转化见如图。转化时正极的电极反应式为_________________。
(4)CuCl悬浊液中加入Na2S,发生的反应为2CuCl(s)+S2-(aq) ![]() Cu2S(s)+2Cl-(aq),该反应的平衡常数K= ________[己知Ksp(CuCl)=1.2×l0-6,Ksp(Cu2S)=2.5×l0-43]。
Cu2S(s)+2Cl-(aq),该反应的平衡常数K= ________[己知Ksp(CuCl)=1.2×l0-6,Ksp(Cu2S)=2.5×l0-43]。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在溶液中能大量共存,加入OH-有沉淀生成,加入H+有气体生成的一组离子是
A. NH4+、Cl-、HCO3-、K+ B. K+、Cu2+、SO42-、Na+
C. NH4+、Cu2+、 Cl-、NO3- Na+ D. K+、Mg2+、Cl-、HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化碳的捕捉、封存与再利用是实现温室气体减排的重要途径之一。
(1)二氧化碳的电子式为___________。
(2)下列利用二氧化碳的反应中原子利用率达100%的是_________(填序号)。
a.CO2+2NH3 ![]() CO(NH2)2+H2O
CO(NH2)2+H2O
b.CO2+CH4![]() CH3COOH
CH3COOH
c.CO2+3H2![]() CH3OH+H2O
CH3OH+H2O
d.![]()
(3)一种正在开发的利用二氧化碳制取甲醇的流程如下:
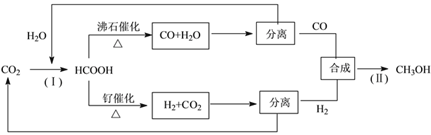
①反应(Ⅰ)将CO2和H2O转化为甲酸常用途径有两种,如下图(a)和(b)。
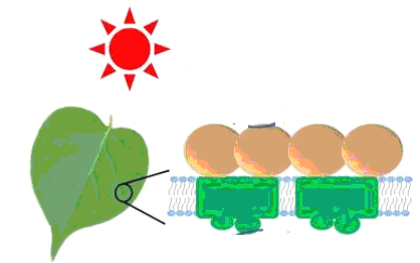
图(a)中能量主要转化方式为___________,图(b)中发生反应的化学方程式为___________。
②在5L的恒温恒容密闭容器中充入1moLCO和4molH2,加入催化剂发生反应,测得CO及CH3OH的物质的量随时间变化如下图所示。
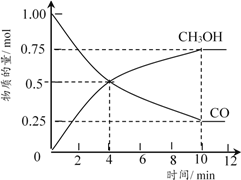
图中第___________min(填数字)反应达到平衡,CO在0~4min内的平均反应速率比在4~8min内的快,其原因是___________;达到平衡时氢气的浓度为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】3mol A和2.5 mol B混合于2L密闭容器中,发生的反应如下:3A(g)+B(g)![]() xC(g)+2D(g)5min后反应达到平衡,容器内压强变小,测得D的平均反应速率为0.1mol/(L·min),下列结论正确的是
xC(g)+2D(g)5min后反应达到平衡,容器内压强变小,测得D的平均反应速率为0.1mol/(L·min),下列结论正确的是
A. A的平均反应速率为0.1mol/(L·min)
B. 平衡时,B的转化率为20%
C. 平衡时,C的浓度为0.125 mol/L
D. 平衡时,容器内的压强为原来的0.875倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W、R为五种短周期元素,其原子半径和最外层电子数之间的关系如下图所示。下列说法错误的是
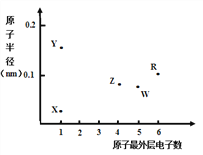
A. 简单离子半径:Y < W
B. 最高价氧化物对应水化物的酸性:Z < W
C. R为氧元素
D. X与Z可以形成正四面体结构的分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通常情况下,氯化钠、氯化铯、二氧化碳和二氧化硅的晶体结构分别如下图所示:
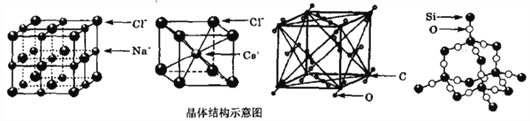
下列关于这些晶体结构和性质的叙述不正确的是( )
A. 在氯化钠晶体中每个Cl-周围同时吸引6个Na+,在氯化铯晶体中每个Cl-周围同时吸引8个Cs+
B. 氯化钠、氯化铯和二氧化碳的晶体都有立方的晶胞结构,它们具有相似的物理性质
C. 二氧化碳晶体是分子晶体,其中不仅存在分子间作用力,而且也存在共价键
D. 在二氧化硅晶体中,硅原子与氧原子个数比为1:2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com