
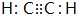 ��D�����ʽCH2=CH2��
��D�����ʽCH2=CH2�� +Br2 $\stackrel{FeBr_{3}}{��}$
+Br2 $\stackrel{FeBr_{3}}{��}$ +HBr���䷴Ӧ����Ϊȡ����Ӧ��B��C�Ļ�ѧ����ʽnCH2=CHCl$\stackrel{����}{��}$
+HBr���䷴Ӧ����Ϊȡ����Ӧ��B��C�Ļ�ѧ����ʽnCH2=CHCl$\stackrel{����}{��}$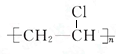 ���䷴Ӧ����Ϊ�Ӿ۷�Ӧ��
���䷴Ӧ����Ϊ�Ӿ۷�Ӧ��
���� D��һ��ֲ���������ڼ����������Դ����ʵ����DΪ��ϩ������A����ת���õ���ϩ����������HCl�����ӳɷ�Ӧ����̼������ˮ��Ӧ��������A����AΪ��Ȳ����Ȳ��HCl�����ӳɷ�Ӧ����B��B������Ӧ���ɺϳ���֬C����BΪCH2=CHCl��CΪ������ϩ������Һ���ڴ��������·���ȡ����Ӧ����EΪ ��
��
��3����ҵ�ϳ���ʯ�͵ķ����Ʊ����͡�ú�͡�ʯ���͵Ȳ�Ʒ��ʯ���ѽ�ķ���������ȡ��ϩ����ϩ��1��3-����ϩ����̬����ԭ�ϣ���ϩ��ˮ��һ�������·����ӳɷ�Ӧ��������ȡ�Ҵ�����F��CH3CH2OH���Ҵ������Ը��������Һֱ������Ϊ���ᣬ��GΪCH3COOH���Ҵ���������Ũ��������·���������Ӧ��������ȡ����������ˮ����H������������CH3COOCH2CH3���й���ζ�������ĺ��������
��� �⣺D��һ��ֲ���������ڼ����������Դ����ʵ����DΪ��ϩ������A����ת���õ���ϩ����������HCl�����ӳɷ�Ӧ����̼������ˮ��Ӧ��������A����AΪ��Ȳ����Ȳ��HCl�����ӳɷ�Ӧ����B��B������Ӧ���ɺϳ���֬C����BΪCH2=CHCl��CΪ������ϩ������Һ���ڴ��������·���ȡ����Ӧ����EΪ ��
��
��1���������Ϸ�����AΪ��Ȳ������ʽΪ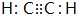 ��DΪ��ϩ����D�Ľṹ��ʽΪCH2=CH2���ʴ�Ϊ��
��DΪ��ϩ����D�Ľṹ��ʽΪCH2=CH2���ʴ�Ϊ��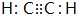 ��CH2=CH2��
��CH2=CH2��
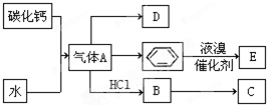
��2��������Ȳ�Ļ�ѧ����ʽΪ��CaC2+2H2O��Ca��OH��2+HC��CH��������E�ķ���ʽΪ +Br2 $\stackrel{FeBr_{3}}{��}$
+Br2 $\stackrel{FeBr_{3}}{��}$ +HBr��Ϊȡ����Ӧ��B�����Ӿ۷�Ӧ����C����Ӧ����ʽΪnCH2=CHCl$\stackrel{����}{��}$
+HBr��Ϊȡ����Ӧ��B�����Ӿ۷�Ӧ����C����Ӧ����ʽΪnCH2=CHCl$\stackrel{����}{��}$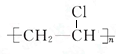 ��
��
�ʴ�Ϊ��CaC2+2H2O��Ca��OH��2+HC��CH���� +Br2 $\stackrel{FeBr_{3}}{��}$
+Br2 $\stackrel{FeBr_{3}}{��}$ +HBr��ȡ����Ӧ��nCH2=CHCl$\stackrel{����}{��}$
+HBr��ȡ����Ӧ��nCH2=CHCl$\stackrel{����}{��}$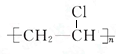 ���Ӿ۷�Ӧ��
���Ӿ۷�Ӧ��
��3����ҵ�ϳ���ʯ�͵ķ����Ʊ����͡�ú�͡�ʯ���͵Ȳ�Ʒ��ʯ���ѽ�ķ���������ȡ��ϩ����ϩ��1��3-����ϩ����̬����ԭ�ϣ���ϩ��ˮ��һ�������·����ӳɷ�Ӧ��������ȡ�Ҵ�����F��CH3CH2OH���Ҵ������Ը��������Һֱ������Ϊ���ᣬ��GΪCH3COOH���Ҵ���������Ũ��������·���������Ӧ��������ȡ����������ˮ����H������������CH3COOCH2CH3���й���ζ�������ĺ��������
a����ҵ�ϣ���ʯ�ͻ�����͡�ú�͡�ʯ���͵ȳɷݵķ����Ƿ��ʴ�Ϊ������
b��D��F�Ļ�ѧ����ʽCH2=CH2+H2O$\stackrel{����}{��}$CH3CH2OH���䷴Ӧ�����Ǽӳɷ�Ӧ���ʴ�Ϊ��CH2=CH2+H2O$\stackrel{����}{��}$CH3CH2OH���ӳɷ�Ӧ��
���� ���⿼���л����ƶϣ�Ϊ��Ƶ���㣬���ؿ���ѧ�������ƶ������������������������Խ����ƶϣ�֪�������л���Ӧ���͡���Ӧ����ʽ����д���л���Ĺ����ż������ʵ�֪ʶ���ǽⱾ��ؼ�����Ŀ�ѶȲ���


 �߲������Ӧ��һ��ͨϵ�д�
�߲������Ӧ��һ��ͨϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
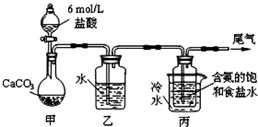 ̼�����׳ƴ�����ճ����������������Ź㷺��Ӧ�ã�ij��ѧ��ȤС���������ѧ֪ʶģ���Ʊ�̼���ƣ��������£�����NaCl��NH3��CO2��ˮ��Ϊԭ���Լ���ͼ��ʾװ����ȡNaHCO3����Ӧ�Ļ�ѧ����ʽΪNH3+CO2+H2O+NaCl�TNaHCO3��+NH4Cl����Ȼ���ٽ�NaHCO3�Ƴ�Na2CO3��
̼�����׳ƴ�����ճ����������������Ź㷺��Ӧ�ã�ij��ѧ��ȤС���������ѧ֪ʶģ���Ʊ�̼���ƣ��������£�����NaCl��NH3��CO2��ˮ��Ϊԭ���Լ���ͼ��ʾװ����ȡNaHCO3����Ӧ�Ļ�ѧ����ʽΪNH3+CO2+H2O+NaCl�TNaHCO3��+NH4Cl����Ȼ���ٽ�NaHCO3�Ƴ�Na2CO3���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | $\frac{{K}^{+}}{K}$ | B�� | $\frac{Mg}{Ca}$ | C�� | $\frac{{O}^{2-}}{N{a}^{+}}$ | D�� | $\frac{Cl}{C{l}^{-}}$ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
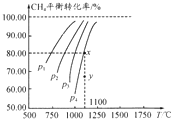 ��һ�ݻ�������ܱ������г���0.1mol/LCO2��0.1mol/LCH4����һ�������·�����Ӧ��CH4��g��+CO2��g��?2CO��g��+2H2��g�������ƽ��ʱCH4��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ�������й�˵����ȷ���ǣ�������
��һ�ݻ�������ܱ������г���0.1mol/LCO2��0.1mol/LCH4����һ�������·�����Ӧ��CH4��g��+CO2��g��?2CO��g��+2H2��g�������ƽ��ʱCH4��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ�������й�˵����ȷ���ǣ�������| A�� | ������Ӧ�ġ�H��0 | |
| B�� | ѹǿP1��P2��P3��P4 | |
| C�� | 1100��ʱ�÷�Ӧ��ƽ�ⳣ��ԼΪ1.64 | |
| D�� | ѹǿΪP4ʱ��y���v����v�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
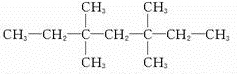
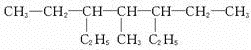
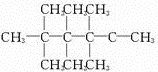
 ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C�ڷ�Ӧ�б���ԭ | B�� | S��KNO3�������˻�ԭ��Ӧ | ||
| C�� | CO2�Ƿ�Ӧ���������� | D�� | K2S��N2���Ƿ�Ӧ�Ļ�ԭ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
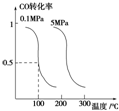 �о��Ϳ���CO2��CO�Ĵ��������ǻ�����������Դ����˫Ӯ�Ŀ��⣮
�о��Ϳ���CO2��CO�Ĵ��������ǻ�����������Դ����˫Ӯ�Ŀ��⣮�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com