
���� ��1���Ȼ��Ϊǿ�������Σ���Һ��笠�����Ϊ���������ӣ����ˮ����������������Ӵٽ�ˮ����ƽ��������У�������Ũ��������Һ�����ԣ�
��2����������ǿ�������Σ���Һ�������ӽ��ˮ����������������Ӵٽ�ˮ����ƽ��������У������Ӧ�������ε�ˮ�⣻
��3���������е�������ˮ��õ�����Һ��ʾ���ԣ��ܺͽ�����������Ӧ��
��� �⣺��1���Ȼ��Ϊǿ��������ˮ�������ԣ���Һ��笠�����Ϊ���������ӣ����ˮ����������������Ӵٽ�ˮ����ƽ��������У�������Ũ���������ӷ���ʽ��NH4++H2O?NH3•H2O+H+��
�ʴ�Ϊ��笠�����ˮ��ʹ��Һ�����ԣ�NH4++H2O?NH3•H2O+H+��
��2����������ǿ�������Σ���Һ�������ӽ��ˮ����������������Ӵٽ�ˮ����ƽ��������У���Ӧ�����ӷ���ʽΪ��Al3++3H2O?Al��OH��3+3H+�������Ӧ�������ε�ˮ�⣬��������Һ�м���ϡ��������ˮ�⣬
�ʴ�Ϊ��Al3++3H2O?Al��OH��3+3H+��ϡH2SO4��
��3��Al3+ˮ�������H+��ͽ�������Ӧ�������ḯʴ��Ͳ�����Բ��ܰ���������Һʢ����Ͳ�Ӧ������ĭ��������õIJ���Ͳ�ڣ�
�ʴ�Ϊ����������
���� ���⿼��ѧ���ε�ˮ��ԭ���Լ�ˮ��ԭ����Ӧ��֪ʶ������ѧ���Խ̲�֪ʶ������������ѶȲ���


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʵ���� | HA���ʵ���Ũ�ȣ�mol/L�� | NaOH���ʵ���Ũ�ȣ�mol/L�� | �����Һ��pH |
| �� | 0.2 | 0.2 | pH=a |
| �� | c | 0.2 | P H=7 |
| �� | 0.2 | 0.1 | pH��7 |
| �� | 0.1 | 0.1 | pH=9 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
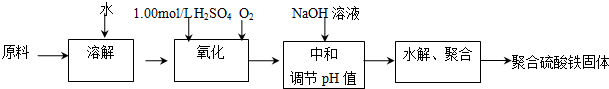
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ˮ�ܽⴿ���ܹ����ȥ���۵�Ч�� | |
| B�� | �����Ȼ�����Һʱ�μӼ���ϡ������Է�ֹ���������γ� | |
| C�� | ����狀Ͳ�ľ�һ��ʩ�õ�ũ�������ǿ��Ч | |
| D�� | �μ�أ���NaCl��Na2CO3��ʩ������ʯ����Խ��������ļ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Cl- | B�� | OH- | C�� | H+ | D�� | NH4+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ����Ʒ�� | �������ͯ���� | ����������� | �л������� |
| Ħ���� | �������� | ̼��� | �������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | X������ľ�ķ���� | |
| B�� | ����II�ķ�Ӧ��Na2SiO3+H2SO4�TH2SiO3�����壩+Na2SO4 | |
| C�� | ������е�ϡ�������CO2������ | |
| D�� | ���������ʵ������ɣ�һ�����������н��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ���������� | ���� | |
| A | ��װ��Fe��NO3��2��Һ���Թ��м���ϡH2SO4�����Թܿڹ۲쵽����ɫ���� | HNO3�ֽ�������NO2 |
| B | �������Һ�м���ϡH2SO4�����ȼ����ӣ���ȴ���ټ�������Cu��OH��2��Һ�����ȣ�û��ש��ɫ�������� | ����û��ˮ��������� |
| C | ����ˮ�Ҵ��м���ŨH2SO4��������170�����������ͨ������KMnO4��Һ����ɫ��ȥ | ʹ��Һ��ɫ����������ϩ |
| D | ��ˮ������Һ��ͨ������CO2 ������ɫ���� | �����˹������ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��1��ijϩ�������������ӳɷ�Ӧ�ɵõ��ṹ��ʽ����ͼ�������������ϩ�����ܵĽṹ��ʽ�ǣ�CH2=CHCH3CHCH3C��CH3��3����CH3��2C=CCH3C��CH3��3����CH3��2CHC=CH2C��CH3��3��
��1��ijϩ�������������ӳɷ�Ӧ�ɵõ��ṹ��ʽ����ͼ�������������ϩ�����ܵĽṹ��ʽ�ǣ�CH2=CHCH3CHCH3C��CH3��3����CH3��2C=CCH3C��CH3��3����CH3��2CHC=CH2C��CH3��3��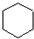 ��E��CH3CH3��
��E��CH3CH3��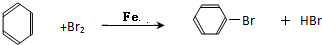 ��
���鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com