
����Ŀ���л��������ұ���G2762011���涨���Ѿ���SO2���ʹ����Ϊ0.25g��L1��ȡ300.00mL���Ѿƣ�ͨ���ʵ��ķ���ʹ����SO2ȫ���ݳ�����H2O2����ȫ������ΪH2SO4��Ȼ����0.0900mol��L��1NaOH����Һ���еζ���
��1���ζ�ǰ������ʱ��Ӧѡ��ͼ�е�___(�����)��


��2������50 mL�ζ��ܽ���ʵ�飬���ζ����е�Һ���ڿ̶���10�����������Һ������___(�����)��
a.��10mL b.��40mL c.��10 mL d.��40mL
��3�������ζ�ʵ���У���ѡ��___Ϊָʾ����ѡ���ָʾ��ʱ����жϷ�Ӧ����ζ��յ㣺___��
��4���ζ����յ�ʱ������NaOH��Һ25.00 mL�������Ѿ���SO2����Ϊ___g��L1���ζ��յ����ʱ���ӿ̶��ߣ�����������ʵ��ֵ___������ƫ��������ƫ����������Ӱ��������
���𰸡��� d ��̪ ���������һ�α���Һ����Һǡ�ñ��ɫ�����ڰ�������ޱ仯��˵������ζ��յ� 0.24 ƫ��
��������
��1����ʽ�ζ�����������Ϊ���������齺��������ʹ�����������ϣ���ָ������ѹ�齺�ܲ������ɣ�
��2������50 mL�ζ��ܽ���ʵ�飬�ζ��̶ܿ�50mL���»���δ֪����ļ�Һ��
��3����Һ��ʼ�����ԣ��ζ����������ԣ����÷�̪��ָʾ��������С������ɫ�仯�����ۺ죬�������ԣ�
��4��H2SO4~2NaOH��2n��H2SO4����V��H2SO4��= n��NaOH����V��NaOH������S�غ���㣻�ζ��յ����ʱ���ӿ̶��ߣ����¶�ȡNaOH��Һ�����ƫС��
��1��ʢ��NaOH��Һ�ĵζ���Ϊ��ʽ�ζ��ܣ���������Ϊ���������齺��������ʹ�����������ϣ���ָ������ѹ�齺�ܲ������ɣ���Ϊ�ۣ�
��2������50 mL�ζ��ܽ���ʵ�飬�ζ��̶ܿ�50mL���»���δ֪����ļ�Һ������ڵ�Һ���������40mL��
��3����Һ��ʼ�����ԣ��ζ����������ԣ����÷�̪��ָʾ��������С������ɫ�仯�����ۺ죬�������ԣ��ж��յ㷽��Ϊ���������һ�α���Һ����Һǡ�ñ��ɫ�����ڰ�������ޱ仯��˵������ζ��յ㣻
��4��H2SO4~2NaOH��2n��H2SO4����V��H2SO4��= n��NaOH����V��NaOH������n��H2SO4��=![]() =0.00375mol/L������Sԭ���غ㣬��SO2����=0.00375��64=0.24g/L���ζ��յ����ʱ���ӿ̶��ߣ����¶�ȡNaOH��Һ�����ƫС��������������ʵ���Ũ��ƫС�����������ĺ���ƫ�͡�
=0.00375mol/L������Sԭ���غ㣬��SO2����=0.00375��64=0.24g/L���ζ��յ����ʱ���ӿ̶��ߣ����¶�ȡNaOH��Һ�����ƫС��������������ʵ���Ũ��ƫС�����������ĺ���ƫ�͡�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ�����и���������ָ����Һ���ܴ����������( )
A.pH =1����Һ�У�NH4+��SO42����ClO����Na+
B.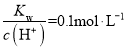 ����Һ�У�Na+��K+��MnO4����HCO3��
����Һ�У�Na+��K+��MnO4����HCO3��
C.0.1molL-1��Na2SO3��Һ�У�H+��K+��SO42����NO3��
D.����������Һ�У�Fe3+��Na+��Cl����SO42��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������ɴ�����Ⱦ����Ҫ���ʡ�
(1)�û���̿��ԭNO���йط�ӦΪ��C(s)��2NO(g)![]() N2(g)��CO2(g)��������ܱ������м���һ�����Ļ���̿��NO��T��ʱ����������ʼŨ�ȼ�10 min��20 min������ƽ��Ũ�������ʾ��
N2(g)��CO2(g)��������ܱ������м���һ�����Ļ���̿��NO��T��ʱ����������ʼŨ�ȼ�10 min��20 min������ƽ��Ũ�������ʾ��
Ũ��mol/L ʱ��min | NO | N2 | CO2 |
0 | 10 | 0 | 0 |
10 | 5 | 2.5 | 2.5 |
20 | 2 | 4 | 0.25 |
����10minʱ����ֻ�ı�ijһ����ʹƽ�ⷢ���ƶ���20minʱ���´ﵽƽ�⣬��ı��������____��
����20minʱ�������¶Ⱥ�������������ٳ���NO��N2��ʹ���ߵ�Ũ�Ⱦ�������ԭ������������ʱ��Ӧv��___v������������������������������
(2)��ҵ����N2��H2���Ʊ�NH3����ͬ�¶��£���������ͬ��������Ͷ����ͬ�ķ�Ӧ����з�Ӧ����ò�ͬ�¶�ʱƽ��������NH3�����ʵ���������ѹǿ������仯��ͼ��ʾ��
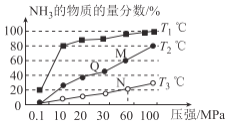
��M���v��_______Q���v������������������������������
��ͼ���������߶�Ӧ���¶ȷֱ�ΪT1��T2��T3�������¶���ߵ���____��
�����º��������£���˵����ӦN2(g)��3H2(g)![]() 2NH3(g)�ﵽƽ��״̬����____����ѡ����ĸ��
2NH3(g)�ﵽƽ��״̬����____����ѡ����ĸ��
A�� 2v(N2)��v(NH3) B��c2(NH3)/[c(N2)c3(H2)]���ֲ���
C����Ӧ���е�ѹǿ���ٷ����仯 D��3 molH��H�����ѵ�ͬʱ����2molN��H������
(3)NO2��������ƽ�⣺2NO2(g)![]() N2O4(g) ��H��0����һ��������NO2��N2O4��������������Եķ�ѹ����ѹ����ѹ�����ʵ��������������¹�ϵ v(NO2)��k1��p2(NO2)��v(N2O4)��k2��p(N2O4)����Ӧ�����������ѹ��ϵ��ͼ��ʾ��
N2O4(g) ��H��0����һ��������NO2��N2O4��������������Եķ�ѹ����ѹ����ѹ�����ʵ��������������¹�ϵ v(NO2)��k1��p2(NO2)��v(N2O4)��k2��p(N2O4)����Ӧ�����������ѹ��ϵ��ͼ��ʾ��
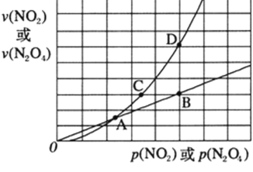
һ���¶��£�k1��k2��ƽ�ⳣ��Kp��ѹ��ƽ�ⳣ������ƽ���ѹ����ƽ��Ũ�ȼ��㣩��Ĺ�ϵ��k1��____������ͼ������У�ָ���ܱ�ʾ��Ӧ�ﵽƽ��״̬�ĵ���______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ճ�����������ĵ�ζ������Ҫ�Ļ���ԭ�ϣ����������䳣�����Σ���֪��25�棬Ka��CH3COOH��=1.69��10-5����
��1����������Һ�ʼ��Ե�ԭ����___��д���йص����ӷ���ʽ����
��2����CH3COONa��Һ������Ũ���ɴ�С��˳��Ϊ___����c��Bn+����ʾ��Ӧ����Ũ�ȣ���
��3�����ڴ�����Һ�ʹ�������Һ������˵����ȷ����___��
A��ϡ�ʹ�����Һ������ĵ���̶�����ϡ�ʹ�������Һ������Ƶ�ˮ��̶ȼ�С
B�������¶ȿ��Դٽ�������룬Ҳ���Դٽ�������ˮ��
C������ʹ����ƻ��Һ�У��������ƴ����Ƶ�ˮ�⡢������Ҳ���ƴ���ĵ���
D������ʹ����ƻ��Һ�У�����ٽ������Ƶ�ˮ�⡢������Ҳ�ٽ�����ĵ���
��4�����ʵ���Ũ�Ⱦ�Ϊ0.1mol/L��CH3COONa��CH3COOH��Һ�������ϣ�ע�����ǰ����Һ����仯���Բ��ƣ������Һ�е����й�ϵʽ��ȷ����___��
A��c��CH3COOH��+2c��H+��=c��CH3COO-��+2c��OH-��
B��c��Na+��+c��H+��=c��CH3COO-��+c��OH-��
C��c��CH3COO-��+c��CH3COOH��=0.1mol/L
��5������ʱ��������3����Һ������pH��С����___��
A��0.02molL1CH3COOH��0.02molL1NaOH��Һ��������Һ
B��0.01molL1CH3COOH��0.03molL1NaOH��Һ��������Һ
C��pH=2��CH3COOH��pH=12��NaOH��Һ��������Һ
��6����pH��ֽ�ڳ����·ֱ�ⶨ0.10mol/L�Ĵ�������Һ��0.10mol/L��̼������Һ����pH��CH3COONa��__pH��Na2CO3���������>������<������=����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����г�����4����Һ��������ڴ�����Һ��������������Һ���ܰ�ˮ����֪�ٺ͢ڵ�pHΪa���ۺܵ͢�pHΪb����![]() b
b![]() �������й۵�������
�������й۵�������
A.��![]() ʱ������Һ����ˮ�������
ʱ������Һ����ˮ�������![]() ����
����![]()
B.�����ٺ͢۷ֱ��ˮϡ��100������ϡ�ͺ�����Һ��pH֮����Ϊ14
C.����������Ģں͢۷ֱ����������۷�Ӧ�����ɵ��������߶�
D.�����ٺܵ͢������ϣ����Ϻ����Һ��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶���,��������AgCl�ֱ��������������,AgCl���ܽ���ɴ�С������˳����
��20 mL 0.01 mol/L KCl��Һ ��30 mL 0.02 mol/L CaCl2��Һ
��40 mL 0.03 mol/L HCl��Һ ��10 mL ����ˮ��50 mL 0.05 mol/L AgNO3��Һ
A. ������������������ B. ������������������
C. ������������������ D. ������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���0.1000 mol/L NaOH��Һ�ֱ�ζ�20. 00 mL 0.1000 mol/L �����20. 00 mL 0.1000 mol/L ������Һ���õ�2���ζ����ߣ�����ͼ��ʾ��
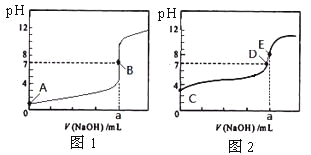
����HA��ʾ�ᣬ����˵����ȷ����
A. �ζ������������ͼ2
B. �ﵽB��D״̬ʱ������Һ������Ũ�Ⱦ�Ϊc(Na+)=C(A-)
C. �ﵽB��E״̬ʱ����Ӧ���ĵ�n(CH3COOH)>n(HCl)
D. ��0 mL<V(NaOH) <20. 00 mLʱ����Ӧ�����Һ�и�����Ũ���ɴ�С��˳���Ϊc(A��) >c(Na+)>c(H+) >c(OH��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NA���������ӵ�������ֵ������˵����ȷ����( )
A.��״���£�11.2 L Cl2����ˮ����Һ��Cl����ClO����HClO������֮��ΪNA
B.32.5 g FeCl3ˮ���γɵ�Fe(OH)3����������Ϊ0.2NA
C.1 mol PC13��1 mol 36C12��Ӧ�ﵽƽ��ʱ�������к�P��36C1����ĿΪ2NA
D.��Ӧ![]() +
+ ![]() ��
�� ![]() +
+ ![]() �У�ÿ����294g
�У�ÿ����294g ![]() �ͷŵ�������Ϊ3NA
�ͷŵ�������Ϊ3NA
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com