
【题目】化学是一门具有创造性的科学。下列事实不能直接体现这一说法的是( )
A.青蒿素的发现与合成B.水力发电
C.新型复合材料的发明D.“21世纪的金属”——钛的冶炼
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】某温度时,在2L密闭容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如右图所示,
由图中数据分析:
(1)该反应的化学方程式:_____________;
(2)反应开始至2min末,X的反应速率为_________;
(3)3min后图中曲线所表示的含义是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验是化学研究的基础,关于下列各实验装置图的叙述中,错误的是( ) 
A.装置①可用于检查装置的气密性
B.装置②可用于除去CO中混有的少量CO2
C.装置③可用于安全吸收极易溶于水的氯化氢来制盐酸
D.装置④可用于排空气收集CO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化铬晶体(CrCl3·6H2O)是一种重要的工业原料,工业上常用铬酸钠(Na2CrO4)来制备。实验室以红矾钠(Na2Cr2O7)为原料制备CrCl3·6H2O的流程如下:

已知:① Cr2O72-+H2O![]() 2CrO42-+2H+;
2CrO42-+2H+;
② CrCl3·6H2O不溶于乙醚,易溶于水、乙醇,易水解。
(1)写出碱溶发生反应的化学方程式____________________________________,所加40%NaOH不宜过量太多的原因是______________________________。
(2)还原时先加入过量CH3OH再加入10%HCl,生成CO2,写出该反应的离子方程式_________________,反应后从剩余溶液中分离出CH3OH的实验方法是_____________。
(3)使用下列用品来测定溶液的pH,合理的是_________(填字母)。
A.酚酞溶液 B.石蕊试纸 C.pH计
(4)请补充完整由过滤后得到的固体Cr(OH)3制备CrCl3·6H2O的实验方案:将过滤后所得的洁净固体 _______________________,蒸发浓缩,__________,过滤, ______________,低温干燥,得到CrCl3·6H2O(实验中可供选择的试剂:盐酸、硫酸、蒸馏水、乙醇、乙醚)。
(5)若取原料红矾钠26.2g,实验最终得到氯化铬晶体42.64g,则该实验的产率为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为探索铜跟浓硫酸的反应,用下图所示装置进行有关实验。

取a g Cu片、12mL 18mol/L浓H2SO4放入圆底烧瓶中加热,直到反应完毕,最后发现烧瓶中还有一定量的H2SO4和Cu剩余。请回答:
(1)请写出Cu与浓H2SO4反应的化学方程式___________________________________,装置E中试管D内盛品红溶液,当D中观察到_____________________时,说明C中气体集满,取下试管D,用酒精灯加热,观察到的现象是_____________________。
(2)装置B的作用是贮存多余的气体,B中放置的液体可以是_________________ (填字母)。
A.酸性KMnO4 B.饱和Na2S溶液 C.饱和NaHCO3溶液 D.饱和NaHSO3溶液
(3)下列药品中,能够证明反应后的烧瓶中有酸剩余的是___________。
A.KNO3晶体 B.NaHCO3溶液 C.Zn粉 D.BaCl2溶液
(4)该法制备硫酸铜溶液有诸多缺点,任意写出一条_______________________,可以用稀硫酸和废铜屑通过绿色方法制得纯净的硫酸铜溶液,写出一种制备方法_______________________(用方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于金属通性的叙述不正确的是( )
A. 在反应中金属原子易失去最外层上的电子
B. 金属单质只具有还原性,而不具有氧化性
C. 金属元素在化合物中不可能为负价
D. 金属单质都能与盐酸溶液发生置换反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用1L1.0mol·L-1的NaOH溶液吸收0.6molCO2,所得溶液中的CO32-和HCO3-的物质的量浓度之比约是( )
A.1∶3B.2∶1C.2∶3D.3∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示,装置Ⅰ为甲醇燃料电池(电解质溶液为KOH溶液),通过装置Ⅱ实现铁棒上镀铜。
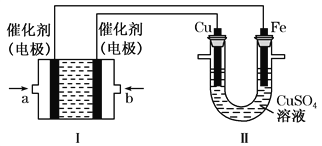
(1)b处应通入_____(填“CH3OH”或“O2”),a处电极上发生的电极反应式是___________________;
(2)电镀结束后,装置Ⅰ中溶液的pH______(填写“变大”“变小”或“不变”,下同),装置Ⅱ中Cu2+的物质的量浓度______________;
(3)若铜电极质量减小6.4 g,则消耗标况下的O2的体积为_____________________。
(4)若将装置I中电解质溶液换成硫酸溶液,则在工作过程中H+ 移向______电极(填“a”或“b”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.1 mol O2和1 mol N2所占的体积都约为22.4 L
B.H2的气体摩尔体积约为22.4 L
C.在标准状况下,1 mol H2和1 mol H2O所占的体积都约为22.4 L
D.在标准状况下,22.4 L由N2、N2O组成的混合气体中所含有的N的物质的量约2 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com