
����Ŀ�������ؾ��п�ͻ���Ԥ�����������ã���ϳ�·�����£�

��֪��
��1 mol G���������Na��NaOH��NaHCO3�����ʵ����ֱ�Ϊ3 mol��2 mol��1 mol��
��![]()
��
(R1��R2��R3Ϊ��������ԭ��)
��ش�
(1)B��C�ķ�Ӧ������__________��д����Ӧ�Ļ�ѧ����ʽ______________________��
(2)C��D��Ӧ�Ļ�ѧ����ʽ��_______________________________________________��
(3)E�ĺ˴Ź����������������壬E�к��еĹ�����������__________��
��֪E��G�ķ�Ӧ�����Ǽӳɷ�Ӧ��д����Ӧ�Ļ�ѧ����ʽ_____________________��
(4)�����й�����ȩ����������ȷ����__________��
a. ����ȩ����NaHCO3��Һ��Ӧ
b. ����ȩ����Ũ��ˮ����ȡ����Ӧ
c. 1 mol����ȩ�������3 mol H2�����ӳɷ�Ӧ
(5)д�����з�����������������ȩ��ͬ���칹��Ľṹ��ʽ___________________��
�ٱ����ϵ�һ����ȡ������2��
����Fe3+����ɫ
�ۺ���![]() �ṹ
�ṹ
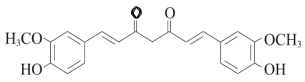
(6)�����صķ�������2��������ṹ��ʽ��__________��
(7)1��3������������Ҫ�Ļ������ʣ�������ɼ״����Ҵ�(�������Լ���ѡ)�ϳ���������ͼ���ϳ�·������ͼʾ�����£�__________________________________
CH2=CH2 ![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH
CH3CH2OH
���𰸡�ȡ����Ӧ BrCH2-CH2Br+2NaOH ![]() HOCH2-CH2OH+2NaBr HOCH2-CH2OH + O2
HOCH2-CH2OH+2NaBr HOCH2-CH2OH + O2![]() OHC-CHO + 2H2O ȩ�����Ȼ�
OHC-CHO + 2H2O ȩ�����Ȼ� 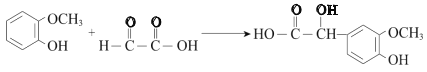 ac
ac ![]() ��
��![]() ��
��![]() ��
��![]()
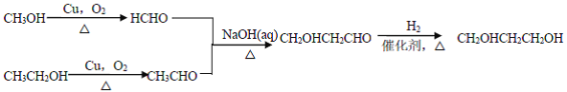
��������
��ϩ���巢���ӳɷ�Ӧ����BΪ![]() ,
,![]() ����
����![]() ,��G����1��
,��G����1��![]() ,
,![]() ���������
���������![]() ,��G������2��
,��G������2��![]() ,
,![]() ����
����![]() ,���H�Ľṹ����֪��,G��Ӧ����1�����ǻ�,����֪G�Ľṹ��ʽΪ
,���H�Ľṹ����֪��,G��Ӧ����1�����ǻ�,����֪G�Ľṹ��ʽΪ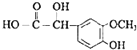 ,FΪ
,FΪ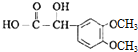 ,�Ա�G�Ľṹ��E�ķ���ʽ,����֪��EΪ
,�Ա�G�Ľṹ��E�ķ���ʽ,����֪��EΪ![]() ,��B����������ˮ��Һ�����������·���ˮ�ⷴӦ����CΪ
,��B����������ˮ��Һ�����������·���ˮ�ⷴӦ����CΪ![]() ,DΪ
,DΪ![]() ,D�в���ȩ������������E,J��һ�������·�����Ϣ�������ȷ�Ӧ����K������ȩ��Ϊ
,D�в���ȩ������������E,J��һ�������·�����Ϣ�������ȷ�Ӧ����K������ȩ��Ϊ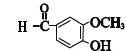 ,�����Ϣ
,�����Ϣ![]() �������صķ���ʽ,����֪�������صĽṹ��ʽΪ:
�������صķ���ʽ,����֪�������صĽṹ��ʽΪ: ,�ݴ˽��
,�ݴ˽��
��1�������������֪��BΪ![]() ��CΪ
��CΪ![]() ������B��C�ķ�Ӧ��BrCH2-CH2Br�ڼ��������µ�ȡ����Ӧ������ʽΪBrCH2-CH2Br+2NaOH
������B��C�ķ�Ӧ��BrCH2-CH2Br�ڼ��������µ�ȡ����Ӧ������ʽΪBrCH2-CH2Br+2NaOH ![]() HOCH2-CH2OH+2NaBr��
HOCH2-CH2OH+2NaBr��
�����Ϊ��ȡ����Ӧ�� BrCH2-CH2Br+2NaOH ![]() HOCH2-CH2OH+2NaBr��
HOCH2-CH2OH+2NaBr��
��2���ɷ�����֪DΪ![]() ������C��D��Ӧ�Ļ�ѧ����ʽ��HOCH2-CH2OH + O2
������C��D��Ӧ�Ļ�ѧ����ʽ��HOCH2-CH2OH + O2![]() OHC-CHO + 2H2O��
OHC-CHO + 2H2O��
�������HOCH2-CH2OH + O2![]() OHC-CHO + 2H2O��
OHC-CHO + 2H2O��
��3�����������������֪EΪ![]() �����Ժ��еĹ�����Ϊȩ�����Ȼ���E��G�ķ�Ӧ�����Ǽӳɷ�Ӧ����Ӧ�Ļ�ѧ����ʽΪ
�����Ժ��еĹ�����Ϊȩ�����Ȼ���E��G�ķ�Ӧ�����Ǽӳɷ�Ӧ����Ӧ�Ļ�ѧ����ʽΪ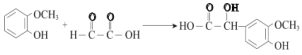 ��
��
�����Ϊ��ȩ�����Ȼ��� ��
��
��4������ȩΪ ��
��
a.����ȩ�в����Ȼ�,���Բ�����![]() ��Һ��Ӧ,�ʴ���
��Һ��Ӧ,�ʴ���
b.����ȩ���з��ǻ��������ӱ����ķ��ǻ���λ����ԭ��,��������Ũ��ˮ��������ȡ����Ӧ,����ȷ��
c.������ȩ�����������������ӳɷ�Ӧ,��![]() ����ȩ�������
����ȩ�������![]() �����ӳɷ�Ӧ,�ʴ���
�����ӳɷ�Ӧ,�ʴ���
�������a c��
��5�������������������ȩ��ͬ���칹��Ϊ��![]() ��
��![]() ��
��![]() ��
��![]() ��
��
�������![]() ��
��![]() ��
��![]() ��
��![]() ��
��
��6�������صķ�����ΪC21H26O6�������������Ľṹ��ʽΪ��![]() ��
��
�������![]() ��
��
��7��������ͼ����֪�۵���ʾ����֪�ɼ״����Ҵ��ϳ�1��3��������������ͼΪ��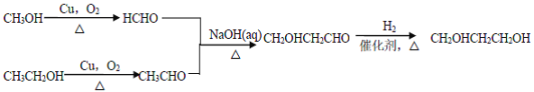 ��
��
�������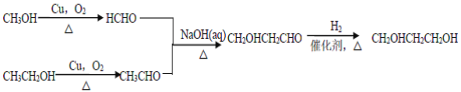 ��
��


 ��ĩ1�����ʽ���������ϵ�д�
��ĩ1�����ʽ���������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��WΪԭ������������������ֶ�����Ԫ��,����ZΪ����Ԫ��,X��WΪͬһ����Ԫ�ء�X��Z��W�γɵ����������ֱ�Ϊ�ס��ҡ�����x��y2��z��w�ֱ�ΪX��Y��Z��W�ĵ��ʣ����ǻ������ת����ϵ��ͼ��ʾ�������жϴ�����ǣ� ��

A. ��Ӧ�١��ڡ��۶�����������ԭ��Ӧ B. X��Y��Z��W����Ԫ���У�Y��ԭ�Ӱ뾶��С
C. Na�Ż�ʱ�����ü����� D. һ�������£�x���Ӧ���ɶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������NF3������ɫ��ζ�����壬�����ɰ��ͷ�ֱ�ӷ�Ӧ�õ���4NH3+3F2![]() NF3+3NH4F�������й�NF3��������ȷ����
NF3+3NH4F�������й�NF3��������ȷ����
A. NF3�����ӻ����� B. NF3�е�N��+3��
C. NF3�������Ա�F2ǿ D. NF3�Ļ�ԭ�Ա�NH3ǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�����ʵ�ֵ���

A. װ�âٿɼ��������鷢����ȥ��Ӧ�õ�������Ϊ��ϩ
B. װ�â��е�CuSO4��Һ�����ڳ�ȥ����
C. װ�â�a���к�ɫ�������ɣ�b��������֤��Xһ����H2
D. װ�âܿ�����ʵ������ȡ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������գ�
��![]() ��
��![]() ��
��![]() ��
��![]()
��![]() ��
��![]() ��
��![]() ��
�� ��
��
��
(1)�����л�������������Ʒ�Ӧ����________(����ţ���ͬ)������̼�����Ʒ�Ӧ����________������̼���Ʒ�Ӧ����____________��
(2)�����л���������ͬ���칹�����_____________(����ţ���ͬ)������ͬϵ�����______________������ͬ�����ʵ���_______________��
(3)��֪��ˮ������ȩ������ֻ����ʹ��һ���Լ����鴿���ʢ��е�̼̼˫�������Լ�Ϊ____��
(4)�������ֻ��̼������Ԫ�أ���ϵͳ����Ϊ________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ԭ�ӻ��ȡ������ܡ����ܵĵ�λ����kJmol��1

������˵����ȷ����
A. Na��s����Cl2��g����Ӧ����1mol NaCl��s���ų�������Ϊ556.1kJ
B. Si��s��+2Cl2��g���TSiCl4��g����H=��602kJmol��1
C. �ӱ��п��Կ������Ȼ��Ƶ��۵�Ⱦ�����
D. �ӱ������ݿ��Կ��������뾶Խ������������Ӽ�Խ���������ۼ�ȴԽǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ش��������⣺
(1)���������ܵ��������ڵ���ʵ�����_______��
A.��̬�Ȼ�þ(MgCl2) B.Һ̬�Ȼ�þ(MgCl2)
C.�Ȼ�����Һ D.��
(2)д������������ˮ��Һ�еĵ��뷽��ʽ:
��Na2CO3______________________;
��H2SO4_____________________;
��NH3��H2O_______________��
(3)����˵�ɽ���������KHSO4��NaHCO3��Ϊͬһ�������Ϊ����������Ҫ��_____������˵�ɽ���������KHSO4��H2SO4��Ϊͬһ�������Ϊ����������Ҫ��_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪ����250mL0.2mol��L��1Na2CO3����Һ��ʾ��ͼ��
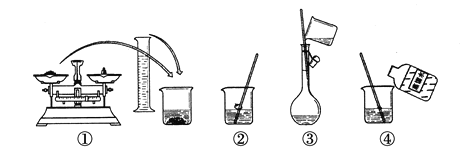
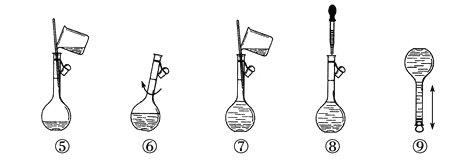
�ش��������⣺
��1��������ƿ��ʹ�÷����У����в�������ȷ����___(����ĸ)��
A��ʹ������ƿǰ������Ƿ�©ˮ
B������ƿ������ˮϴ�������ô�����Һ��ϴ
C��������Һʱ����������ǹ��壬�ѳƺõ�������ֽ��С�ĵ�������ƿ�У�������������ˮ���ӽ��̶���1��2 cm�����ý�ͷ�ιܵμ�����ˮ���̶���
D��������Һʱ�����������Һ�壬����Ͳ��ȡ������ֱ�ӵ�������ƿ�У�������������ˮ���ӽ��̶���1��2 cm�����ý�ͷ�ιܵμ�����ˮ���̶���
E���Ǻ�ƿ������ʳָ��סƿ��������һֻ����סƿ�ף�������ƿ��ת��ҡ�����
��2�����гƵ�Na2CO3___g��
��3���������ڢڡ��������е����÷ֱ���___��____��
��4�������������������������ҺŨ���к�Ӱ�죿(����ƫ������ƫ����������Ӱ����)
A��ijͬѧ�ڵڢಽ�۲�Һ��ʱ����____��
B���ڵڢݲ�����������Һ����������ƿ��____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������̫���ܵ���е������ྦྷ��̫���ܵ�ء�GaAs̫���ܵ�ؼ�ͭ��������Ĥ̫���ܵ�صȡ���ش��������⣺
��1����̬��ԭ�ӵļ۵����Ų�ʽΪ___��H2O�ķе����H2Se�ķе�(��42��)����ԭ����___��
��2����֪GaCl3�����۵�Ϊ77.9�棬�е�Ϊ201.3�棬GaCl3Ʒ������Ϊ____��
��3��Na3AsO4�������ӵĿռ乹��Ϊ_____��Asԭ�Ӳ�ȡ_____�ӻ���
��4��������CuO����ת��ΪCu2O���Դ�ԭ�ӽṹ�ǶȽ���ԭ��_____��
��5��п��ͭλ��ͬһ���ڡ���п�ľ����ṹ��ͼ��ʾ��S2����Χ�Ⱦ����������Zn2+����Ϊ____���������߳�Ϊdpm������п���ܶ�Ϊ____g��cm��3(���ؼ�)��

�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com