
����Ŀ����ͼΪ����250mL0.2mol��L��1Na2CO3����Һ��ʾ��ͼ��
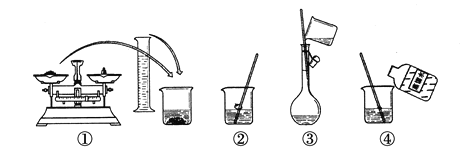
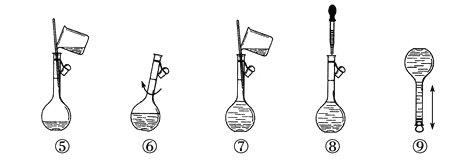
�ش��������⣺
��1��������ƿ��ʹ�÷����У����в�������ȷ����___(����ĸ)��
A��ʹ������ƿǰ������Ƿ�©ˮ
B������ƿ������ˮϴ�������ô�����Һ��ϴ
C��������Һʱ����������ǹ��壬�ѳƺõ�������ֽ��С�ĵ�������ƿ�У�������������ˮ���ӽ��̶���1��2 cm�����ý�ͷ�ιܵμ�����ˮ���̶���
D��������Һʱ�����������Һ�壬����Ͳ��ȡ������ֱ�ӵ�������ƿ�У�������������ˮ���ӽ��̶���1��2 cm�����ý�ͷ�ιܵμ�����ˮ���̶���
E���Ǻ�ƿ������ʳָ��סƿ��������һֻ����סƿ�ף�������ƿ��ת��ҡ�����
��2�����гƵ�Na2CO3___g��
��3���������ڢڡ��������е����÷ֱ���___��____��
��4�������������������������ҺŨ���к�Ӱ�죿(����ƫ������ƫ����������Ӱ����)
A��ijͬѧ�ڵڢಽ�۲�Һ��ʱ����____��
B���ڵڢݲ�����������Һ����������ƿ��____��
���𰸡�BCD 5.3g ���裬�����ܽ� ���� ƫ�� ƫ��
��������
(1)��������ƿ�Ľṹ��ʹ�÷������������Һ��һ�㲽������жϣ�
(2)�������ʵ�����m=nM=cVM���㣻
(3)�ܽ����ʱ��Ҫ�ò��������裬ת����Һʱ��Ҫ�ò�����������
(4)�������������ʵ����ʵ��������Һ�������Ӱ�죬����c=![]() �����жϡ�
�����жϡ�
(1)A������ƿ�ڲ������ӣ�ʹ������ƿǰӦ�ü����Ƿ�©ˮ����A��ȷ��B������ƿ��ˮϴ�������ô�����Һ��ϴ�������Ӱ��������Һ��Ũ�ȣ���B����C��������Һʱ����������ǹ��壬Ӧ�����ձ����ܽ⣬��ҩƷ��ȫ�ܽ�ָ������£��ٰ���ҺС�ĵ�������ƿ�У�������ˮ���ӽ��̶���1��2cm�����ý�ͷ�ιܼ�����ˮ���̶��ߣ����ܰѳƺõĹ�����ֽ����������ƿ�У���C����D��������Һʱ����������Һ�壬Ӧ�����ձ���ϡ�ͣ���ҩƷ��ȫ�ܽ�ָ������£��ٰ���ҺС�ĵ�������ƿ�У�������ˮ���ӽ��̶���1��2cm�����ý�ͷ�ιܼ�����ˮ���̶��ߣ����ܰ�Һ��ҩƷֱ��������������ƿ�У���D����E���Ǻ�ƿ������ʳָ��סƿ������һֻ����סƿ�ף�������ƿ������ת��Σ�ҡ�ȣ���E��ȷ������ȷ����BCD���ʴ�Ϊ��BCD��
(2)����0.2molL-1Na2CO3��Һ250mL��ҪNa2CO3������Ϊ��0.25L��0.2mol/L��106g/mol=5.3g���ʴ�Ϊ��5.3��
(3)���������ܽ����ʱ����Ϊ�˼����ܽ⣬��������ã�ת��ʱ�����������ã�
�ʴ�Ϊ�����裬�����ܽ⣻������
(4)A��ijͬѧ�ڵڢಽ�۲�Һ��ʱ���ӣ�������Һ�����ƫ��������ҺŨ��ƫ�ͣ��ʴ�Ϊ��ƫ�ͣ�
B���ڲ�����в���������Һ����������ƿ�⣬�������ʵ����ʵ���ƫС��Ũ��ƫ�ͣ��ʴ�Ϊ��ƫ�͡�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ѧ���ݣ��ش��������⣺
��ijͬѧ����Ӱ����������Ը��������Һ��Ӧ�������ص��о������������Ը�����صķ�ӦΪ��2KMnO4+5H2C2O4+3H2SO4��K2SO4+2MnSO4+10CO2��+8H2O�������£���֧�Թֱܷ��Ţٺ͢ڣ�ʵ���������£�
ʵ����� | �� | �� |
�����Լ� | 4 mL 0.01mol/L���� KMnO4��Һ 2 mL 0.1mol/L H2C2O4��Һ | 4 mL 0.01mol/L���� KMnO4��Һ 2 mL 0.1mol/L H2C2O4��Һ һ���ƶ������MnSO4���� |
��ɫʱ��/s | 116 | 6 |
�Թܢ���KMnO4��Һ��ɫ�����ʿ�ʼʮ�ֻ�����һ��ʱ���ͻȻ�ӿ졣
��ش�
(1)��ʵ�������___________________________________________________________��
(2)ʵ���ѡ��MnSO4���������MnCl2�����ԭ����____________________________��
(3)��ͬѧΪʹʵ��������ܣ����Թܢ�����������ʵ�飬��Ԥ����ɫʱ��ԼΪ_____��
ʵ����� | �� |
�����Լ� | 4 mL 0.01mol/L���� KMnO4��Һ 2 mL 0.1mol/L H2C2O4��Һ һ���ƶ������Na2SO4���� |
��ɫʱ��/s |
�ζ�����һ����Ҫ�Ķ�������������Ӧ�÷�Χ�ܹ㡣ij���г������۵�һ��ʳ�þ����ΰ�װ���������²���˵����
��Ʒ�ȼ� | һ�� |
���� | ʳ�Ρ������(KIO3)������� |
�⺬��(��I��) | 20��50 mg��kg��1 |
��֪��IO3����5I����6H�� = 3I2��3H2O��I2��2S2O32- = 2I����S4O62-ijѧ����ⶨʳ�þ����εĵ⺬�����䲽��Ϊ
a��ȷ��ȡW gʳ�Σ�����������ˮʹ����ȫ�ܽ�
b����ϡ�����ữ������Һ����������KI��Һ��ʹKIO3��KI��Ӧ��ȫ
c������ָʾ������μ������ʵ���Ũ��Ϊ2.0��10/span>��3 mol��L��1��Na2S2O3��Һ10.0 mL��ǡ�÷�Ӧ��ȫ
(4)c�м����ָʾ����ѡ��_________��ǡ����ȫ��Ӧʱ��������_______________��
(5)������b�ڿ�������ʱ������������ղⶨ�IJⶨʳ�þ������еĵĵ⺬����__________(����ƫ��������ƫ��������û��Ӱ����)��
(6)��������ʵ��Ͱ�װ˵�����������ʳ�þ����εĵ⺬����(�Ժ�W�Ĵ���ʽ��ʾ)________mg��kg��1(������������������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ؾ��п�ͻ���Ԥ�����������ã���ϳ�·�����£�

��֪��
��1 mol G���������Na��NaOH��NaHCO3�����ʵ����ֱ�Ϊ3 mol��2 mol��1 mol��
��![]()
��
(R1��R2��R3Ϊ��������ԭ��)
��ش�
(1)B��C�ķ�Ӧ������__________��д����Ӧ�Ļ�ѧ����ʽ______________________��
(2)C��D��Ӧ�Ļ�ѧ����ʽ��_______________________________________________��
(3)E�ĺ˴Ź����������������壬E�к��еĹ�����������__________��
��֪E��G�ķ�Ӧ�����Ǽӳɷ�Ӧ��д����Ӧ�Ļ�ѧ����ʽ_____________________��
(4)�����й�����ȩ����������ȷ����__________��
a. ����ȩ����NaHCO3��Һ��Ӧ
b. ����ȩ����Ũ��ˮ����ȡ����Ӧ
c. 1 mol����ȩ�������3 mol H2�����ӳɷ�Ӧ
(5)д�����з�����������������ȩ��ͬ���칹��Ľṹ��ʽ___________________��
�ٱ����ϵ�һ����ȡ������2��
����Fe3+����ɫ
�ۺ���![]() �ṹ
�ṹ
(6)�����صķ�������2��������ṹ��ʽ��__________��
(7)1��3������������Ҫ�Ļ������ʣ�������ɼ״����Ҵ�(�������Լ���ѡ)�ϳ���������ͼ���ϳ�·������ͼʾ�����£�__________________________________
CH2=CH2 ![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH
CH3CH2OH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���״���һ�ֿ�������Դ����CO2�Ʊ��״��Ĺ��̿����漰�ķ�Ӧ���£�
��Ӧ��CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ��H1=-49.58kJ��mol-1
CH3OH(g)+H2O(g) ��H1=-49.58kJ��mol-1
��Ӧ��CO2(g)+H2(g)![]() CO(g)+H2O(g) ��H2
CO(g)+H2O(g) ��H2
��Ӧ��CO(g)+2H2(g)![]() CH3OH(g) ��H3=-90.77kJ��mol-1
CH3OH(g) ��H3=-90.77kJ��mol-1
�ش��������⣺
(1)��Ӧ��ġ�H2=_________________��
(2)��Ӧ���ܹ��Է����е�������_______________(�����ϵ��¶��� ���ϸ��¶��������κ��¶��� )��
(3)���£������ܱ������У����ڷ�Ӧ������˵������˵���÷�Ӧ�ﵽ��ѧƽ��״̬����______��
A�����������ܶȲ��ٱ仯 B����������ƽ����Է����������ٱ仯
C��CO2��H2��CH3OH��H2O�����ʵ���֮��Ϊ1��3��1��1
D���״��İٷֺ������ٱ仯
(4)���ڷ�Ӧ��ͬ�¶ȶ�CO2��ת���ʼ�������Ч��Ӱ����ͼ��ʾ�������й�˵������ȷ����__________��

A�������������䣬����ʹ�ô�������250��ʱCO2��ƽ��ת���ʿ���λ��M1
B���¶ȵ���250 ��ʱ�����¶����״��IJ�������
C��M ��ʱƽ�ⳣ����N��ʱƽ�ⳣ����
D��ʵ�ʷ�ӦӦ�������ڽϵ͵��¶��½��У������CO2��ת����
(5)��֪����������20���µ�Ksp���£��Իش��������⣺
��ѧʽ | AgCl | AgBr | AgI | Ag2S | Ag2CrO4 |
��ɫ | ��ɫ | dz��ɫ | ��ɫ | ��ɫ | ��ɫ |
Ksp | 1.8��10-10 | 5.4��10-13 | 8.3��10-17 | 6.3��10-50 | 2.0��10-12 |
��20��ʱ�������������α�����Һ�У�Ag+���ʵ���Ũ�ɴ�С��˳����____________��
����BaCl2��Һ�м���AgNO3��KBr�������ֳ�������ʱc(Br-)/c(Cl-)=________________��
�� �ⶨˮ�����Ȼ���ĺ��������ñ������������еζ����ζ�ʱ��Ӧ�����ָʾ����____��
A.KBr B��KI C��K2S D��K2CrO4
(6)��֪25��ʱKsp[Mg(OH)2]=5.6��10-12��Ksp[Cu(OH)2]=2.2��10-20��Ksp[Fe(OH)3]=4.0��10-38��Ksp[Al(OH)3]=1.1��10-33��
����25���£���Ũ�Ⱦ�Ϊ0.1 mol��L-1��AlCl3��CuCl2�����Һ����μ��백ˮ��������______________����(�ѧʽ)��
����Һ��ij�������ʵ���Ũ�ȵ���1.0��10-5 mol��L-1ʱ������Ϊ�ѳ�����ȫ������һ��Ũ�ȵ�AlCl3��FeCl3�Ļ����Һ����μ��백ˮ����Fe3+�պ���ȫ����ʱ���ⶨc(Al3+)=0.2mol��L-1����ʱ���ó�����___________(������������������������)Al(OH)3������д��������̡�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾһЩ�����е�ijЩ�ṹ����ش��������⣺

(1)�������ʯ����(������ĸ����ͬ)________������ÿ��̼ԭ����________��̼ԭ������Ҿ�����ȡ����ʯ����________���塣
(2)����ʯī����________��ÿ����������ռ�е�̼ԭ����ƽ��Ϊ________����
(3)����NaCl����________��ÿ��Na����Χ��������Ҿ�����ȵ�Na����________����
(4)����CsCl����________��������________���壬ÿ��Cs����________��Cl�����ڡ�
(5)�����ɱ�����________��������________���壬ÿ��CO2������________��CO2���ӽ��ڡ�
(6)��֪ʯī��̼̼���ļ����Ƚ��ʯ��̼̼���ļ����̣����������������۵��ɸߵ��͵�����˳��Ϊ______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ԭ�ӽṹģ�͵��ݱ�ͼ���������з�����ʷ�ݱ�˳���һ��������

A. ��1����3����2����4�� B. ��1����2����3����4��
C. ��1����4����3����2�� D. ��1����3����4����2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ں��º��ݵ������н��з�ӦN2(g)��3H2(g) ![]() 2NH3(g)��������Ũ����0.1 mol��L-1����0.06 mol��L-1��2 s����ô��0.06 mol��L-1����0.024 mol��L-1��Ҫ�ķ�Ӧʱ��Ϊ
2NH3(g)��������Ũ����0.1 mol��L-1����0.06 mol��L-1��2 s����ô��0.06 mol��L-1����0.024 mol��L-1��Ҫ�ķ�Ӧʱ��Ϊ
A. ����1.8 s B. ����1.2 s C. ����1.8 s D. ��1.8 s
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������� 0.1mol/L��H2A��Һ��H2A��HA-��A2-��������ռ���ʵ����������ֲ�ϵ������pH�仯�Ĺ�ϵ��ͼ��ʾ�����б�������ȷ����

A. HA-![]() H+ + A2- K=10-4.2
H+ + A2- K=10-4.2
B. �� 0.1mol/L NaHA ��Һ�У�������Ũ�ȴ�С��ϵΪ��c(Na+)��c(HA-)��c(H+)��c(A2-)��c(OH-)
C. ��֪25��ʱHF��Ka=10-3.45��������H2A����Һ��������NaF��Һ�У������ķ�ӦΪ��H2A+F���T HF+HA��
D. �������ʵ�����NaHA��Na2A����ˮ�У�������ҺpHǡ��Ϊ4.2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̽��CO2��CH4�ķ�Ӧʹ��ת��ΪCO��H2���Լ���ȼ��Σ������������ЧӦ������Ҫ���塣�ش���������
(1)��֪����CH4(g)+H2O(g)![]() CO(g)+3H2(g) ��H1=+206.1kJ��mol��1
CO(g)+3H2(g) ��H1=+206.1kJ��mol��1
��2H2(g)+CO(g)![]() CH3OH(1) ��H2=��128.3kJ��mol��1
CH3OH(1) ��H2=��128.3kJ��mol��1
��2H2(g)+O2(g)![]() 2H2O(g) ��H3=��483.6kJ��mol��1
2H2O(g) ��H3=��483.6kJ��mol��1
25��ʱ���ں��ʵĴ��������£����ü��������һ���ϳ�Һ̬�״����Ȼ�ѧ����ʽΪ______________________��
(2)��ij�ܱպ���������ͨ�����ʵ���Ũ�Ⱦ�Ϊ0.1mol��L��1��CH4��CO2����һ�������·�����ӦCH4(g)+CO2(g)![]() 2CO(g)+2H2(g)�����CH4��ƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��
2CO(g)+2H2(g)�����CH4��ƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��

�ٹ�ҵ����ʱһ���ѡ����P4��1250�������½��з�Ӧ���������ԭ��______________________��
����ѹǿΪP4��1100��������£��÷�Ӧ��5minʱ�ﵽƽ���X����0-5min�ڣ���CO��ʾ�÷�Ӧƽ������Ϊ___________�����¶��£���Ӧ��ƽ�ⳣ��Ϊ___________(����3λ��Ч����)��
(3)��ҵ����CO��H2��ȡ�״���Ӧ����ʽΪ2H2(g)+CO(g)![]() CH3OH(g)�����ڸúϳɷ�Ӧ����ͨ���CO�����ʵ���һ������ͼΪ4��Ͷ�ϱ�[n(CO)�Un(H2)�ֱ�Ϊ5�U7��10�U17��5�U9��1�U2]ʱ����Ӧ�¶ȶ�COƽ��ת���ʵ�Ӱ�����ߡ�
CH3OH(g)�����ڸúϳɷ�Ӧ����ͨ���CO�����ʵ���һ������ͼΪ4��Ͷ�ϱ�[n(CO)�Un(H2)�ֱ�Ϊ5�U7��10�U17��5�U9��1�U2]ʱ����Ӧ�¶ȶ�COƽ��ת���ʵ�Ӱ�����ߡ�

������b��Ӧ��Ͷ�ϱ���___________
�ڵ���Ӧ������a��b��c��Ӧ��Ͷ�ϱ��´ﵽ��ͬ��ƽ��ת����ʱ����Ӧ�ķ�Ӧ�¶Ⱥ�Ͷ�ϱȵĹ�ϵ��___________��
��Ͷ�ϱ�Ϊ10�U17��Ӧ�¶�ΪT1ʱ��ƽ����������CO�����ʵ�������Ϊ___________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com