
【题目】(1)
① 欲使蛋白质从水溶液中析出而又不改变它的主要性质,应加入________(填字母)。
a. 福尔马林 b. 饱和硫酸钠溶液 c. 硫酸铜溶液
② 鉴别苯和甲苯的方法或试剂是________(填字母)。
a. 浓溴水 b. 酸化的KMnO4溶液 c. 在空气中点燃
③ 下列化合物中,常温常压呈液态的是________(填字母)。
a. 甲醇 b. 乙炔 c. 丙烯
(2) 制备聚酯玻璃钢需要下列四种物质:
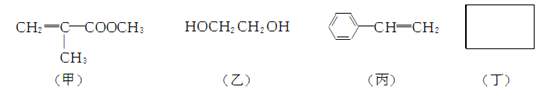
① 甲中不含氧原子的官能团是________(填名称)。
② 淀粉通过下列转化可以得到乙(其中A~D均为有机物):
 A的化学式是________,C→D的反应类型是________。
A的化学式是________,C→D的反应类型是________。
③ 丙发生加聚反应的生成物为________(写结构简式)。
④ 化合物丁仅含碳、氢、氧三种元素,相对分子质量为110。丁与FeCl3溶液作用显紫色,且丁分子中烃基上的一氯取代物只有一种。则丁的结构简式为________。
(3) A~F的转化关系如下(已知A分子中无甲基):
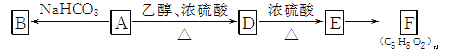
① 有机物A的相对分子质量为90,9 g A和足量Na反应,生成2.24 L H2(标准状况),则A的分子式为________。
② A缩聚生成高分子化合物的结构简式为________。
③ 由E生成F的反应类型是________。
④ 由D生成E的化学方程式为________。
⑤ 写出与A具有相同官能团的A的同分异构体的结构简式:________。
【答案】 b b a 碳碳双键 C6H12O6 加成反应 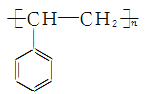
![]() C3H6O3
C3H6O3 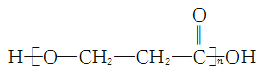 加聚反应 HOCH2CH2COOCH2CH3
加聚反应 HOCH2CH2COOCH2CH3![]() CH2==CHCOOCH2CH3+H2O
CH2==CHCOOCH2CH3+H2O 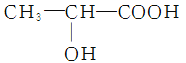
【解析】(1) ①a.福尔马林能使蛋白质发生变性,故a错误;b.饱和硫酸钠溶液能使蛋白质发生盐析,故b正确;c.硫酸铜溶液能使蛋白质发生变性,故c错误,故答案为b;
②苯与甲苯均不能使溴水褪色,燃烧均有浓厚的黑烟,苯不使能使酸化的KMnO4溶液褪色,而甲苯能使酸化的KMnO4溶液褪色,故答案为b;
③甲醇在常温下为液体,乙炔、乙烯在常温下都是气态,故答案为a;
(2)①甲中含C=C和-COOC两种官能团,则不含氧的官能团为碳碳双键;
②淀粉水解生成A葡萄糖,A发生酒化反应生成B乙醇,B发生消去反应生成C为乙烯,C发生加成反应生成D,则X为Br2/CCl4溶液,最后D水解生成乙,则A的分子式为C6H12O6,C→D的反应类型是加成反应;
③丙中含碳碳双键,则加聚产物的结构简式为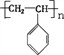 ;
;
④化合物丁含碳、氢、氧三种元素,相对分子质量为110,丁与FeCl3溶液作用显现特有的紫色,则含苯酚结构,110-12×6-16-6=16,则还含1个O原子,且丁分子中苯环上的一氯代物只有一种,其结构对称,应为对二苯酚,丁的结构简式为![]() ;
;
(3)①由上述分析可知,A的分子式为C3H6O3;
②A为HOCH2CH2COOH,缩聚生成高分子化合物的结构简式为![]() ;
;
③由E生成F的反应类型是加聚反应;
④由D直接生成E的化学方程式为HOCH2CH2COOCH2CH3![]() CH2==CHCOOCH2CH3+H2O;
CH2==CHCOOCH2CH3+H2O;
⑤与A具有相同官能团的A的同分异构体的结构简式为: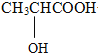 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】在一体积可变的密闭容器中,加入一定量的X、Y、Z,发生反应mX(g)+nY(g)![]() pZ(g) △H=Q kJ/mol。反应达到平衡后,Y的物质的量浓度与温度、容器体积的关系如下表所示。
pZ(g) △H=Q kJ/mol。反应达到平衡后,Y的物质的量浓度与温度、容器体积的关系如下表所示。

下列说法不正确的是
A. m+n>p
B. Q <0
C. 体积不变,温度升高,平衡向逆反应方向移动
D. 温度不变,压强增大,Y的质量分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是
A. 对平衡体系H2(g)+I2(g)![]() 2HI(g)加压后,混合气体的颜色加深
2HI(g)加压后,混合气体的颜色加深
B. 用稀盐酸洗涤AgCl沉淀比用等体积的蒸馏水洗涤损失的AgCl少
C. 实验室可用排饱和食盐水的方法收集氯气
D. 工业合成三氧化硫的过程中使用过量的氧气,以提高二氧化硫的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ciprofibrate是一种降血脂的药物,其结构如图所示: ,某实验小组以苯酚和化合物A为原料合成Ciprofibrate的路线图如下:
,某实验小组以苯酚和化合物A为原料合成Ciprofibrate的路线图如下:

已知:I. 
Ⅱ. 
Ⅲ.化合物A的分子式为C3H6O,且1H-NMR谱显示只有1种峰
请回答下列问题:
(1)反应①的反应类型是______,C中的官能团有______(填名称)。
(2)B的化学名称为_________。
(3)下列关于有机物D说法正确的是________(填字母代号)。
a.有机物D中的所有原子有可能在同一个平面上
b.1molD与足量溴水反应,可消耗2molBr2
c.常温下,有机物D的水溶性很好
d.有机物D能与Na2CO3溶液反应
(4)由C、D生成E的化学方程式为________________。
(5)有机物![]() 的某同系物的分子式为C10H12O2,写出分子式为C10H12O2且符合下列条件的所有有机物的结构简式_______________。
的某同系物的分子式为C10H12O2,写出分子式为C10H12O2且符合下列条件的所有有机物的结构简式_______________。
a.分子含苯环,1H-NMR谱显示只有4种峰
b.能发生银镜反应
c.与FeCl3溶液不会发生显色反应
(6)已知:① ;
;
②苯环上有甲基时,新取代基主要取代在邻位或对位,有醛基时主要取代在间位。请写出以甲苯为原料,合成![]() 的流程图,其它无机试剂任选。
的流程图,其它无机试剂任选。
(合成路线常用的表示方式为:![]() )_______________
)_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
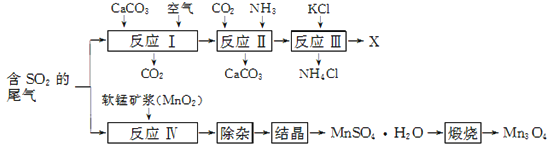
【题目】Mn3O4是生产软磁铁氧体材料的主要原料。以硫酸工业的尾气联合制备化肥X和Mn3O4的工艺流程如下:
请回答下列问题:
(1) 几种盐的溶解度见下如图。化肥X的化学式为________;为获得固体X,加入KCl溶液后需对混合溶液进行蒸发浓缩,当析出大量晶体后,应________(填操作名称),再洗涤、干燥晶体。
(2) 检验X样品是否含有氯化物杂质的实验操作是________。
(3) 如图是隔绝空气条件煅烧MnSO4·H2O时剩余固体质量与温度的变化曲线,请写出A→B的化学方程式:____________________。
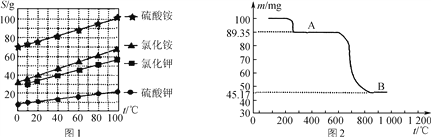
(4) 为了测定产品中Mn3O4的纯度,取2.500 g样品与浓盐酸共热(杂质不与盐酸反应),将产生的气体通入足量淀粉碘化钾溶液中,稀释至250 mL,从中取25.00 mL用0.100 0 mol·L-1 Na2S2O3标准溶液滴定至终点时,消耗20.00 mL标准溶液(2Na2S2O3 +I2===2NaI+Na2S4O6)。
① 样品与浓盐酸发生反应的离子方程式为________。
② 该样品的纯度为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为解决日益加剧的温室效应等问题,科学家正在研究建立如下图所示的二氧化碳新循环体系:
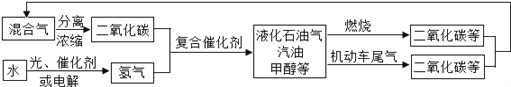
上述关系图能反映的化学观点或化学思想有:( )
①化学变化中元素种类是不变的;②燃烧时化学能可以转化为热能和光能;
③光能或电能可以转化为化学能;④无机物和有机物可以相互转化;
⑤二氧化碳可成为一种重要的资源。
A. ①②③④ B. ①②③⑤ C. ①②④⑤ D. ①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】K2Cr2O7是一种橙红色固体,可用于火柴制造、电镀、有机合成等方面。用某酸性废液(主要含Cr3+、还含有少量Fe2+、Fe3+和Al3+等)制备的流程如下:

已知:H++CrO2-+H2O![]() Cr(OH)3
Cr(OH)3![]() Cr3++3OH-
Cr3++3OH-
回答下列问题:
(1)沉淀A的主要成分是_____________(填化学式,下同),流程中的X是__________。
(2)滤液Ⅰ中铬元素的存在形式主要是_____________(填离子符号)。
(3)操作是向滤液中加入稀硫酸调PH至一定范围。在酸性环境中CrO42-转化为Cr2O72-,溶液变为橙红色,该转化的离子方程式是__________;若PH高于此范围,造成的影响是__________。
(4)操作②是向Na2Cr2O7溶液中加入KCl固体后得到K2Cr2O7,说明相同温度下,在水中的溶解度:Na2Cr2O7______________ K2Cr2O7(填“>”、“<”或“=”)。
(5)PbO2可直接将溶液中的Cr3+氧化成Cr2O72-,该反应的离子方程式是__________。
(6)K2Cr2O7可用来测定溶液中Fe2+的含量,还原产物为Cr3+。若1L FeSO4溶液与100mL 0.1mol/L K2Cr2O7溶液恰好完全反应,则c(FeSO4)=___________mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A(g)+B(g)![]() C(g)+D(g) 反应的平衡常数和温度的关系如下:
C(g)+D(g) 反应的平衡常数和温度的关系如下:
温度/℃ | 700 | 800 | 830 | 1000 | 1200 |
平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
完成下列填空:
(1)该反应的平衡常数表达式K=______,该反应为_____反应(选填“ 吸热”、“放热”)。当反应达到平衡时,升高温度,A的转化率_____(选填“增大”、“减小”或“不变”)。
(2)830℃时,向一个5L的密闭容器中充入0.20mol的A和0.80mol的B,如反应初始6s内A的平均反应速率v(A)=0.003mol/(L·s),则6s时c(A)=______mol/L,C的物质的量为____mol.
(3)一定条件下,向体积为2L的恒容密闭容器中充入1molA(g)和3molB(g),判断该反应达到平衡状态的依据是___________。
a.c(A)=c(C) b.容器中压强不变
c.混合气体的平均相对分子质量不变 d.v逆(D)=v正(B)
(4)1200℃时反应C(g)+D(g)![]() A(g)+B(g)的平衡常数的值为________。
A(g)+B(g)的平衡常数的值为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com