
【题目】已知 A、B、D、H 是中学化学中常见的单质,其中 A、D 为气体,J 为蓝色溶液。转化关系如下(部分生成物及反应条件已略去):
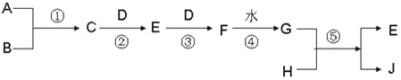
(1)若 B 为气体时,当用玻璃棒分别蘸取 C、G 的浓溶液并使它们靠近时,有白烟生成。则
①请写出下列物质的化学式C__________,F______________。
②在溶液中,检验白烟中阳离子的方法__________________。
(2)若B为固体时,已知 E 是一种常见的空气污染物,且将 C 与 E 混合可生成淡黄色固体 B,写出 G 与 H 反应的化学方程式_____,简述检验气体E的方法_____。
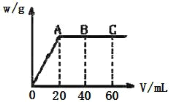
(3)若G 分别是HNO3 和H2SO4,取两者的混合溶液 10 mL,加入0.25molL﹣1Ba(OH)2 溶液时,生成沉淀的质量 w(g)和 Ba(OH)2 溶液的体积 V(mL)的关系如图所示(C 点混合液呈中性)。则原混合液中 H2SO4 的物质的量浓度为_________mol·L-1,HNO3 的物质的量浓度为_____________mol·L-1。
【答案】NH3 NO2 取少量溶液于试管,加入氢氧化钠溶液并加热,试管口湿润红色石蕊试纸变蓝,含有 NH4+(其他合理答案即可) Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O 通入品红溶液,使其褪色(其他合理答案即可) 0.5 2
CuSO4+SO2↑+2H2O 通入品红溶液,使其褪色(其他合理答案即可) 0.5 2
【解析】
A、B、D、H是中学化学中常见的单质,J为蓝色溶液,应含有铜离子,根据各物质的转化关系,
(1)若A、B均为气体时,当用玻璃棒分别蘸取C、G的浓溶液并使它们靠近时,有白烟生成,应为HCl或HNO3和NH3的反应生成NH4Cl,由于C连续与单质D反应后又与水反应生成G,则C为NH3,D为O2,E为NO,F为NO2,G为HNO3,A、B应为氮气和氢气,硝酸与铜反应生成硝酸铜和NO,所以H为Cu,J为Cu(NO3)2;
(2)若A为气体,B为固体时,已知C在D中完全燃烧可生成E和水,E是一种常见的空气污染物,且将C与E混合可生成淡黄色固体B,则A为H2,B为S,C为H2S,D为O2,E为SO2,F为SO3,G为H2SO4,浓硫酸与铜反应生成硫酸铜和SO2,所以H为Cu,J为CuSO4,据此答题。
(3)根据图像以及反应方程式进行计算。
A、B、D、H是中学化学中常见的单质,J为蓝色溶液,应含有铜离子,根据各物质的转化关系,
(1)若A、B均为气体时,当用玻璃棒分别蘸取C、G的浓溶液并使它们靠近时,有白烟生成,应为HCl或HNO3和NH3的反应生成NH4Cl,由于C连续与单质D反应后又与水反应生成G,则C为NH3,D为O2,E为NO,F为NO2,G为HNO3,A、B应为氮气和氢气,硝酸与铜反应生成硝酸铜和NO,所以H为Cu,J为Cu(NO3)2,
①根据上面的分析可知,C为NH3,F为NO2,故答案为:NH3,NO2。
②有白烟生成,是因为生成了氯化铵,在溶液中,检验铵根离子的方法为:取少量溶液于试管中,加入氢氧化钠溶液并加热,在试管口能使湿润的红色石蕊试纸变蓝,说明含有NH4+,故答案为:取少量溶液于试管中,加入氢氧化钠溶液并加热,在试管口能使湿润的红色石蕊试纸变蓝,说明含有NH4+。
(2)若A为气体,B为固体时,已知C在D中完全燃烧可生成E和水,E是一种常见的空气污染物,且将C与E混合可生成淡黄色固体B,则A为H2,B为S,C为H2S,D为O2,E为SO2,F为SO3,G为H2SO4,浓硫酸与铜反应生成硫酸铜和SO2,所以H为Cu,J为CuSO4,G与H反应的化学方程式为Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O,检验气体SO2的方法是将气体体SO2通入品红溶液,溶液褪色,加热后恢复红色,证明E是SO2,
CuSO4+SO2↑+2H2O,检验气体SO2的方法是将气体体SO2通入品红溶液,溶液褪色,加热后恢复红色,证明E是SO2,
故答案为:Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O;将气体体SO2通入品红溶液,溶液褪色,加热后恢复红色,证明E是SO2。
CuSO4+SO2↑+2H2O;将气体体SO2通入品红溶液,溶液褪色,加热后恢复红色,证明E是SO2。
(3)由图像可知,0~20mL氢氧化钡溶液发生H2SO4+Ba(OH)2=BaSO4↓+2H2O,即加入20mL氢氧化钡溶液时,硫酸钡沉淀量达到最大,则根据反应方程式可知硫酸的物质的量为:n(H2SO4)=n[Ba(OH)2]=0.25mol/L×0.020L=0.005mol,硫酸的物质的量浓度为0.005mol÷0.01L=0.5mol/L,


 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的数值,下列叙述中正确的是( )
A. 28g以任意比组成的CO与N2混合气体中含有原子数为2NA
B. 将100mL0.1mol/L的FeCl3溶液滴入沸水中可制得Fe(OH)3胶粒数目为0.01 NA
C. 在H2O2 + Cl2 =2HCl + O2反应中,每生成32g氧气,则转移4NA个电子
D. 1L 1 mol/L 的盐酸中有NA 个HCl分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是
a | b | c | |
① | Cu | CuO | Cu(OH)2 |
② | CH3CH2OH | CH3CHO | CH2=CH2 |
③ | S | SO3 | H2SO4 |
④ | NO | NO2 | HNO3 |
⑤ | FeCl2 | Fe | FeCl3 |

A. ②⑤ B. ③④ C. ④⑤ D. ①⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要配制0.50 mol·L-1NaCl溶液480 mL。按下列操作步骤填上适当的文字,以使整个操作完整。
(1)选择仪器。完成本实验所必需的仪器有:托盘天平(精确到0.1 g)、药匙、烧杯、玻璃棒、________、________以及等质量的两片滤纸。
(2)计算。配制该溶液需取NaCl晶体________g。
(3)称量。
①天平调平之后,应将天平的游码调至某个位置,请在下图中用一根竖线标出游码左边缘所处的位置:

②称量过程中NaCl晶体应放于天平的________(填“左盘”或“右盘”)。
③称量完毕,将药品倒入烧杯中。
(4)溶解、冷却,该步实验中需要使用玻璃棒,目的是_________________。
(5)转移、洗涤。在转移时应使用________引流,需要洗涤烧杯2~3次是为了_____________。
(6)定容,摇匀。
(7)将配好的溶液静置一段时间后,倒入指定的试剂瓶,并贴好标签,注明配制的时间、溶液名称及浓度。
(8)在配制过程中,某学生观察定容时液面情况如图所示,所配溶液的浓度会________(填“偏高”、“偏低”或“无影响”)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年6月8日,国际纯粹与应用化学联合会(IUPAC)宣布,将合成化学元素第118号(Og)提名为化学新元素。该新元素由美国劳伦斯利弗莫尔国家实验室和俄罗斯的科学家联合合成 ,为向极重元素合成先驱者、俄罗斯物理学家尤里·奥加涅相致敬,研究人员将第118号元素命名为oganesson(缩写Og),中文名称为![]() 。已知 原子的相对原子质量为293,核电荷数为118,其核内中子数和核外电子数分别为( )
。已知 原子的相对原子质量为293,核电荷数为118,其核内中子数和核外电子数分别为( )
A. 118 175 B. 118 118 C. 193 118 D. 175 118
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)![]() 的系统命名为___________________;
的系统命名为___________________;
(2)有机物的结构可用“键线式”简化表示,CH3-CH=CH-CH3的键线式为________;
(3)分子式为C2H4O2的有机物,其中有两种同分异构体:乙酸(CH3COOH)、甲酸甲酯(HCOOCH3),则通过下列方法,不可能将二者区别开来的是 (_______)
A.红外光谱法 B. 元素定量分析法 C.质谱法 D.与NaHCO3溶液反应
(4)已知乙烯分子是平面结构, 1,2-二氯乙烯可形成![]() 和
和![]() 两种不同的空间异构体,称为顺反异构。下列能形成类似上述空间异构体的是(_______)
两种不同的空间异构体,称为顺反异构。下列能形成类似上述空间异构体的是(_______)
A.1-丙烯 B.4-辛烯 C.1-丁烯 D.2-甲基-1-丙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列反应式,据两式判断,下列各组离子中,还原性由强到弱的排列顺序正确的是( )
(1)2Fe3++2I—=2Fe2++I2(2)Br2+2Fe2+=2Fe3++2Br—
A.Br—>Fe2+>I—B.I—>Fe2+>Br—C.Br—>I—>Fe2+D.Fe2+>I—>Br—
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com