
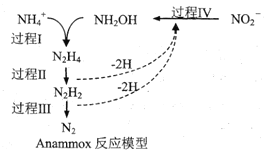
【题目】厌氧氨化法(Anammox)是一种新型的氨氮去除技术,下列说法中正确的是( )
A.![]() 所含的质子总数为
所含的质子总数为![]() (设NA为阿伏加德罗常数的值)
(设NA为阿伏加德罗常数的值)
B.![]() 中含有σ键和π键
中含有σ键和π键
C.过程IV中,![]() 发生氧化反应
发生氧化反应
D.该方法每处理![]() ,需要
,需要![]()
科目:高中化学 来源: 题型:
【题目】锂—铜空气燃料电池是低成本高效电池。该电池通过一种复杂的铜“腐蚀”现象产生电能,其中放电过程为2Li+Cu2O+H2O===2Cu+2Li++2OH-。下列说法不正确的是
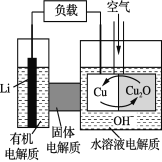
A. 放电时,Li+透过固体电解质向Cu极移动
B. 通空气时,铜被腐蚀,产生Cu2O
C. 放电时,正极的电极反应式为:Cu2O+2H+ +2 e- ===2Cu+H2O
D. 整个反应过程中,氧化剂为O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汉黄芩素是传统中草药黄芩的有效成分之一,对肿瘤细胞的杀伤有独特作用。下列有 关汉黄芩素的叙述正确的是
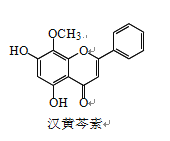
A. 汉黄芩素的分子式为 C16H13O5
B. 该物质遇 FeCl3 溶液显色
C. 1 mol 该物质与溴水反应,最多消耗 1 mol Br2
D. 与足量 H2 发生加成反应后,该分子中官能团的种类减少 1 种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砷(As)是第四周期ⅤA族元素,可以形成As2O3、As2O5、H3AsO3、H3AsO4等化合物,有着广泛的用途。回答下列问题:
(1)画出砷的原子结构示意图____________。
(2)工业上常将含砷废渣(主要成分为As2S3)制成浆状,通入O2氧化,生成H3AsO4和单质硫。写出发生反应的化学方程式________。该反应需要在加压下进行,原因是________。
(3)已知:As(s)+![]() H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+![]() O2(g)=H2O(l) ΔH2
O2(g)=H2O(l) ΔH2
2As(s)+![]() O2(g) =As2O5(s) ΔH3
O2(g) =As2O5(s) ΔH3
则反应As2O5(s) +3H2O(l)= 2H3AsO4(s)的ΔH =_________。
(4)298 K时,将20 mL 3x mol·L1 Na3AsO3、20 mL 3x mol·L1 I2和20 mL NaOH溶液混合,发生反应:AsO33(aq)+I2(aq)+2OH![]() AsO43(aq)+2I(aq)+ H2O(l)。溶液中c(AsO43)与反应时间(t)的关系如图所示。
AsO43(aq)+2I(aq)+ H2O(l)。溶液中c(AsO43)与反应时间(t)的关系如图所示。

①下列可判断反应达到平衡的是__________(填标号)。
a.溶液的pH不再变化
b.v(I)=2v(AsO33)
c. c (AsO43)/c (AsO33)不再变化
d. c(I)=y mol·L1
②tm时,v正_____ v逆(填“大于”“小于”或“等于”)。
③tm时v逆_____ tn时v逆(填“大于”“小于”或“等于”),理由是_____________。
④若平衡时溶液的pH=14,则该反应的平衡常数K为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于柠檬酸(如图)的性质推测的叙述错误的是
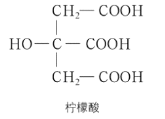
A.柠檬酸可与 NaHCO3 溶液反应生成 CO2
B.柠檬酸分子中具有羟基官能团,因此可与NaOH 溶液反应
C.家里可以用柠檬酸除水垢
D.柠檬酸分子中的两种官能团都能跟金属钠反应生成氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式为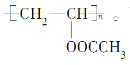 下列叙述正确的是
下列叙述正确的是
A. 1 mol该有机物与NaOH溶液完全反应时,消耗1 mol NaOH
B. 该有机物可通过加聚反应生成
C. 该有机物水解所得的产物能发生加成反应
D. 该有机物分子的单体为两种
查看答案和解析>>
科目:高中化学 来源: 题型:
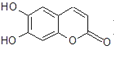
【题目】中草药秦皮中含有的七叶树内酯(每个折点表示一个碳原子,氢原子未画出),具有抗菌作用。若1 mol七叶树内酯分别与浓溴水、NaOH溶液和足量氢气完全反应,则消耗的Br2 、NaOH和H2的物质的量分别为
A. 1 mol Br2;2 mol NaOH;1 mol H2
B. 3 mol Br2;4 mol NaOH;1 mol H2
C. 2 mol Br2;3 mol NaOH;4 mol H2
D. 3 mol Br2;4 mol NaOH;4 mol H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某菱镁矿主要成分是MgCO3,还含有Al2O3、FeCO3、Fe2O3、SiO2等杂质,由该菱镁矿制备高纯MgO的流程如图。回答下列问题:
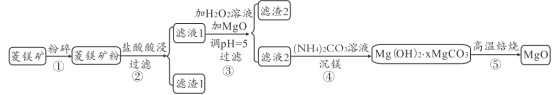
(1)将矿石粉碎的目的是_____,滤渣1的成分是_____
(2)步骤③先加入足量H2O2溶液,再加MgO调节溶液pH=5,加入足量的H2O2溶液后发生的所有氧化还原反应的方程式为_____
(3)滤渣2的成分是_____,1mol该滤渣用3mol/L硫酸溶解,需消耗硫酸_____mL
(4)列举沉镁之后的滤液的一种用途_____,称取14.2g的![]() 在_____(填仪器名称)中进行高温焙烧得到的MgO质量为8.0g,则x=_____。
在_____(填仪器名称)中进行高温焙烧得到的MgO质量为8.0g,则x=_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物甲的结构简式为:![]() ,它可以通过下列路线合成(分离方法和其他产物已经略去)
,它可以通过下列路线合成(分离方法和其他产物已经略去)

(1)写出 反应银氨溶液反应的化学方程式_____。
反应银氨溶液反应的化学方程式_____。
(2)写出甲发生聚合反应的化学方程式_____。
(3)步骤 I 和 IV 在合成甲过程中的目的是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com