
汽车的启动电源常用铅蓄电池,该电池在放电时的反应如下:
Pb (s)+ PbO2(s) +2H2SO4(aq) 2PbSO4(s) +2H2O(l),根据此反应判断下列叙述中正确的是( )
2PbSO4(s) +2H2O(l),根据此反应判断下列叙述中正确的是( )
| A.PbO2是电池的负极 |
| B.负极的电极反应式为:Pb(s)+SO42-(aq)–2e – = PbSO4(s) |
| C.铅蓄电池属于一次电池 |
| D.电池放电时,溶液酸性增强 |
科目:高中化学 来源: 题型:单选题
高铁电池是电动汽车首选的电池之一,该电池的工作原理为:3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH,下列关于该电池放电时的说法中正确的是 ( )
3Zn(OH)2+2Fe(OH)3+4KOH,下列关于该电池放电时的说法中正确的是 ( )
| A.高铁电池产生的电流从负极经外电路到达正极 |
| B.正极反应式为Zn+2OH-—2e - =Zn(OH)2 |
| C.负极pH减小,正极pH增大,电解液pH增大 |
| D.每氧化1mol高铁酸钾转移3mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
Cu—Zn稀硫酸组成原电池装置,当导线中有0.5mol电子通过时,理论上两极的变化是
①锌极反应:Zn-2e-=Zn2+,锌片上产生0.25mol的H2
②铜极反应:2H++2e-=H2↑,锌片溶解16.25g
③电流由铜极经导线流向锌极 ④溶液中SO42-移向铜极
| A.①④ | B.③④ | C.②③ | D.①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
如图所示,两电极一为碳棒,一为铁片,若电流表的指针发生偏转,且a极上有大量气泡生成,则以下叙述正确的是:( )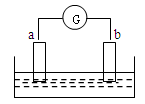
| A.a为负极,是铁片,烧杯中的溶液为硫酸 |
| B.b为负极,是铁片,烧杯中的溶液为硫酸铜溶液 |
| C.a为正极,是碳棒,烧杯中的溶液为硫酸 |
| D.b为正极,是碳棒,烧杯中的溶液为硫酸铜溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
利用电解法可将含有Fe、Zn、Ag、Pt等杂质的粗铜提纯,下列叙述正确的是
| A.电解时以精铜作阳极 |
| B.电解时阴极发生还原反应 |
| C.粗铜连接电源负极,其电极反应是Cu =Cu2+ + 2e- |
| D.电解结束,电解槽底部会形成含少量Ag、Pt等金属的阳极泥 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
(8分)可以将氧化还原反应2H2+O2=2H2O设计成原电池。
(1)利用H2、O2、HCl溶液构成燃料电池,则正极的电极反应式为_________________________
___________;负极的电极反应式为__________________________________。
(2)把H2改成CH4,KOH溶液作电解质,则负极的电极反应式为________________________
_____________,当导线中通过4 mol电子时,需消耗______mol的KOH;将4 mol CH4完全与Cl2发生取代反应,并生成等物质的量的四种氯代物,则理论上需要消耗Cl2的物质的量为_______mol。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某MCFC型燃料电池可同时供应电和水蒸汽,其工作温度为600℃~700℃,所用燃料为氢气,电解质为熔融的K2CO3。该电池的总反应为:2H2+O2=2H2O,负极电极反应式为: H2+CO32——2e— H2O+CO2。则下列判断中正确的是
H2O+CO2。则下列判断中正确的是
| A.放电时CO32—向负极移动 |
| B.放电时CO32—向正极移动 |
| C.正极反应: 4OH——4e—=2H2O+O2↑ |
| D.当电池中生成1 mol水时,转移4 mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
航天器中常使用可充电电池,构造示意图如图(氢化物电极为储氢金属,可看做H2直接参加反应)。白天太阳能帆板发电,将一部分电量储存在镍氢电池里,夜晚镍氢电池供电。下列说法正确的是( )
| A.在使用过程中此电池要不断补充水 |
| B.放电时NiOOH在电极上发生氧化反应 |
| C.充电时阴极区电解质溶液pH升高 |
| D.充电时阴极反应为Ni(OH)2-e-+OH-= NiOOH+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com