
在1 L溶液中含有Fe(NO3)3和H2SO4两种溶质,其浓度分别为0.2 mol?L-1和1.5
mol?L-1,现向该溶液中加入39.2 g铁粉使其充分反应。下列有关说法正确的是( )
A.反应后溶液中Fe3+物质的量为0.8 mol
B.反应后产生13.44 L H2(标准状况)
C.反应后溶液中Fe2+和Fe3+物质的量之和为0.9 mol
D.由于氧化性Fe3+>H+,故反应中先没有气体产生后产生气体
C
【解析】
试题分析: 39.2g的铁粉的物质的量是0.7mol,原溶液中铁离子、氢离子、硝酸根离子的物质的量0.2mol、3mol、0.6mol,氧化性为HNO3>Fe3+>H+,则铁先与硝酸反应,
Fe+4H++NO3-═Fe3++NO↑+2H2O
1 4 1 1
0.6 2.4 0.6 0.6
Fe+2Fe3+═3Fe2+,
1 2 3
0.1 0.2 0.3
Fe完全反应,没有剩余,溶液中存在0.6molFe3+、0.3molFe2+。A、反应后溶液中Fe3+物质的量为0.6mol,错误;B.该过程中不发生Fe+2H+═Fe2++H2↑,没有氢气生成,错误;C.反应后溶液中存在0.6molFe3+、0.3molFe2+,反应后溶液中Fe2+和Fe3+物质的量之和为0.9mol,正确;D.氧化性为HNO3>Fe3+>H+,先发生Fe+4H++NO3-═Fe3++NO↑+2H2O,有气体生成,错误;
考点:考查铁的化学性质和铁的计算


科目:高中化学 来源:2015届河南省偃师市高三上学期第一次月考化学试卷(解析版) 题型:选择题
铝合金在日常生活、建筑装潢、航空航天和汽车制造等方面均有着广泛的用途。下列关于铝合金具有广泛用途的分析不正确的是
A.铝元素在地壳中的含量高,储量丰富
B.铝容易形成致密的氧化膜,抗腐蚀性能好
C.铝化学性质稳定,常温下不与任何酸碱反应
D.铝的冶炼技术基本成熟,可以大量生产
查看答案和解析>>
科目:高中化学 来源:2015届河北省“五个一名校联盟”高三教学质量监测(一)化学试卷(解析版) 题型:填空题
【化学—选修5:有机化学基础】(15分)
有机化合物J是治疗心脏病药物的一种中间体,分子结构中含有3个六元环。其中一种合成路线如下:
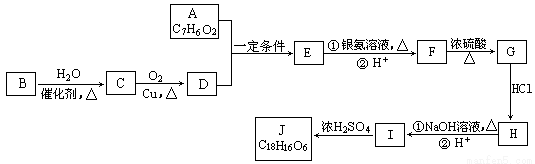
已知:
①A既能发生银镜反应,又能与FeCl3溶液发生显色反应,其核磁共振氢谱显示有4种氢,且峰面积之比为1︰2︰2︰1。
②有机物B是一种重要的石油化工产品,其产量可用来衡量国家的石油化工发展水平。
③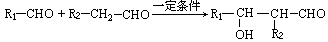
回答以下问题:
(1)A中含有的官能团名称是。
(2)写出有机反应类型B→C,F→G,I→J。
(3)写出F生成G的化学方程式 。
(4)写出J的结构简式。
(5)E的同分异构体有多种,写出所有符合以下要求的E的同分异构体的结构简式
。
FeCl3溶液发生显色反应 ②能发生银镜反应 ③苯环上只有两个对位取代基 ④能发生水解反应。
查看答案和解析>>
科目:高中化学 来源:2015届河北省“五个一名校联盟”高三教学质量监测(一)化学试卷(解析版) 题型:选择题
用石墨电极电解CuCl2溶液(见下图)。下列分析正确的是

A.a端是直流电源的负极
B.通电使CuCl2发生电离
C.阳极上发生的反应:Cu2++2e-=Cu
D.通电一段时间后,在阴极附近观察到黄绿色气体
查看答案和解析>>
科目:高中化学 来源:2015届河北省“五个一名校联盟”高三教学质量监测(一)化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.沼气和水煤气都是可再生能源
B.石油裂解和油脂皂化都有高分子生成小分子的过程
C.不能用植物油萃取溴水中的溴
D.可以用加热使蛋白质变性的方法分离提纯蛋白质
查看答案和解析>>
科目:高中化学 来源:2015届河北正定中学上学期高三第一次考试化学试卷(解析版) 题型:选择题
某碱金属R与其氧化物R2O的混合物2.16g,跟足量水充分反应后,将所得溶液蒸干,得固体3.2 g,由此判定金属是( )
A.锂 B.钠 C.钾 D.铷
查看答案和解析>>
科目:高中化学 来源:2015届河北正定中学上学期高三第一次考试化学试卷(解析版) 题型:选择题
把有机物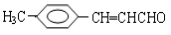 氧化为
氧化为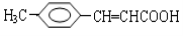 ,所用氧化剂最合理的是( )
,所用氧化剂最合理的是( )
A.O2 B.酸性KMnO4 C.银氨溶液 D.溴水
查看答案和解析>>
科目:高中化学 来源:2015届江西省高三暑期化学试卷(解析版) 题型:填空题
(8分)(一)下列各组离子在指定溶液中一定能大量共存的是___________________。
①无色溶液中:K+、Na+、MnO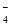 、SO
、SO
②甲基橙呈黄色的溶液中:I-、Cl-、NO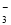 、Na+
、Na+
③石蕊呈蓝色的溶液中:Na+、AlO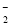 、NO
、NO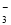 、HCO
、HCO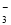
④在pH=1的溶液中:Fe2+、NO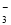 、SO
、SO 、Na+
、Na+
⑤在pH=0的溶液中:Na+、NO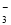 、SO
、SO 、K+
、K+
⑥在pH=12的溶液中:K+、Cl-、HCO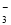 、Na+
、Na+
⑦含大量OH-的溶液中:CO 、Cl-、F-、K+
、Cl-、F-、K+
⑧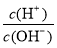 =1012的溶液中:NH
=1012的溶液中:NH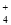 、Al3+、NO
、Al3+、NO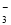 、Cl-
、Cl-
⑨加入Al能放出H2的溶液中:Cl-、HCO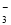 、SO
、SO 、NH
、NH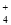
⑩由水电离出的c(OH-)=10-14 mol/L的溶液中:Ca2+、K+、Cl-、HCO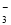
?c(Fe3+)=0.1 mol/L的溶液中:K+、ClO-、SO 、SCN-
、SCN-
?含大量Al3+的溶液中:K+、Na+、NO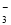 、ClO-
、ClO-
(二)三氟化氮(NF3)是一种新型电子材料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,请根据要求回答下列问题:
(1)反应过程中,被氧化与被还原的元素原子的物质的量之比为____________。
(2)写出该反应的化学方程式_____________________________________。
(3)NF3是一种无色、无臭的气体,但一旦NF3在空气中泄漏,还是易于发现.你判断该气体泄漏时的现象是_______________________________________。
(4)一旦NF3泄漏,可以用NaOH溶液喷淋的方法减少污染,其产物除NaNO2、NaF、H2O外,还肯定有______________________________(填化学式)。
查看答案和解析>>
科目:高中化学 来源:2015届江西省第一学期高三第一次月考化学(A卷)试卷(解析版) 题型:填空题
“温室效应”是哥本哈根气候变化大会研究的环境问题之一。CO2是目前大气中含量最高的一种温室气体。因此,控制和治理CO2是解决“温室效应”的有效途径。
(1)下列措施中,有利于降低大气中CO2浓度的有 (填字母)。
a.采用节能技术,减少化石燃料的用量 b.鼓励乘坐公交车出行,倡导低碳生活
c.利用太阳能、风能等新型能源替代化石燃料
(2)一种途径是将CO2转化成有机物实现碳循环。如:
2CO2(g)+2H2O(l)=C2H4(g)+3O2(g) △Hl=+1411.0 kJ/mol
2CO2(g)+3H2O(l)=C2H5OH(l)+3O2(g) △H2=+1366.8 kJ/mol
则由乙烯水化制乙醇的热化学方程式是 。
(3)在一定条件下,6H2(g)+2CO2(g) CH3CH2OH(g)+3H2O(g)。
CH3CH2OH(g)+3H2O(g)。
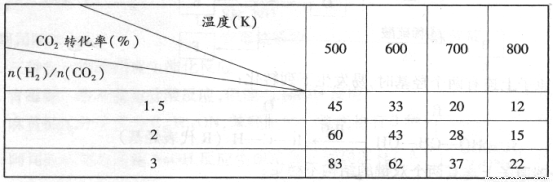
根据上表中数据分析:
①温度一定时,提高氢碳比[n(H2)/n(CO2)],CO2的转化率 (填“增大”“减小”或“不变”)。
②该反应的正反应为 (填“吸”或“放”)热反应。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com