
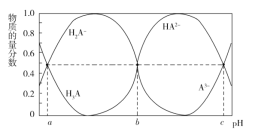
【题目】某三元羧酸 H3A 在表面活性剂、洗涤剂、润滑剂等方面具有重要的地位。常温时,向 10 mL 0.01 mol·L1 的 H3A 溶液中滴入 0.01 mol·L1 的 NaOH 溶液,H3A、H2A、HA2、A3的物质的量分数与溶液的 pH 的关系如 图所示。下列说法错误的是( )
A.该温度下,H3A 的电离常数 Ka1=10a
B.若 b=7,加入 20 mL NaOH 溶液时,溶液的 pH<7
C.NaOH 溶液的体积为 30 mL 时,溶液中:c(OH)=3c(H3A)+2c(H2A)+c(HA2)+c(H+)
D.反应 2H2A![]() H3A+HA2在该温度下的平衡常数K=10a-b
H3A+HA2在该温度下的平衡常数K=10a-b
【答案】B
【解析】
由图像可知pH<a时,溶液中存在H3A和H2A-,且c(H3A)>c( H2A-),pH=a时,c(H3A)=c( H2A-),pH=b时c(HA2-)=c( H2A-),pH=c时c(HA2-)=c( A3-),结合溶液中电荷守恒、物料守恒和电离平衡常数进行分析计算。
A.电离常数只与温度有关,H3A的一级电离常数看图像左侧的第一个交点,故Ka1=c(H+),故A正确;
B.加入20 mL NaOH溶液时,溶液中的溶质为Na2HA,位于pH=b=7的右侧,此时溶液的pH>7,故B错误;
C.NaOH溶液的体积为30mL时,物料守恒表达式为![]() ,电荷守恒表达式为
,电荷守恒表达式为![]() ,两式联立可得题中表达式,故C正确;
,两式联立可得题中表达式,故C正确;
D.该反应在此温度下的平衡常数为![]() ,故D正确;
,故D正确;
故答案选:B。


科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | Ⅵ | VⅡA | 0 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ |
(1)在这些元素中,化学性质最不活泼的是___(填元素符号)。
(2)②③⑦三种元素的原子半径从大到小的顺序为___(填元素符号)。
(3)在最高价氧化物的水化物中,酸性最强的化合物的化学式___,碱性最强的化合物的名称___。
(4)元素⑤的氧化物与元素④的最高价氧化物对应水化物反应的化学方程式为:___。
(5)元素⑥和⑦形成的气态氢化物较稳定是___(填化学式),用方程式来说明元素⑦的非金属性比⑥的非金属强的事实___(一个或两个方程式均可)。
(6)表示①与③形成的化合物的电子式___,写出它的一种用途___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)钙钛型复合氧化物可用于制造航母中的热敏传感器,其晶胞结构如图所示,其中A为晶胞的顶点,A可以是Ca、Sr、Ba或Pb,当B是V、Cr、Mn或Fe时,这种化合物具有好的电学性能。下列说法正确的是_____ (填序号)。
A.金属Ca、Sr、Ba采用体心立方堆积
B.用A、B、O表示的钙钛型复合氧化物晶体的化学式为ABO3
C.在制造Fe薄片时,金属键完全断裂
D.V、Cr、Mn、Fe晶体中均存在金属阳离子和阴离子

(2)辽宁号航母飞行甲板等都是由铁及其合金制造的。铁有δ、γ、α三种同素异形体,其晶胞结构如图所示。
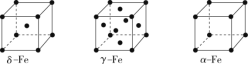
①γ—Fe晶胞中含有的铁原子数为_____。—
②δ—Fe、α—Fe两种晶体中铁原子的配位数之比为_____。
③若α—Fe晶胞的边长为acm,γ—Fe晶胞的边长为bcm,则两种晶体的密度之比为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
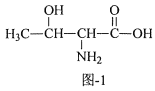
【题目】配合物X{[Cu(phen)(Thr)(H2O)]ClO4}能够通过插入或部分插入的模式与DNA作用,它可由Cu(ClO4)2、HThr(结构简式如图l所示)、phen等为原料制备。
(1)Cu2+基态电子排布式为___。
(2)ClO4-的空间构型为__(用文字描述),与ClO4-互为等电子体的一种分子的化学式为___。
(3)HThr分子中,碳原子的杂化类型为___;1molHThr中含有σ键的数目为___。
(4)配合物X中配离子的结构如图2所示,则配位原子为___(填元素符号)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁铝合金10.2g溶于50mL4 mol/L的盐酸溶液中,若加入2mol/LNaOH溶液,使得溶液中的沉淀达到最大值,则需要加入氢氧化钠溶液的体积为
A.0.2LB.0.5LC.0.8LD.0.1L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸溶液中存在电离平衡:CH3COOH![]() H++CH3COO,下列叙述不正确的是
H++CH3COO,下列叙述不正确的是
A.升高温度,平衡正向移动,醋酸的电离常数Ka增大
B.0.10 mol/L的CH3COOH溶液加水稀释,溶液中c(OH-)增大。
C.CH3COOH溶液中加少量的CH3COONa固体,平衡逆向移动
D.25℃时,欲使醋酸溶液的pH、电离常数Ka和电离程度都减小,可加入少量冰醋酸。
查看答案和解析>>
科目:高中化学 来源: 题型:
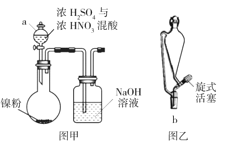
【题目】硫酸镍(NiSO4)是电镀镍工业所用的主要镍盐,易溶于水。下图为某兴趣小组设计的在实验室中
制备 NiSO46H2O 的装置。
回答下列问题:
(1)实验室中配制浓 H2SO4 与浓 HNO3 混酸的操作为______。
(2)图甲中仪器 a 的名称为__________,有同学认为将仪器 a 换作图乙中的仪器 b 效果更好,其理由 为______。
(3)混酸与镍粉反应时,除生成 NiSO4 外,还生成了 NO2、NO 和 H2O,若 NO2 与 NO 的物质的量之比为 1∶1,则该反应的化学方程式为______。从反应后的溶液中得到 NiSO46H2O 的操作有_____和过滤、洗涤、干燥。
(4)该小组同学查阅资料发现用镍粉与混酸制备 NiSO4 成本高,用冶铁尾矿提取的草酸镍(NiC2O4)与硫酸制取 NiSO4 成本较低。反应原理为:NiC2O4![]() NiO+CO↑+CO2↑,NiO+H2SO4===NiSO4+H2O(已知 PdCl2溶液能够吸收 CO)。现加热 NiC2O4 制备 NiO,并检验生成的 CO,可能用到的装置如下:
NiO+CO↑+CO2↑,NiO+H2SO4===NiSO4+H2O(已知 PdCl2溶液能够吸收 CO)。现加热 NiC2O4 制备 NiO,并检验生成的 CO,可能用到的装置如下:
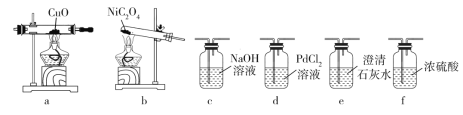
①各装置的连接顺序为:_____→______→_______→ f →_____→_____→_____。(填装置 标号,可重复使用)
②能够说明生成 CO 的现象有______。
③PdCl2 溶液吸收 CO 时产生黑色金属单质和 CO2 气体,该反应其他产物的化学式为______________________。
(5)将 NiSO46H2O 制成电镀液时往往加入少量稀硫酸,其目的是___________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常见含硫物质A~D,在生活、生产中有着广泛应用,它们之间的转化关系如下图所示。其中反应①、②中所需物质B溶液的浓度不同。
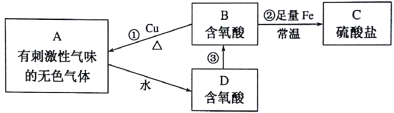
请按要求回答下列问题:
(1)A的化学式为_______。
(2)反应①、②中Cu、Fe所起的作用相同,即都作_______(填“氧化剂”或“还原剂”),你判断的依据是它们都是金属,在反应中都_______。
(3)反应②的离子方程式为_______。
(4)大气中因废气A引起酸雨的反应流程之一可用下图示意:
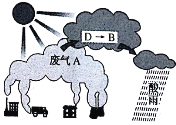
上图中由D→B的转化所需氧化剂为_______。
当将含D的雨水敞口放置一段时间后(忽略溶液体积、温度的变化),其c(H+)将_______。(填“增大”“减小”或“不变”)。废气A是一种重要的化工原料,常采用氨吸收法进行循环利用、变废为宝。某工厂若将4.48×106L(标准状况下)废气A进行环保处理,完全转化为 NH4HSO3时,需消耗10mol/L氨水溶液(溶质全部以NH3H2O计)的体积为_______L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物F可用于某抗凝血药的制备,工业生成F的一种路线图如下(其中H与FeCl3溶液能发生显色反应):
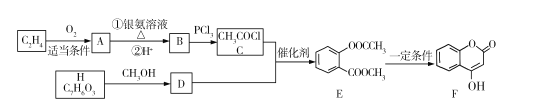
回答下列问题:
(1)A的名称是 ___,E中的官能团是名称是____。
(2)B→C的反应类型是 ___,F的分子式为____。
(3)H的结构简式为 ___。
(4)E与NaOH溶液反应的化学方程式为 ___。
(5)同时满足下列条件的D的同分异构体共有____种,写出核磁共振氢谱有5组峰的物质的结构简式 ___
①是芳香族化合物
②能与NaHCO3溶液反应
③遇到FeCl3溶液不显色
④1mol该物质与钠反应时最多可得到1molH2
(6)以2氯丙酸、苯酚为原料制备聚丙烯酸苯酚酯(![]() ),写出合成路线图(无机试剂自选)_________。
),写出合成路线图(无机试剂自选)_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com