
| A�� | ԭ�Ӱ뾶�Ĵ�С˳��r��B����r��C����r��D�� | |
| B�� | Ԫ��B��E������������ˮ���ﶼ��ǿ�� | |
| C�� | C��D�������ﶼ�����������Ʒ�Ӧ | |
| D�� | ��ҵ�ϳ��õ��Ԫ��C��D���Ȼ�������ȡ���ǵĵ��� |
���� ����������Ԫ��A��B��C��D��E��ԭ���������ε�����DԪ�صĵ��ʼ��������ᷴӦҲ����NaOH��Һ��Ӧ����DΪAl��
Eԭ�ӵ�������������Bԭ���ڲ��������3������Cԭ��������������3����E����������С��8����B�ڲ������Ϊ2��E����������Ϊ6��Eԭ����������D������EΪSԪ�أ�
C����������Ϊ2��Cԭ������С��D��B��C��Eԭ�ӵ�����������֮��Ϊ13����B����������Ϊ5������BΪNԪ�ء�CΪMgԪ�أ�A�ĵ����ڳ����³���̬����AΪHԪ�أ�
ͨ�����Ϸ���֪��A��B��C��D��E�ֱ���H��N��Mg��Al��SԪ�أ�
A��ԭ�ӵ��Ӳ���Խ����ԭ�Ӱ뾶Խ��ͬһ����Ԫ�أ�ԭ�Ӱ뾶����ԭ�������������С��
B��B��E����������ˮ����ֱ�����������
C��C��D��������ֱ��Ǽ���������������������������ͼ���Һ����Ӧ��
D���Ȼ����Ƿ��Ӿ��壬����״̬�²����磮
��� �⣺����������Ԫ��A��B��C��D��E��ԭ���������ε�����DԪ�صĵ��ʼ��������ᷴӦҲ����NaOH��Һ��Ӧ����DΪAl��
Eԭ�ӵ�������������Bԭ���ڲ��������3������Cԭ��������������3����E����������С��8����B�ڲ������Ϊ2��E����������Ϊ6��Eԭ����������D������EΪSԪ�أ�
C����������Ϊ2��Cԭ������С��D��B��C��Eԭ�ӵ�����������֮��Ϊ13����B����������Ϊ5������BΪNԪ�ء�CΪMgԪ�أ�A�ĵ����ڳ����³���̬����AΪHԪ�أ�
ͨ�����Ϸ���֪��A��B��C��D��E�ֱ���H��N��Mg��Al��SԪ�أ�
A��ԭ�ӵ��Ӳ���Խ����ԭ�Ӱ뾶Խ��ͬһ����Ԫ�أ�ԭ�Ӱ뾶����ԭ�������������С������r��B����r��D����r��C������A����
B��B��E����������ˮ����ֱ�����������ᣬ�������ᶼ��ǿ�ᣬ��B��ȷ��
C��C��D��������ֱ��Ǽ���������������������������ͼ���Һ����Ӧ������������ͼ���Һ��Ӧ����C����
D���Ȼ����Ƿ��Ӿ��壬����״̬�²����磬��ҵ�ϲ��õ�������������ķ���ұ��Al����D����
��ѡB��
���� ���⿼��ԭ�ӽṹ��Ԫ�������ɣ�Ϊ��Ƶ���㣬���ؿ���ѧ�������жϼ�֪ʶ�ۺ�Ӧ���������漰Ԫ���ƶϡ�Ԫ�������ɡ��������ʡ�����ұ����֪ʶ�㣬ע�����������ǿ�������ұ��������ϵ���״�ѡ����D��


 ѧ�ڸ�ϰһ��ͨѧϰ�ܶ�Ա��ĩ������ӱ����������ϵ�д�
ѧ�ڸ�ϰһ��ͨѧϰ�ܶ�Ա��ĩ������ӱ����������ϵ�д� â���̸����������������ϵ�д�
â���̸����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
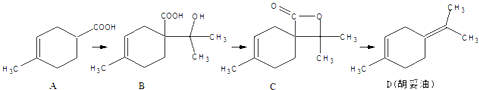
| A�� | ���л���A���������ϩ��C5H8���ͱ�ϩ�ᣨC3H4O2�����ȵõ��ģ���÷�Ӧ�ķ�Ӧ��������ȡ����Ӧ | |
| B�� | �л���D����������̼ԭ��һ������ | |
| C�� | �л���C������ͬ���칹���в����з����廯������� | |
| D�� | �л���B���ܸ�Na��Ӧ�ų�H2�����ܸ�NaHCO3��Һ��Ӧ�ų�CO2���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ���渽�Ű�ˮ��̼�ظ��ڿ�������Ҫ�������ⸯʴ | |
| B�� | ��ӦNH3��g��+HCl��g��?NH4Cl ��s���ġ�H��0����S��0 | |
| C�� | 25��ʱ��pH=11�İ�ˮ��pH=3������������ϣ�������Һ��pH��7 | |
| D�� | ��2NH3��g��?N2��g��+3H2��g����ƽ����ϵ�м��������NH3��ƽ��ת�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
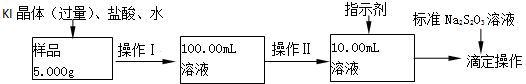
| A�� | $\frac{2a-4b}{V}$ | B�� | $\frac{2��a-b��}{V}$ | C�� | $\frac{a-2b}{V}$ | D�� | $\frac{2a-b}{V}$ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �⻯��ķе�Y��R��X | B�� | ����������R��X | ||
| C�� | X��Y�����ܹ��������ӻ������� | D�� | ԭ�Ӱ뾶Z��R��X��Y |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com