
【题目】关于元素周期表,下列叙述中不正确的是 ( )
A. 在金属元素与非金属元素的分界线附近可以寻找制备半导体材料的元素
B. 在过渡元素中可以寻找制备催化剂及耐高温和耐腐蚀的元素
C. 在非金属元素区域可以寻找制备新型农药材料的元素
D. 在地球上元素的分布和它们在元素周期表中的位置有密切关系
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)具有极强的氧化性,可作为水处理剂和高容量电池材料.
(1)FeO42﹣与水反应的方程式为4FeO42﹣+10H2O4Fe(OH)3+8OH﹣+3O2↑,K2FeO4在处理水的过程中所起的作用有;
(2)与MnO2﹣Zn电池类似,K2FeO4﹣Zn也可以组成碱性电池,K2FeO4在电池中作为正极材料,其电极反应式为;
(3)将适量K2FeO4配制成c(FeO42﹣)=1.0×10﹣3molL﹣1(1.0mmolL﹣1)的试样,FeO42﹣在水溶液中的存在形态如图所示.下列说法正确的是(填字母) 
A.不论溶液酸碱性如何变化,铁元素都有4种存在形态
B.改变溶液的pH,当溶液由pH=10降至pH=4的过程中,HFeO4﹣的分布分数先增大后减小
C.向pH=8的这种溶液中加KOH溶液,发生反应的离子方程式为:H2FeO4+OH﹣=HFeO4﹣+H2O
D.pH约为2.5 时,溶液中H3FeO4+和HFeO4﹣比例相当
(4)HFeO4﹣═H++FeO42﹣的电离平衡常数表达式为K,其数值接近(填字母).
A.10﹣2.5
B.10﹣6
C.10﹣7
D.10﹣10
(5)25℃时,CaFeO4的Ksp=4.536×10﹣9 , 若要使100mL,1.0×10﹣3molL﹣1的K2FeO4溶液中的c(FeO42﹣ )完全沉淀(一般认为离子浓度小于1×10﹣5molL﹣1时上为完全沉淀),则理论需控制溶液中Ca2+浓度至少为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某铁矿石(若只含铁的氧化物和SiO2)取36g溶于过量的稀盐酸中,过滤、洗涤、干燥后得5.6g不溶物,向得到的滤液中加入足量的NaOH溶于,过滤、洗涤后将沉淀灼烧,得32g红棕色固体.根据题意下列结论不正确的是( )
A.由铁矿石转化为红棕色固体的过程中发生了氧化还原反应
B.溶于盐酸后得到的滤液中n(Fe2+):n(Fe3+)=1:1
C.铁矿石中的铁的氧化物的化学式一定是Fe3O4
D.若稀盐酸为3.0molL﹣1 400mL,反应前后体积变化忽略不计,则滤液中剩余H+的物质的量浓度是0.5molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某“化学鸡尾酒”通过模拟臭虫散发的聚集信息素可高效诱捕臭虫,其中一种组分T可通过下列反应路线合成(部分反应条件略). 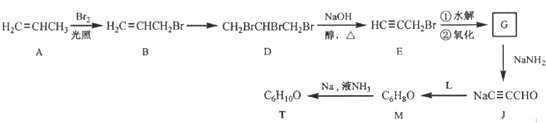
(1)A的化学名称是 , A→B新生成的官能团是;
(2)D的核磁共振氢谱显示峰的组数为 .
(3)D→E的化学方程式为 .
(4)G与新制的Cu(OH)2发生反应,所得有机物的结构简式为 .
(5)L可由B与H2发生加成反应而得,已知R1CH2Br+NaC≡CR2→R1CH2C≡CR2+NaBr,则M的结构简式为 .
(6)已R3C≡CR4 ![]()
![]() ,则T的结构简式为 .
,则T的结构简式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验现象所对应的离子方程式不正确的是( )
实 验 | 现 象 | 离子方程式 | |
A |
| 在空气中放置一段时间后,溶液呈蓝色 | 4H++4I﹣+O2═2I2+2H2O |
B |
| 溶液由浅绿色变为红色 | 2Fe2++Cl2═2Fe3++2Cl﹣、 |
C |
| 溶液由黄绿色变为无色 | Cl2+2OH﹣═Cl﹣+ClO﹣+H2O |
D |
| 有白色沉淀生成,溶液由红色变为无色 | Ba2++OH﹣+H++SO |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种气态烷烃和一种气态烯烃的混合物9g,其密度是相同条件下氢气密度的11.25倍,当混合气体通过足量溴水时,溴水增重4.2g,则这两种气态烃是( )
A.甲烷和乙烯
B.乙烷和乙烯
C.甲烷和丙烯
D.甲烷和丁烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列推理正确的是( )
A. 铝粉在氧气中燃烧生成Al2O3,故铁丝在氧气中燃烧生成Fe2O3
B. 铁能从硫酸铜溶液中置换出铜,故钠也能从硫酸铜溶液中置换出铜
C. 活泼金属钠保存在煤油中,故活泼金属铝也保存在煤油中
D. 钠与氧气、水等反应时钠均作还原剂,故金属单质参与反应时金属均作还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学科研小组的同学在精确测试Na2SO3溶液的pH时,遇到了困惑.为此,他们进行了冷静的思考和准备,决心重新实验,揭开奥秘.请你了解情况,参与交流讨论.
[查阅资料]①常温下0.1molL﹣1的H2SO3溶液的pH约为2.1.
②通常情况下,H2S为无色,有腐蛋臭味的气体,其水溶液称为氢硫酸.常温下0.1molL﹣1的H2S溶液的pH约为4.5.
[实验操作]①准确称取纯净的Na2SO37H2O晶体25.20g,配成1L水溶液,测得其pH=7.8.
②以坩埚再次准确称取25.20g上述晶体,继而隔绝空气在600℃以上高温下强热至恒重(只有硫元素的化合价变化成最高价和最低价),质量为12.60g.
③将②所得之12.60g固体进行元素定性定量分析,组成与Na2SO3无异.将其溶于水得250mL溶液,测得pH=10.3.
[分析猜想]Na2SO37H2O在强热下,失去结晶水,进而发生了分解反应(自身氧化还原反应)
[交流讨论]
(1)实验操作②中除坩埚、酒精灯、三角架及隔绝空气的设备外,还需要的仪器有 .
(2)给Na2SO37H2O加热时要隔绝空气,请以简要的文字和化学方程式给以说明. .
(3)猜想Na2SO3在高温强热下发生分解反应的化学方程式是 .
(4)实验①和③中,两次测得的溶液pH相差明显,其合理的解释是 . 实验③中溶液的pH=10.3的原理是(以相关的离子方程式表示) .
(5)请你设计简单的实验方案,给上述分析、猜想及解释以佐证.请简单叙述实验步骤、现象和结论. .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com