
����Ŀ��ij�¶��������������εij����ܽ�ƽ��������ͼ��ʾ��ͼ��X2-��ʾCO32-��SO42-����MSO4�������ᣬ�����й�˵��������ǣ� ��
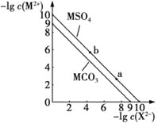
A.MSO4�ı�����Һ��c(M2+)=1��10-5molL-1
B.MCO3(s)+SO42-(aq)![]() MSO4(s)+CO32-(aq)��ƽ�ⳣ��KΪ10
MSO4(s)+CO32-(aq)��ƽ�ⳣ��KΪ10
C.�������ŨNa2CO3��Һ�п��ܽ�MSO4ת��ΪMCl2
D.��a�㺬MSO4�ķ�ɢϵ�м���M(NO3)2�������ϵ�п���ת��Ϊb��ķ�ɢϵ

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��[��ѧһ�л���ѧ����]��13�֣�
�Զ��ױ���Ӣ������p-xylene����дΪPX���ǻ�ѧ��ҵ����Ҫԭ�ϡ�
��1��д��PX�Ľṹ��ʽ ��
��2��PX �ɷ����ķ�Ӧ�� �� ���Ӧ���ͣ���
��3�����ܼ���DEHP����������ͼ��ʾ��ת����ϵ������A ��PX��һ��ͬ���칹�塣
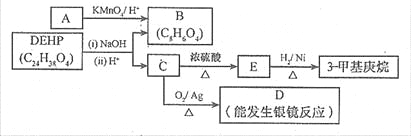
�� B �ı����ϴ���2 �ֲ�ͬ��ѧ��������ԭ�ӣ���B �Ľṹ��ʽ�� ��
�� D ���������������� �������ƣ���
�� C ������1��̼ԭ�������һ�����������DEHP�Ľṹ��ʽ��
��4��F ��B ��һ��ͬ���칹�壬��������������
a.�DZ�����λ��ȡ���b.��FeCl3��Һ��ʾ������ɫ��c.����̼��������Һ��Ӧ��
д��F ��NaHCO3��Һ��Ӧ�Ļ�ѧ����ʽ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ά����C��һ��ˮ����ά���أ���ˮ��Һ�����ԣ������ķ���ʽ��C6H8O6��ά����C�ױ������е����������������ʵ�ˮ�����߲ˣ�����Ʒ�ж�������ά����C�������ʳ�֭��ά����C�ĺ���Ϊ500mg��L��1���ҡ�ijУ����С��ⶨ��ijƷ�Ƶ�����װ��֭��ά����C�ĺ����������Dzⶨ������ʵ�鱨�棺
��1���ⶨĿ�ģ��ⶨXX������װ��֭��ά����C�ĺ�����
��2���ⶨԭ����C6H8O6+ I2 �� C6H6O6+ 2H++ 2I����
��3��ʵ����Ʒ��
��ʵ����������ʽ�ζ��ܣ�����̨����ƿ���ιܵȡ�
���Լ���ָʾ��__________�������ƣ���7.5��10-3mol��L��1����Һ������ˮ��
��4��ʵ�鲽�裺
��ϴ�����������ζ����Ƿ�©ˮ����ϴ�ú�װ�ñ���Һ��
�ڴ�����װ��֭��Ŀ����ɫ���Ȼ�ɫ������Ⱥã�������ʽ�ζ�������ƿ������20.00ml�����֭������2��ָʾ����
�������ֿ��Ƶζ��ܵ�___________���λ��������ҡ����ƿ���۾�ע����ƿ����Һ��ɫ�ı仯ֱ���ζ��յ㣬�жϵζ��յ��������__________________��
���¶��������ظ��������Ρ�
��5�����ݼ�¼�������������ݴ������ζ������ı�����Һ�������15.00ml����˳�֭��ά����C�ĺ���Ϊ_________mg��L��1��
��6���������ʵ���д������в��������л�ʹά����C�ĺ���ƫ�͵���________
A. ��ȡ�����֭������ˮϴ��δ��ϴ
B. ��ƿˮϴ��δ�ô���Һ��ϴ
C. �ζ�ǰ���첿����һ���ݣ��ζ��յ�ʱ��ʧ
D. �ζ�ǰ���Ӷ������ζ����Ӷ���
��7�����ñ�������Һ�ζ�δ֪Ũ�ȵ�NaOH��Һ�����ü�����ָʾ������ָʾ�����������������Χ�ڣ�����Ȼ�ᵼ�²��Ũ�ȱ�ʵ��ֵ_________������ƫ��������ƫС����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�������£�Ksp.(ZnS)=1.6��10��24��pM=��lgc(M2+)(MI2+ΪCu2+��Zn2+)�������£���10 mL 0.10 mol/L CuCl2��Һ�еμ�0.10 mol/L Na2S��Һ���μӹ�����pM��Na2S��Һ���(V)�Ĺ�ϵ��ͼ��ʾ������˵���������( )
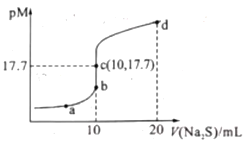
A.Ksp(CuS)��������Ϊ10-36
B.a����Һ�У�c(Na+)=2[c(S2��)+c(HS��)+c(H2S)]
C.d����Һ�У�c(Na+)>c(Cl��)>c(S2��)>c(H+)
D.��ͬ�����£����õ�Ũ�ȵ������ZnCl2��Һ��������CuCl2��Һ����Ӧ�յ�c��b�����ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮΪ�ܼ������к͵ζ���ԭ���ǣ�H3O++OH-��2H2O����֪Һ̬SO2�ʹ�ˮ�ĵ������������ΪҺ̬SO2Ҳ�ᷢ������⣺SO2��l��+SO2��l��![]() SO32-+SO2+������Һ̬SO2Ϊ�ܼ�����SOCl2�ζ�Cs2SO3������������������� �� ��
SO32-+SO2+������Һ̬SO2Ϊ�ܼ�����SOCl2�ζ�Cs2SO3������������������� �� ��
A. �õζ���Ӧ���Ա�ʾΪ��SO32-+ SO2+��2SO2
B. ��һ���¶��£�Һ̬SO2��c��SO32-����c��SO2+���ij˻���һ������
C. �����Ĵ��ڣ�˵��SO2�����ӻ�����
D. ��ͨ�����������仯���ж��Ƿ�ζ��յ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E�Ǻ˵�������������5�ֶ���������Ԫ�أ�ԭ�Ӱ뾶��D��E��B��C��A˳�����μ�С��B��E��ͬ����Ԫ�ء�
��1�������ƶ���ȷ����________��
a A��B��E��������ͬһ����
b A��B��C������ͬһ����
c C������������ˮ��������Լ���
d C��D�ĵ��ʿ����������ӻ�����
��2����A��Dͬ���壬B���ǽ���Ԫ�أ�����һ�ֵ����ǵ�������壬Cԭ�ӵ�������������A��B�������������ܺͻ���1�����A��CԪ�ذ�ԭ�Ӹ�����1:1�γɵĻ�����F�ĵ���ʽΪ______��F����__________���ӣ����������������Ǽ�������
����A��B��C��D��Ԫ�ذ�ԭ�Ӹ�����1:1:3:1�γɵĻ�����Ϊ_________������A��C��D�γɵĻ�������ˮ��Һ�з�Ӧ�����ӷ���ʽΪ_______;
��E�����ڱ��е�λ�� ______ C��E�γɵĻ���������_____����
����A��B��CԪ���е����ֻ����ֿ�����ɶ��ַ��ӣ����к���18�����ӵķ�����____���ѧʽ����
��B��C��E�⻯��ķе��ɸߵ���Ϊ__________,��˵��ԭ�� _____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���õ�ⷨ���ᴿ����ijЩ����������ʵĴ�KOH��Һ���乤��ԭ����ͼ��ʾ�������й�˵���������

A. ͨ���������������ҺpH������
B. ������ӦʽΪ4OH��-4e����2H2O+O2��
C. ������KOH��Һ��b���ڵ���
D. K+ͨ������Ĥ������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾװ���У�a��b���Ƕ��Ե缫��ͨ��һ��ʱ���b��������Һ����ɫ������˵���в���ȷ����( )
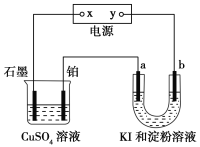
A��x��������y�Ǹ��� B��a������������b������I2
C��a����Pt�缫�������ݲ��� D��U�ι�����Һ�ļ�����ǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������(H2C2O4)�Ƕ�Ԫ���ᣬNaHC2O4��Һ�����ԡ������£���10 mL 0.01 mol/L NaHC2O4��Һ�еμ�0.01 mol/L NaOH��Һ������NaOH��Һ��������ӣ���Һ������Ũ�ȹ�ϵ�������( )
A.V(NaOH) = 0ʱ��c(H��) >1��10��7mol/L
B.V(NaOH)��10 mLʱ�����ܴ���c(Na��) = 2c(C2O42-)��c(HC2O4- )
C.V(NaOH) = 10 mLʱ����Һ��pHΪ9����10-9= 10-5-2c(H2C2O4)-c(HC2O4-)
D.V(NaOH)��10 mLʱ�����ܴ���c(OH- )��c(Na��)��c(C2O42-)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com